Clear Sky Science · ru
Натуральные пептидные продукты, нацеленные на ClpC1, по‑разному нарушают протеом Mycobacterium tuberculosis
Почему нарушение клеточной «уборки» бактерий важно
Туберкулез по‑прежнему остаётся одним из самых смертоносных инфекционных заболеваний в мире, и штаммы Mycobacterium tuberculosis с устойчивостью к препаратам усложняют лечение. Большинство существующих антибиотиков атакуют клеточную стенку бактерии или её способность вырабатывать энергию и копировать генетический материал. В этом исследовании рассматривается совершенно иная уязвимость: внутренняя «уборочная бригада» клетки, поддерживающая здоровье белков. Поняв, как новые молекулы на основе природных продуктов нарушают эту систему, учёные надеются разработать будущие лекарства, которые смогут убивать возбудителя туберкулёза новыми и более стойкими способами.
Центр по уходу за белками в клетке
Как и все живые клетки, бактерия туберкулёза постоянно синтезирует, сворачивает, ремонтирует и перерабатывает свои белки. Центральную роль в этой сети «уборки» белков играет крупный аппарат — комплекс ClpC1–ClpP1P2. Одна его часть (ClpC1) действует как шаперон, распознавая и втягивая повреждённые или ненужные белки, а другая (ClpP1P2) разрезает их на фрагменты для повторного использования. Эта система жизненно важна для выживания бактерии, особенно при стрессовых условиях, таких как повышение температуры или воздействие антибиотиков. Несколько природных пептидных соединений — экумицин, иламицины (руфомицины) и цикломарины — уже известны своим связыванием с ClpC1 и выраженной активностью против туберкулёза, что делает этот комплекс перспективной мишенью для лекарств. 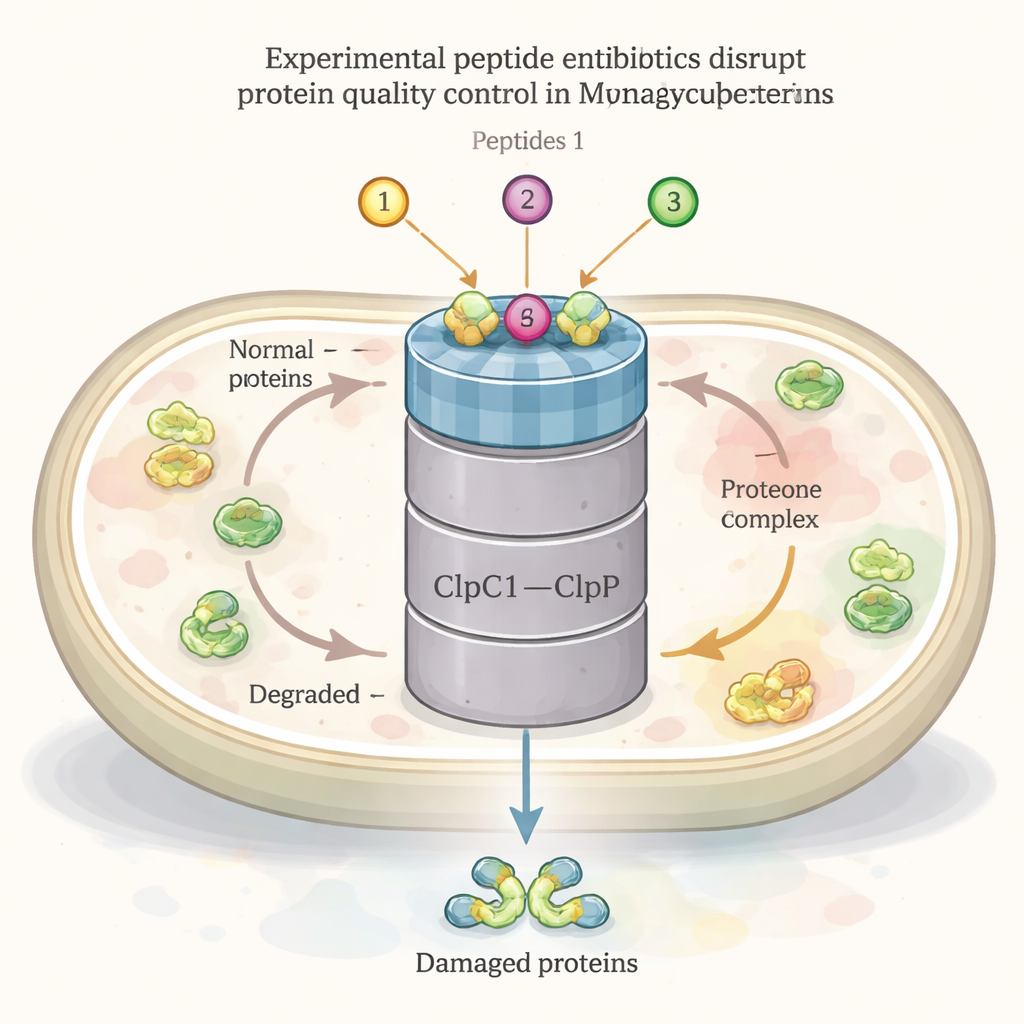
Три родственных препарата — три разных эффекта
Исследователи изучили по одному представителю каждой из трёх семейств пептидов: аналог экумицина (Ecu*), иламицин E (IlaE) и производное цикломарина (дезоксцикломарин, dCym). Несмотря на то, что все три связываются с одной и той же областью ClpC1, они по‑разному ведут себя внутри клетки. С помощью количественного протеомного анализа — подхода, позволяющего одновременно измерять тысячи белков — учёные обнаружили, что Ecu* вызвал наибольшее нарушение: значительные изменения уровней почти 17% всех белков бактерии. IlaE изменял около 12%, а dCym — примерно 7%. Лишь 72 белка стабильно затрагивались всеми тремя соединениями, и большинство из них уменьшились в абундансе. Это показывает, что каждое вещество переводит аппарат ClpC1 в своё «настроенное» состояние, перестраивая белковый ландшафт клетки по‑разному, а не просто «выключая» машину.
Забивание шредера против отключения питания
Чтобы поставить эти эффекты в контекст, команда сравнила пептиды с бортезомибом, противораковым препаратом, который широко блокирует ферменты деградации белков. У бактерий туберкулёза бортезомиб вызывал общее накопление многих белков, как и ожидалось при полном отключении «шредеров». Напротив, пептиды породили более избирательные паттерны: некоторые известные мишени ClpC1 накапливались, другие истощались, и не наблюдалось повсеместного подавления всех путей деградации белков. Детальные лабораторные тесты с очищенными компонентами показали, что каждый пептид по‑разному меняет обработку конкретных субстратов. Например, все три мешали уничтожению одного регуляторного белка (PanD), но только Ecu* блокировал распад модели неструктурированного белка, а только dCym нарушал деградацию стресс‑защищающего белка Hsp20. Эти различия указывают на то, что общая форма и гибкость каждой мишени влияют на то, как она пострадает, когда ClpC1 «неправильно настроен» данным соединением. 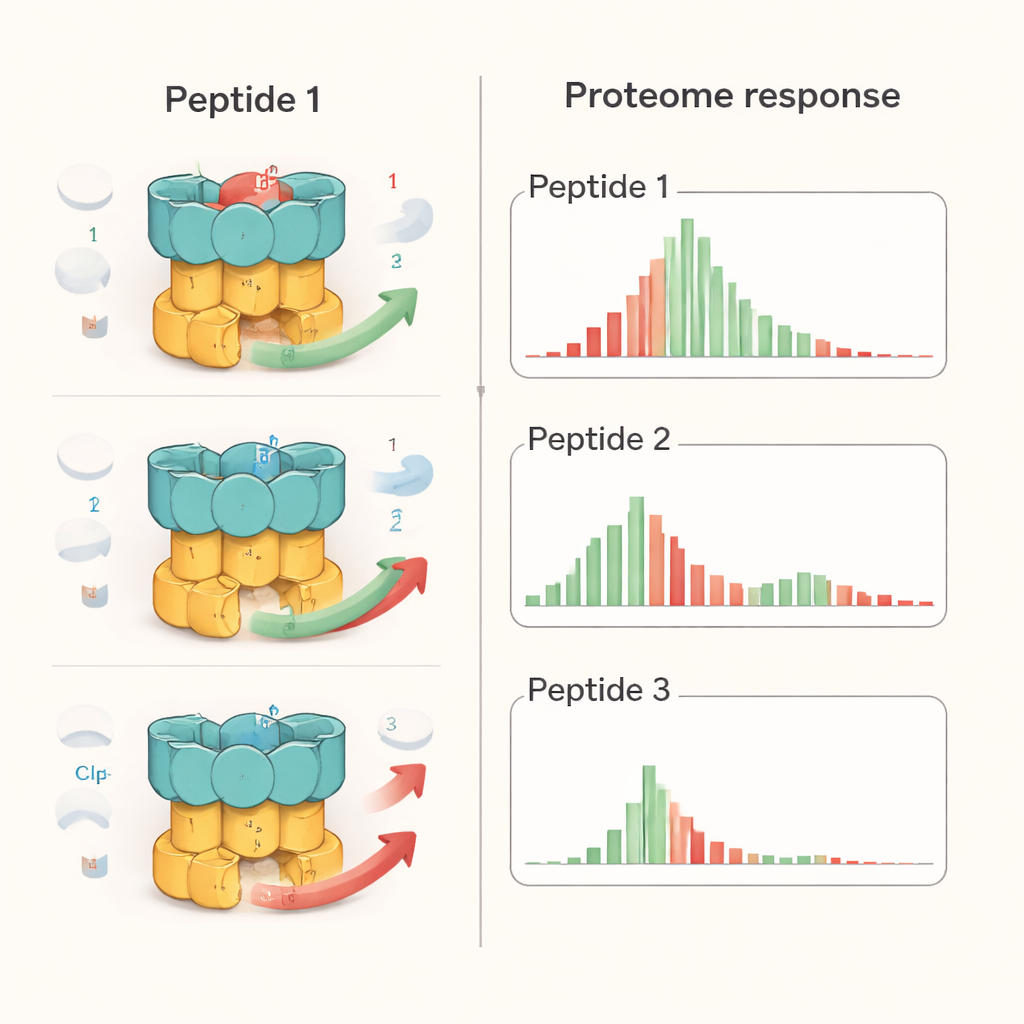
Ответы на стресс и самоспасение бактерии
Бактерия туберкулёза обладает резервными системами, которые включаются, когда повреждения белков перегружают основную «уборочную» машину. Одна из таких систем включает другой шаперон, ClpC2, который может связывать молекулы типа цикломарина и ослаблять их влияние на ClpC1. В исследовании показали, что хотя все три пептида способны связываться с ClpC2 в пробирке, только производное цикломарина (dCym) действительно повышало уровни ClpC2 в живых бактериях и становилось более мощным при экспериментальном снижении ClpC2. Напротив, Ecu* и IlaE оставались эффективными даже при ослаблении ClpC2, что говорит о том, что они во многом обходят этот путь самоспасения. Команда также обнаружила сильную, специфичную для соединения связь с Hsp20 — небольшим белком, помогающим предотвращать вредные агрегаты: Ecu* (и в меньшей степени IlaE) вызывал драматическое увеличение уровней Hsp20, а Ecu* непосредственно связывался с Hsp20, раскрывая новую связь между этими кандидатами в лекарства и сетью стресс‑ответа клетки.
Преобразование стресса в терапевтическое преимущество
Поскольку система ClpC1 особенно важна в жёстких условиях, исследователи проверили действие препаратов при лёгком тепловом стрессе, который увеличивает поток неправильно свернутых белков. В этих условиях и Ecu*, и dCym стали значительно более летальными, достигнув токсичности, сравнимой с бортезомибом, несмотря на их более селективный механизм. Это демонстрирует, что прицельное вмешательство в систему контроля качества белков может быть столь же эффективным, как и полное отключение основных протеаз, но с потенциально большей точностью управления. Работа также показала, что многие изменения уровней белков под действием Ecu* не просто отражали изменения в активности генов, подчёркивая, что нарушение ClpC1 в основном влияет на посттрансляционную регуляцию.
Что это значит для будущих методов лечения туберкулёза
Для неспециалистов ключевое послание таково: бактерии туберкулёза зависят от тонко сбалансированной внутренней системы уборки и стресс‑ответа для выживания. Три протестированных здесь природных пептидных производных все нацелены на один центральный аппарат, но переводят его в разные режимы, вызывая разнообразные и высокоспецифичные искажения белкового состава бактерии. Важно, что соединения, подобные экумицину и иламицину, избегают встроенного бактериального механизма спасения, который может ослаблять эффект цикломарина, и при этом эффективно выводят патоген из строя при стрессовых условиях. Эти свойства делают их перспективными остовами для будущих препаратов от туберкулёза, включая дизайнерские молекулы, которые могли бы заставить клетки туберкулёза избирательно разрушать свои жизненно важные белки, или быть использованы в «химерах, нацеленных на белки», для точного направления саморазрушения бактерий.
Цитирование: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Ключевые слова: туберкулез, качество белков, ClpC1, антибиотикорезистентность, натуральные антибиотики