Clear Sky Science · ru
Одновременное эпигеномное профилирование и измерение регуляторной активности с помощью e2MPRA
Чтение скрытых переключателей клетки
Каждая клетка вашего организма несёт по сути одинаковую ДНК, но нервная клетка и печёночная клетка ведут себя совершенно по-разному. Секрет кроется в коротких участках ДНК, которые действуют как регуляторы яркости для генов, повышая, понижая или выключая их. В этом исследовании представлен мощный новый инструмент под названием e2MPRA, который позволяет учёным одновременно тестировать тысячи таких переключателей, наблюдая при этом, как ДНК упакована и помечена внутри клетки — ключевые шаги на пути к пониманию развития, риска заболеваний и того, почему одни генетические варианты имеют значение, а другие — нет.
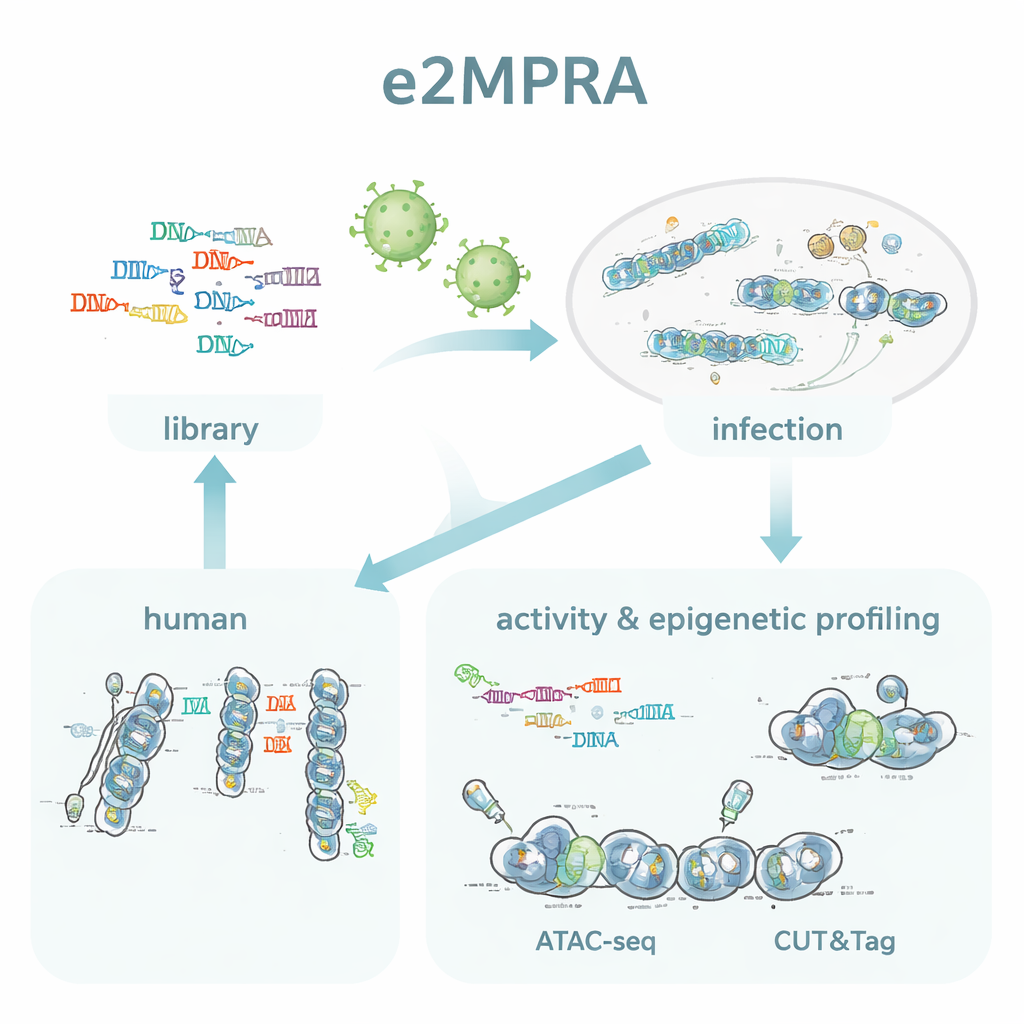
От карт ДНК к функции ДНК
За последнее десятилетие исследователи составили огромные карты «кандидатных» регуляторных элементов, известных как цис-регуляторы. Они используют методы, показывающие, где ДНК слабо упакована (открытая хроматиновая структура), какие белки связаны и какие гистоновые метки окружают участок. Эти карты впечатляют, но в основном носят описательный характер: факт связывания белка или появления метки не доказывает, что последовательность действительно контролирует активность гена. Традиционные массовые параллельные репортерные анализы (MPRA) могут проверять, усиливают ли или подавляют тысячи фрагментов ДНК репортерный ген, но они не сообщают, какие белки там связываются и какие эпигенетические изменения сопутствуют этой активности.
Комбинированный анализ активности и эпигенетических меток
Авторы создали e2MPRA, объединив лентивирусный MPRA с двумя эпигеномными методиками — ATAC-seq и CUT&Tag. Сначала они собирают библиотеку ДНК, в которой каждый кандидат на роль регулятора связан с коротким баркодом и помещён рядом с минимальным промотором и репортерным геном. Эту библиотеку упаковывают в лентивирусы и многократно интегрируют в геномы культивируемых человеческих клеток. Из того же пула клеток считывают баркоды из РНК, чтобы измерить регуляторную активность, и используют ATAC-seq и CUT&Tag для оценки открытости хроматина и ключевой гистоновой метки (H3K27ac) именно в вставленных последовательностях. Нормализуя эти сигналы по частоте интеграции каждой последовательности, они получают параллельные измерения «сильности вкл/выкл» и эпигенетического состояния для тысяч элементов в одном эксперименте.
Расшифровка совместной работы мотивов факторов транскрипции
Чтобы показать, что может выявить эта технология, команда собрала синтетические энхансеры из известных мотивов факторов транскрипции, используемых в печёночных клетках. Они располагали эти мотивы в разном количестве и порядке на нейтральных ДНК-шаблонах. Некоторые факторы, такие как HNF1A и XBP1, вели себя как классические активаторы: увеличение числа копий повышало выход репортера. Другие, например HNF1A и ONECUT1, в основном усиливали доступность хроматина, соответствуя их роли «пионерных» факторов, которые открывают закрытую ДНК. PPARA показал иную картину: он сильно изменял хроматин и гистоновые метки, но сам по себе не вызывал транскрипции, однако в сотрудничестве с другими факторами повышал активность гена. REST, известный репрессор, подавлял активность, когда располагался рядом с активаторами. Поразительно, что простая смена порядка четырёх мотивов могла существенно изменить силу энхансера, а активаторы обычно работали лучше вблизи промотора, выявляя некую грамматику в расположении этих мотивов.
Выявление чувствительных оснований в энхансерах плюрипотентности
Далее исследователи обратились к энхансерам, важным для идентичности стволовых клеток, сосредоточившись на регионах, связаных с факторами плюрипотентности POU5F1 (также называемым OCT4) и SOX2. Они создали плотные библиотеки мутаций, в которых каждая база 100-нуклеотидных энхансеров систематически изменялась, а также небольшие шестибазные окна случайным образом переставлялись. Применяя e2MPRA в индуцированных плюрипотентных стволовых клетках, они могли видеть, какие мутации ослабляли или усиливали репортерную активность и как это отражалось на открытости хроматина и ацетилировании. Нарушение мотива связывания POU5F1::SOX2 часто снижало и активность гена, и эпигенетические метки, подтверждая его центральную роль. В хорошо изученном энхансере рядом с геном POU5F1 они также обнаружили, что изменение мотива YY1 увеличивало транскрипцию, но уменьшало открытие хроматина, намекая на то, что некоторые факторы могут способствовать открытому состоянию, удерживая при этом экспрессию.
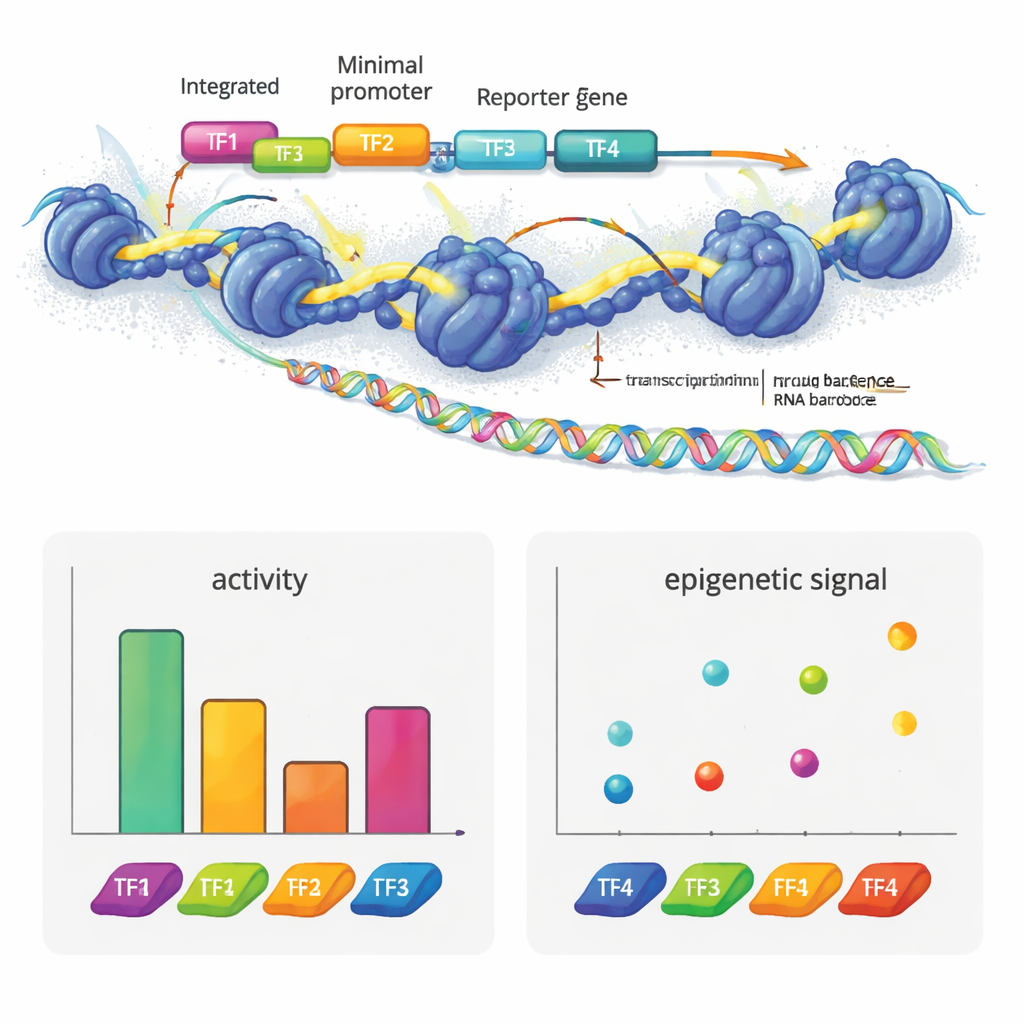
Что это значит для генов и заболеваний
e2MPRA не идеально воспроизводит все нюансы естественной трёхмерной архитектуры генома, но предоставляет практичный способ сравнивать тысячи регуляторных последовательностей и вариантов в одинаковых условиях. Сочетая функциональное считывание (насколько сильно сегмент ДНК активирует ген) с эпигенетическими измерениями (как эта ДНК упакована и помечена), этот метод помогает понять, почему определённые мотивы факторов транскрипции, их комбинации и позиции настолько важны. В перспективе инструменты вроде e2MPRA могут упростить интерпретацию некодирующих генетических вариантов, связанных с заболеваниями, помочь в создании синтетических энхансеров для генной терапии и построить более полный «регуляторный код», связывающий последовательность ДНК с поведением клетки.
Цитирование: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Ключевые слова: регуляция генов, энхансеры, эпигенетика, факторы транскрипции, функциональная геномика