Clear Sky Science · ru
Защитные убиквитиновые E3-лигазы нацеливают ассоциированные с раком деаминазы APOBEC3 на деградацию, чтобы поддерживать целостность генома человека
Защита нашей ДНК от «дружественного огня»
Наши клетки используют мощные ферменты для повреждения вирусной ДНК, помогая отражать инфекции. Но некоторые из этих же ферментов, если их не контролировать, могут случайно повредить собственный геном и способствовать развитию рака. В этом исследовании раскрывается, как человеческие клетки контролируют эти рискованные ферменты, показывая встроенную систему «контроля качества», которая помечает опасные варианты для уничтожения, прежде чем они успеют изменить нашу ДНК.
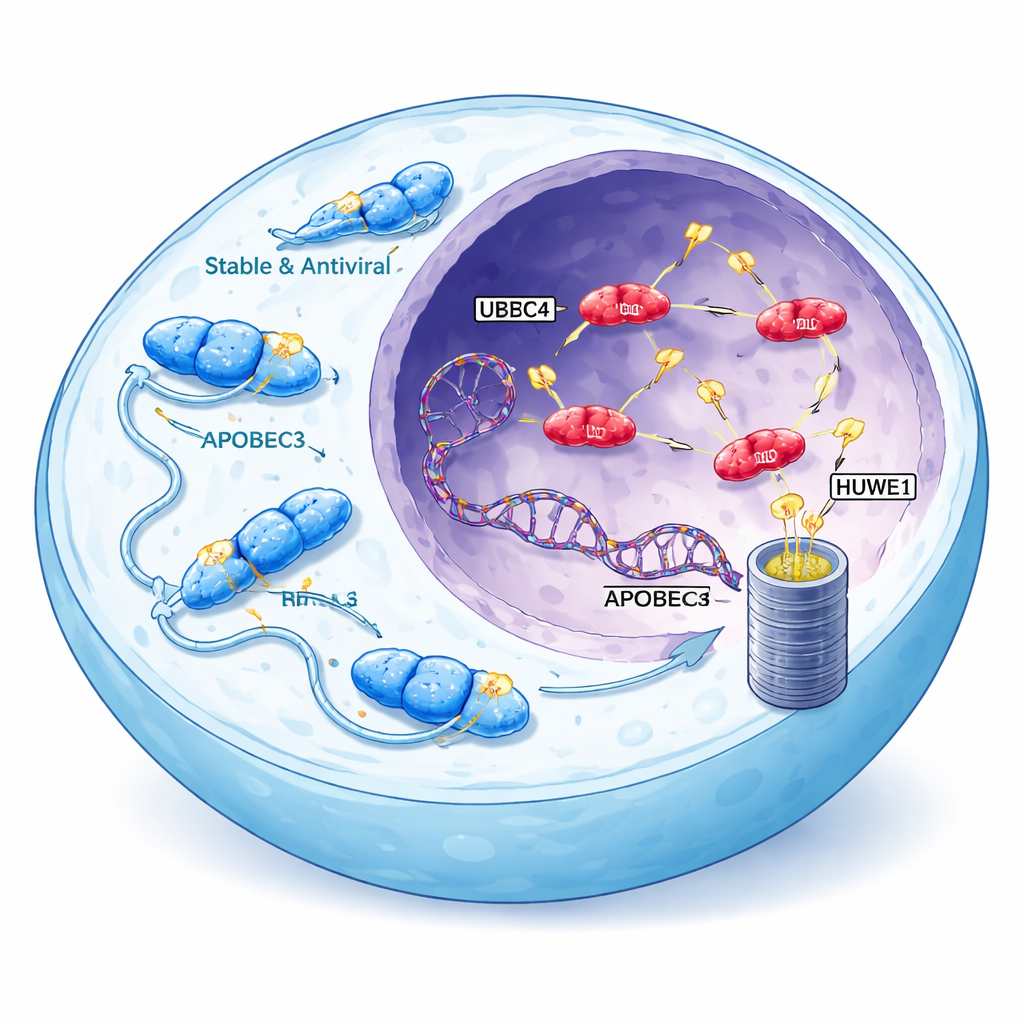
Борцы с вирусами, которые могут обернуться против нас
Семейство ферментов APOBEC3 обычно защищает от вирусов, таких как ВИЧ, химически изменяя вирусную ДНК и вызывая фатальные ошибки. У человека есть семь вариантов APOBEC3, и три из них — A3A, A3B и форма A3H, называемая гаплотипом I (A3H-I) — тесно связаны с паттернами мутаций, наблюдаемыми во многих раках. Эти конкретные ферменты могут проникать в ядро клетки, где находятся хромосомы, и вносить характерные кластеры мутаций в геном. Подписи, связанные с APOBEC, встречаются более чем в половине всех человеческих опухолей, особенно в молочной железе, легких и мочевом пузыре, где они расширяют пул генетических изменений, которыми опухоли могут пользоваться для адаптации и сопротивления лечению.
Почему самые опасные формы удивительно нестабильны
Любопытно, что APOBEC3-ферменты, наиболее сильно связанные с раком, также наименее стабильны. В отличие от своих цитоплазматических собратьев, которые накапливаются в больших количествах и эффективно блокируют вирусы, A3A, A3B и A3H-I быстро разрушаются и обычно присутствуют в ядре в низких концентрациях. Исследователи предположили, что эта нестабильность может быть преднамеренной: если клетки активно ограничивают уровни ядерных APOBEC3-белков, любое нарушение такого контроля может вызвать вспышки мутагенеза. На примере A3H-I они показали, что связанная с раком APOBEC3 в основном уничтожается протеасомой — клеточной «теркой» для белков — после пометки небольшими молекулярными «флажками» убиквитином в нескольких аминокислотных позициях.
Поиск клеточных стражей
Чтобы выявить аппаратуру, ответственную за пометку A3H-I и A3B, команда объединила CRISPR-скрининг с картированием белковых соседств. Они создали клетки, которые по-разному светятся в зависимости от стабильности A3H-I и его безвредного варианта A3H-II, затем систематически нарушали гены, вовлеченные в деградацию белков. Выделились три убиквитиновые лигазы — UBR4, UBR5 и HUWE1. Удаление любой из этих лигаз избирательно повышало уровни нестабильного ядерного A3H-I, не влияя на стабильный цитоплазматический A3H-II. Те же лигазы независимо увеличивали уровни эндогенного A3B в клеточных линиях толстой кишки и иммунных клетках, а одновременное удаление всех трёх давало суммирующее увеличение содержания A3B. Биохимические эксперименты дополнительно показали, что UBR5 и HUWE1 физически связываются с A3B и A3H-I и непосредственно прикрепляют цепочки убиквитина, тогда как UBR4, по-видимому, специализируется на удлинении этих цепочек, делая белки более эффективно утилизируемыми.
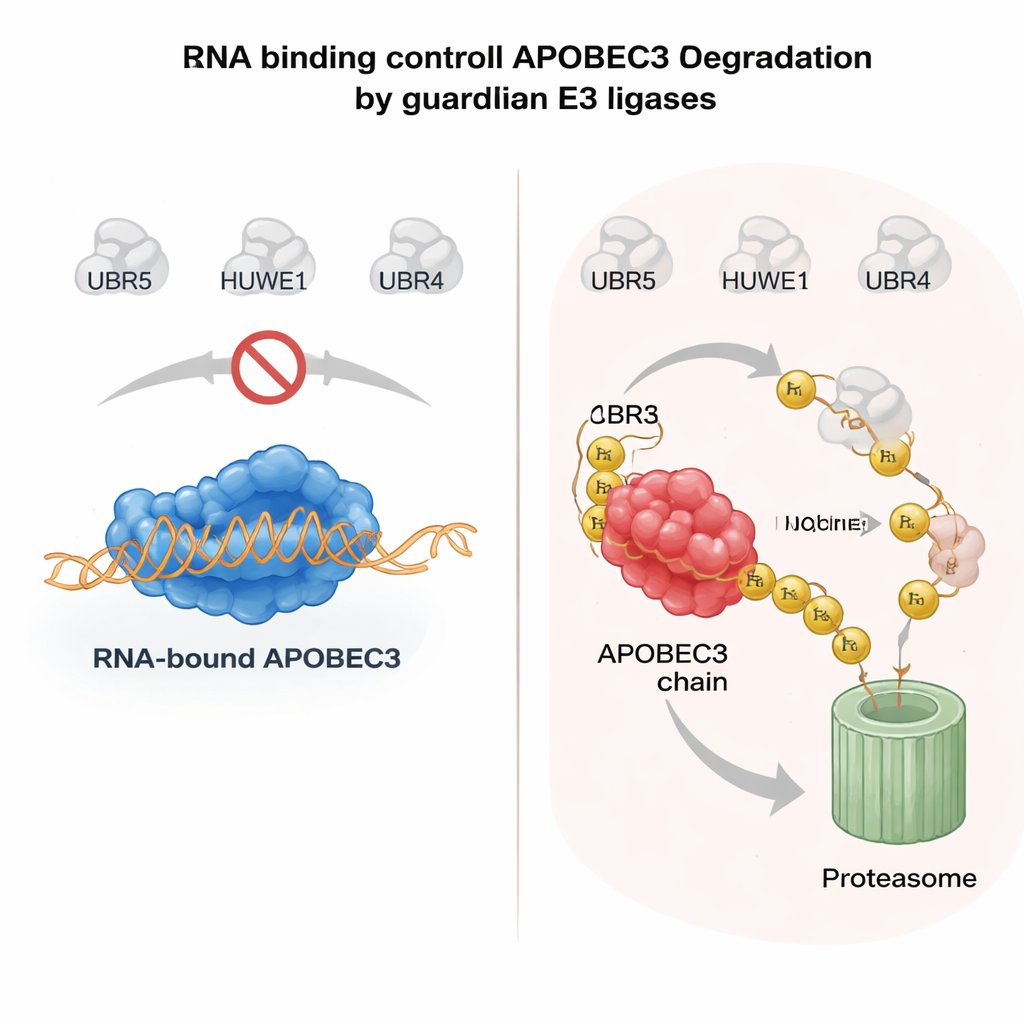
РНК как предохранительный ремень для рискованных ферментов
Что определяет, будет ли фермент APOBEC3 пощажён или уничтожен? Важная подсказка исходила из того, как APOBEC3-белки связываются с молекулами РНК в цитоплазме. Когда A3H или другой участник семейства, A3G, связываются с РНК, они склонны оставаться в крупных комплексах в цитозоле и относительно стабильны. Мутации, ослабляющие связывание с РНК, заставляют эти ферменты перемещаться в ядро, терять защитных партнёров и становиться крайне нестабильными. Авторы показали, что когда APOBEC3-белки не связаны с РНК, UBR5 и HUWE1 распознают открывшиеся поверхности белка, помечают их убиквитином и нацеливают на ядерную деградацию. В очищённых системах добавление РНКазы, удаляющей РНК, значительно усиливало способность этих лигаз связывать и убиквитинировать APOBEC3, что подтверждает роль связывания с РНК как молекулярного щита. Этот механизм позволяет клеткам поддерживать активность антивирусных APOBEC3 в цитоплазме, одновременно быстро очищая любой несвязанный, угрожающий геному пул в ядре.
Когда стражи дают сбой: связь с опухолевыми мутациями
Если UBR4, UBR5 и HUWE1 действуют как стражи, их потеря должна повышать уровень мутаций. Исследователи проверили это, деактивировав каждую лигазу в клетках рака толстой кишки и отслеживая изменения ДНК с течением времени с помощью чувствительного секвенирования, читающего «подписи» мутаций. Удаление этих лигаз, особенно в клетках, экспрессирующих A3H-I, усиливало специфические для APOBEC паттерны мутаций — точно такие же, как в опухолях человека. Расширив анализ на данные пациентов, они изучили тысячи геномов раковых опухолей и обнаружили, что опухоли с мутациями в UBR5 или HUWE1 имели значительно большую долю подписи мутаций, связанной с APOBEC, чем опухоли с интактными лигазами, даже с учётом общего числа мутаций. Это указывает на то, что дефекты в этих «стражевых» лигазах у пациентов могут позволить ассоциированным с раком APOBEC3-ферментам выходить из-под контроля и перестраивать геном опухоли.
Что это значит для будущего лечения рака
Для неспециалиста ключевая мысль такова: наши клетки обладают сложной системой надзора, чтобы предотвратить случайное повреждение собственной ДНК полезными антивирусными ферментами. UBR4, UBR5 и HUWE1 действуют как стражи, которые чувствуют, когда APOBEC3-белки больше не надежно связаны с РНК и, особенно в ядре, отправляют их на клеточную утилизацию. Когда эта система контроля ослаблена — из-за мутаций в лигазах или из‑за препаратов, блокирующих деградацию белков — активность APOBEC3 может подпитывать генетический хаос, который ускоряет эволюцию опухоли и её устойчивость к лечению. Понимание этой сети стражей открывает пути для новых диагностических маркеров, таких как мутации лигаз или уровни APOBEC-белков, и указывает на то, что аккуратная модуляция этого пути может однажды помочь ограничить вредные вспышки мутаций в опухолях, не подрывая наши антивирусные механизмы защиты.
Цитирование: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Ключевые слова: APOBEC3, стабильность генома, убиквитиновая лигаза, канцерогенная мутагенез, деградация белков