Clear Sky Science · ru
Конфигурация концов ДНК определяет формирование синаптического комплекса при NHEJ-опосредованном сближении концов
Когда ДНК ломается, клеткам нужно действовать быстро
Каждый день ДНК в наших клетках подвергается порезам, надрывам и повреждениям из‑за обычного метаболизма и внешних стрессов. Одними из самых опасных повреждений являются двухцепочечные разрывы, при которых разрываются обе цепи спирали ДНК. Если такие разрывы не восстановить быстро и точно, клетки могут погибнуть или, что хуже, сдвинуться в сторону онкогенных преобразований. В этом исследовании изучают, как точная форма и химия обломанных концов ДНК помогают определить, будет ли ключевой путь репарации — несовмещённое (не гомологичное) сшивание концов (NHEJ) — эффективно сближать эти концы и с минимальным числом ошибок.
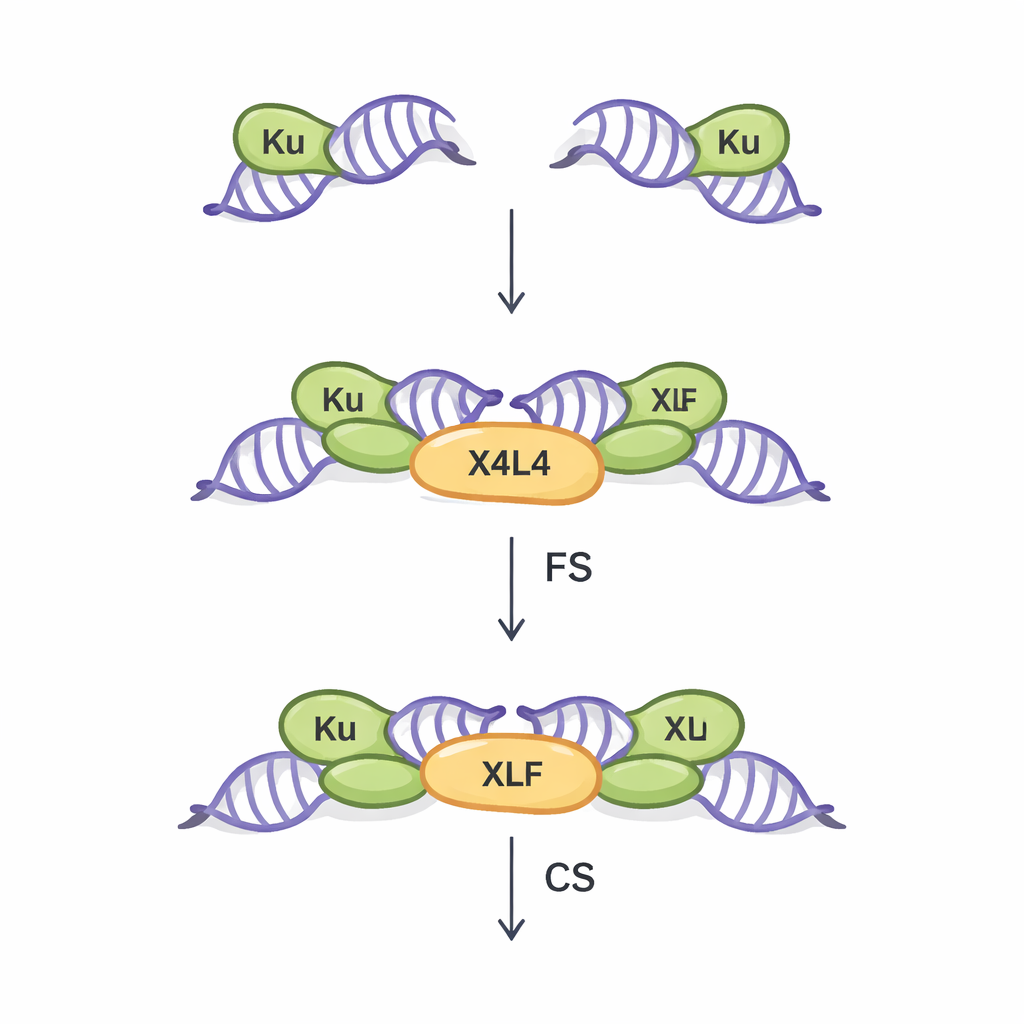
Два способа сближения сломанных концов ДНК
NHEJ — основной путь репарации двухцепочечных разрывов в большинстве клеток организма. Он работает без необходимости в матричной последовательности, поэтому быстр, но отчасти склонен к ошибкам. Первым критическим этапом в этом пути является синапсис: физическое мостирование двух разорванных концов ДНК, чтобы их затем можно было сшить. Ранние работы, в основном на идеализированных прямых (blunt) концах ДНК, выявили два типа синаптических ансамблей. В состоянии «гибкого синапсиса» (FS) концы держатся рядом и могут двигаться, перебирая возможные способы выравнивания. В состоянии «плотного синапсиса» (CS) концы выстраиваются торцом к торцу и готовы к запечатыванию лигирующим ферментом. Известно, что три ключевых белка — Ku, XRCC4–Ligase IV (в совокупности X4L4) и XLF — координируют этот процесс, но то, как реальные, нерегулярные концы ДНК влияют на выбор синаптического состояния, оставалось малопонятным.
Форма концов и короткие совпадения направляют маршрут репарации
Исследователи использовали одномолекулярную ФЭРТ (FRET) — флуоресцентный метод, отслеживающий расстояния на нанометровом масштабе, — чтобы наблюдать отдельные молекулы ДНК в процессе их сближения белками NHEJ. Они сравнивали простые прямые концы с более реалистичными концами, имеющими короткие выступы — одноцепочечные хвостики, которые потенциально могут спариваться друг с другом. Выяснилось, что когда выступы комплементарны, даже всего пара-тройка оснований резко повышает вероятность формирования плотного синаптического комплекса. Фактически три совпадающие базы «микросходства» в месте разрыва были достаточно, чтобы Ku и X4L4 сами по себе создали стабильный CS‑комплекс без участия XLF. Это показывает, что сама ДНК может вносить часть энергии и направляющей, которые обычно обеспечивают вспомогательные белки.
Как крошечные язычки ДНК помогают стабилизировать мост
Анализируя разные ФЭРТ‑сигнатуры, команда выявила по крайней мере две структурные разновидности плотного синаптического состояния для концов с выступами. В одном варианте кончики выступов спариваются между собой, образуя «разрезанное» или с щелью соединение. В другом месте стыки, где двойные цепи переходят в одноцепочечные выступы, прижимаются в линию, в то время как выступы отгибаются наружу как маленькие клапаны. Эти клапаны при этом всё ещё допускают образование пар оснований и удерживают концы в очень близком соседстве, что, вероятно, стабилизирует комплекс и даёт ферментам пространство для обрезки или удлинения ДНК перед окончательным сшиванием. Любопытно, что обычные оксидативные повреждения в выступах, такие как 8‑оксогуанин, лишь умеренно влияют на этот процесс, подчёркивая, насколько NHEJ устойчив к некоторым видам повреждений.
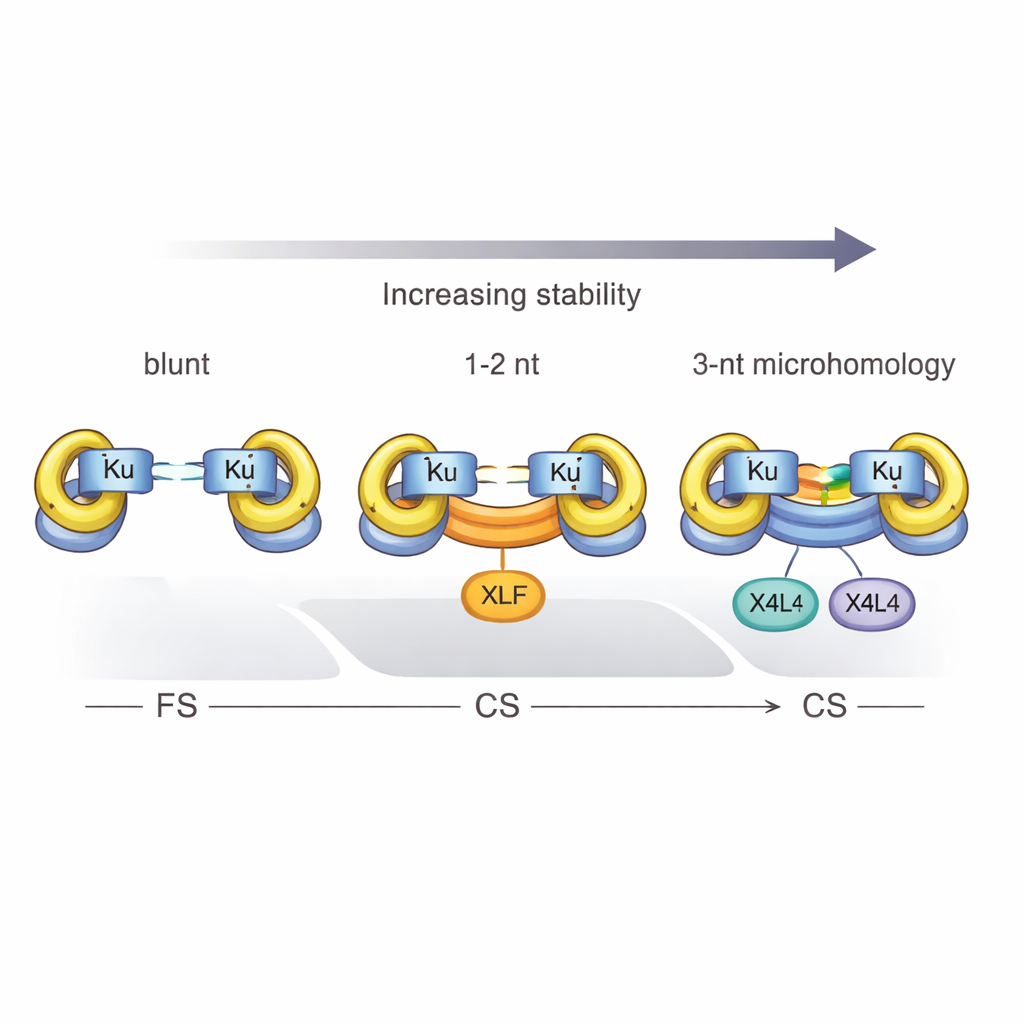
Белки, фосфаты и «сила трёх»
Исследование также определило чёткий порог: по крайней мере три комплементарные пары оснований требуются, чтобы Ku и X4L4 надёжно превратили гибкий комплекс в плотный. При наличии только одной или двух совпадающих пар система в основном застревает в гибком состоянии, если только XLF не подключится, чтобы помочь зажать концы вместе. Химические детали также имеют значение. Когда разорванная ДНК несёт 5′‑фосфатную группу — обычную особенность многих физиологических разрывов — синапсис становится более эффективным, и плотные комплексы с большей вероятностью завершаются лигированием, превращая временный мост в постоянный ремонт. Однако этот «фосфатный» эффект не может полностью заменить стабилизирующее действие спаривания оснований в месте разрыва.
Почему это важно для здоровья и редактирования генома
Проще говоря, эта работа демонстрирует, что сломанные концы ДНК не являются пассивными жертвами, ожидающими починки. Их точные формы, крошечные участки совпадающей последовательности и химические метки активно направляют то, как белки‑репараторы хватают, выравнивают и воссоединяют их. Когда присутствуют три или более совпадающих основания, сами концы ДНК помогают зафиксировать разрыв в состоянии, готовом к ремонту, делая порой некоторых вспомогательных белков необязательными. Когда таких совпадений мало, становятся необходимы дополнительные белковые факторы. Эти наблюдения объясняют, почему одни разрывы восстанавливаются аккуратно, тогда как другие приводят к мелким мутациям или перестройкам. Они также дают подсказки для улучшения инструментов редактирования генома, таких как CRISPR: поскольку специально создаваемые разрывы восстанавливаются той же NHEJ‑машинерией, тонкая настройка концов разрывов может помочь лучше контролировать, как именно будет перестроен геном.
Цитирование: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Ключевые слова: репарация двухцепочечных разрывов ДНК, несовместное (не гомологичное) сшивание концов, синапсис ДНК, микросходство, стабильность генома