Clear Sky Science · ru
Переключение одной валина на лейцин нарушает связывание ДНК Plasmodium falciparum AP2-G и раскрывает роль GDV1 в активации ap2-g
Как паразиты малярии принимают критическое решение между жизнью и смертью
Паразиты малярии, находящиеся в нашей крови, постоянно сталкиваются с судьбоносным выбором: продолжать размножаться внутри одного хозяина или превратиться в форму, способную перескочить к следующему хозяину через укус комара. В этом исследовании показано, как одно крошечное изменение в одном белке паразита может полностью отключить стадию, готовую к передаче через комара, что открывает новые подходы для блокирования передачи малярии.
Развилка на пути паразита
В кровотоке Plasmodium falciparum в основном фокусируется на быстром росте, что вызывает заболевание. Но небольшая часть преобразуется в половые формы — гаметоциты, единственные стадии, которые комары могут подобрать и передать дальше. Почему только некоторые паразиты в популяции делают этот переход, долгое время оставалось загадкой. Ранее было показано, что два белка паразита, GDV1 и ДНК-связывающий белок AP2-G, находятся в центре этого решения. GDV1 помогает пробудить обычно молчащий ген ap2-g, а AP2-G, в свою очередь, включает набор генов, приводящих к половому развитию. Текущее исследование задумывалось как изучение другого белка — киназы STK2, но вместо этого обнаружило гораздо более драматичный результат, связанный с самим AP2-G.
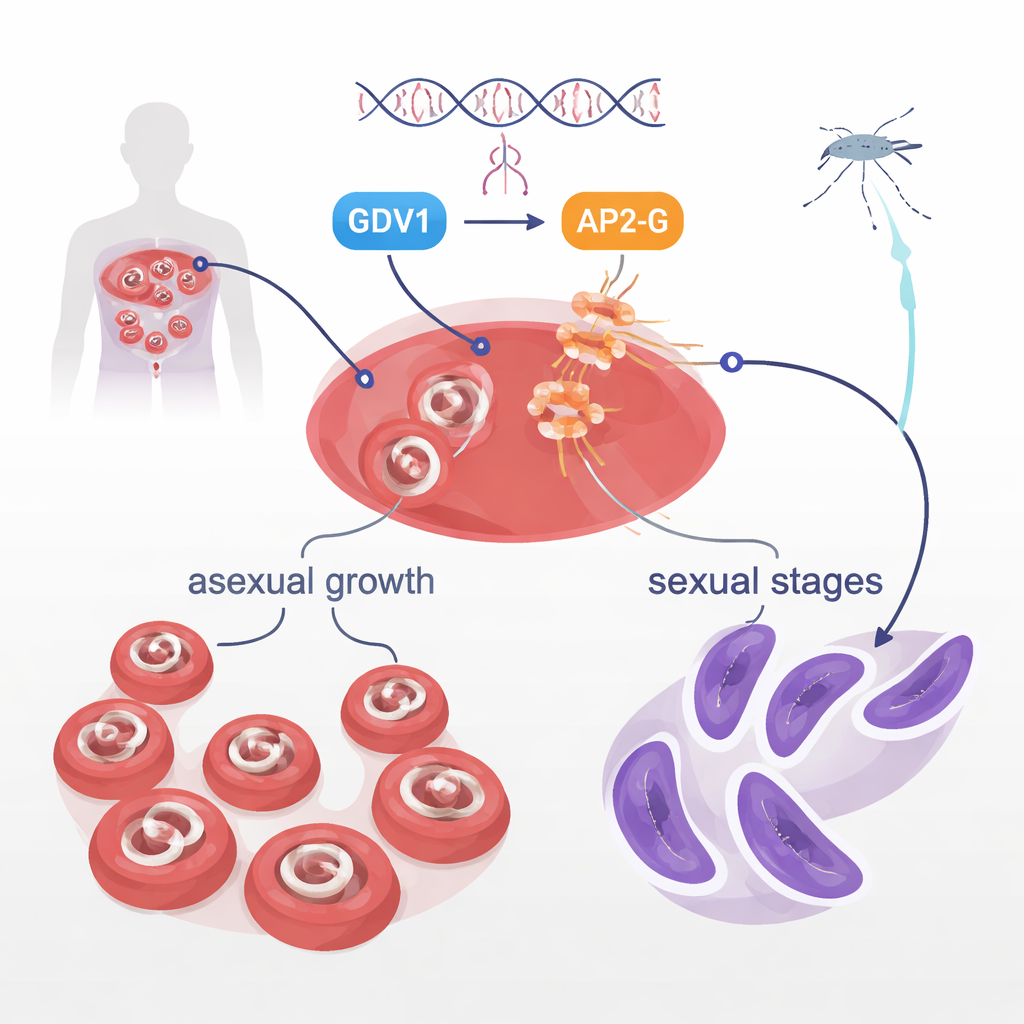
Одна аминокислота, которая останавливает передачу
При удалении гена stk2 в одном лабораторном штамме исследователи заметили, что эти паразиты полностью утратили способность образовывать гаметоциты, при этом их бесполое размножение оставалось нормальным. Удивительно, но при аналогичных манипуляциях в другом штамме гаметоциты формировались как обычно. Полное секвенирование генома выявило скрытого виновника: одна «буква» в гене ap2-g, меняющая одну аминокислоту — валин — на очень похожую лейцин в позиции 2163. Эта позиция находится в самом начале ДНК‑связывающего участка AP2-G, той части, которая физически захватывает специфические ДНК‑мотивы для включения генов. Этот крошечный обмен валина на лейцин сам по себе оказался достаточным, чтобы отменить образование гаметоцитов. Когда учёные встроили эту мутацию в обычно нормальных паразитов, гаметоциты исчезали; при обратном восстановлении валина половое развитие полностью восстанавливалось.
Как переключатель ломает молекулярный замок
Чтобы понять, почему это тонкое изменение настолько разрушительно, команда совместила компьютерное моделирование с лабораторными экспериментами. Прогнозы структуры показали, что замена валина на лейцин смещает и дестабилизирует точную форму ДНК‑связывающего домена AP2. В тест‑трубных анализах с очищенными белками нормальный AP2-G прочно связывался со своей предпочтительной ДНК‑последовательностью, коротким кодом, содержащим мотив «GnGTAC». Напротив, мутантный AP2-G с лейцином в позиции 2163 совершенно не связывался с этой последовательностью. Без стабильного связывания с ДНК AP2-G не мог самостоятеьно включать свой собственный ген (положительная петля обратной связи, известная как авторегуляция) и активировать десятки нижестоящих генов, необходимых для перевода паразитов в половой путь. Функционально мутантные паразиты становились «стерильными»: они не могли образовывать формы, инфицирующие комаров, хотя и продолжали процветать в эритроцитах.
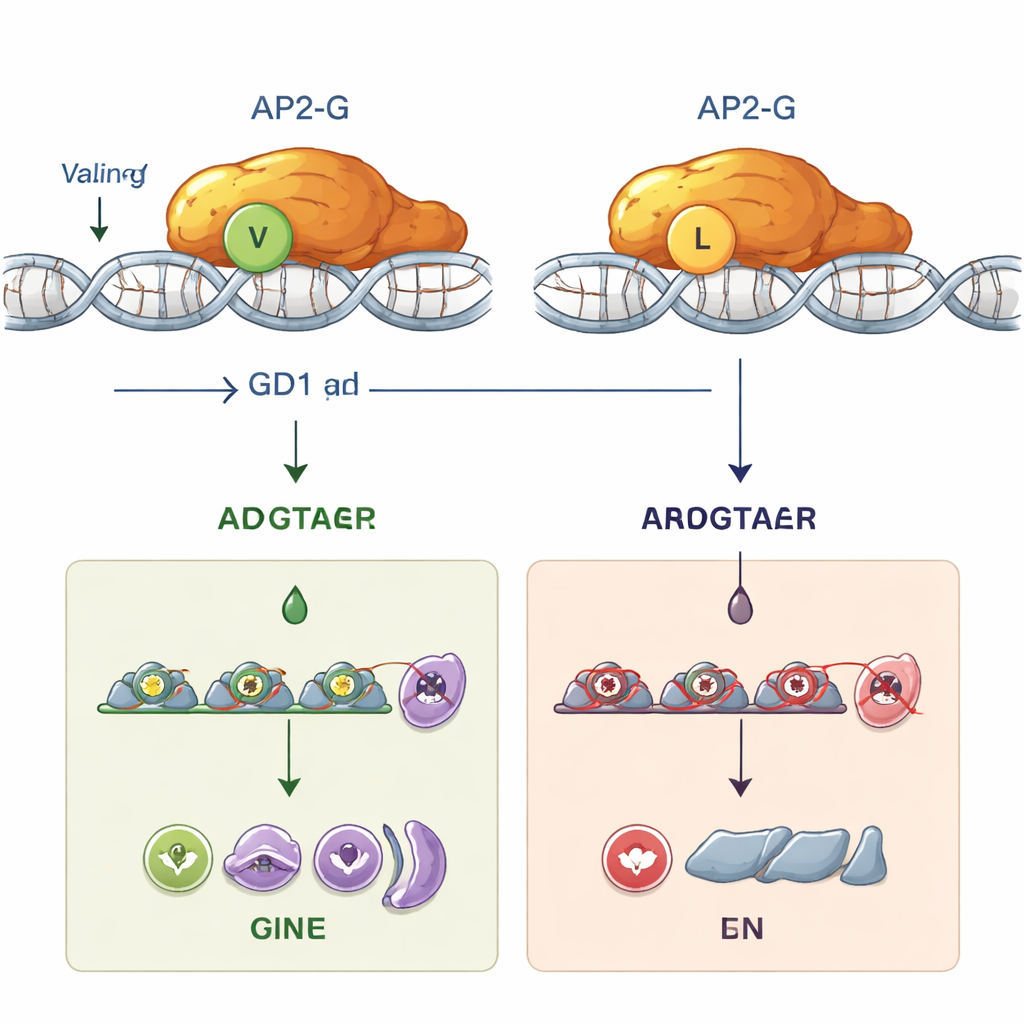
Скрытая роль GDV1 до того, как AP2-G берет на себя управление
Мутация также дала исследователям уникальный инструмент: паразитов, у которых ген ap2-g можно включить, но AP2-G не может связываться с ДНК. С помощью светящихся репортеров они отслеживали, когда разные участники действуют в течение 48‑часового цикла паразита в эритроцитах. Они обнаружили, что белок GDV1 появляется первым, рано на стадии шизогонии, и необходим для того, чтобы запустить экспрессию ап2-g из его заглушенного состояния. Это раннее включение происходило как в случае нормального AP2-G, так и мутантной версии. Только позже, когда накапливался достаточный уровень нормального AP2-G, наступала сильная самоподдерживающая петля и активация других «половых» генов. Ключевой маркер, белок MSRP1, загорается только в паразитов с функциональным AP2-G, что даёт удобный способ отличить ранние и поздние клетки, предрасположенные к половому развитию. В мутантных линиях с заменой на лейцин GDV1 всё ещё мог пробудить ap2-g, но сломанный AP2-G не мог продвинуть процесс дальше, и половое развитие останавливалось.
Последствия для остановки распространения малярии
Для широкого читателя главный вывод прост: паразиты малярии опираются на чрезвычайно чувствительный молекулярный замок, чтобы решать, станут ли они передаваемыми. Исследование показывает, что изменение всего одного «зубца» в этом замке — одного валина в ДНК‑захватывающем участке AP2-G — препятствует образованию форм, инфекционных для комаров. При этом оно уточняет, что другой белок, GDV1, действует раньше как ключ, чтобы сначала разблокировать молчащий ген ap2-g, прежде чем AP2-G усилит собственную продукцию и запустит более широкий половой программ. Нанесение карт этого ряда событий и создание репортерных линий паразитов, которые светятся на каждом этапе, обеспечивают мощные инструменты для скрининга лекарств или факторов хозяина, мешающих половой приверженности. В долгосрочной перспективе нацеливание на ДНК‑связывающий участок AP2-G или на шаг активации, управляемый GDV1, может лечь в основу новых стратегий, которые не просто лечат малярию у одного пациента, но и разрывают цепочку передачи полностью.
Цитирование: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Ключевые слова: передача малярии, Plasmodium falciparum, развитие гаметоцитов, AP2-G, GDV1