Clear Sky Science · ru
Иерархические механизмы контролируют удаление ДНК-повреждением остановленной РНК-полимеразы II
Когда машины копирования генов натыкаются на препятствие
Каждую секунду миллионы крошечных молекулярных машин, называемых РНК-полимеразой II, движутся по нашей ДНК, переписывая гены в РНК. Но когда ДНК повреждена — например ультрафиолетовым (УФ) светом солнца — эти машины могут застрять. Если застрявших комплексов накопится много, клетки теряют способность корректно считывать гены, что особенно опасно для нервных клеток и может приводить к редким заболеваниям, таким как синдром Кокейна. В этом исследовании подробно раскрывают, как клетки распознают заблокированные полимеразы и либо перезапускают, либо удаляют их, прежде чем они нанесут длительный вред.
Новый способ наблюдать «пробки» на клеточных дорогах
Чтобы понять, как клетки очищают заблокированные полимеразы, исследователи создали временно разрешающую «камеру наблюдения» за транскрипцией. Они применили препарат, позволяющий существующим молекулам РНК-полимеразы II продолжать движение, но препятствующий началу работы новым молекулам, и затем вызвали небольшой участок УФ-повреждения внутри каждого ядра клетки. Отслеживая специфическую химическую метку на активной форме полимеразы, они могли наблюдать, как быстро она исчезает из повреждённой зоны по сравнению с остальной частью генома. Параллельно был разработан вспомогательный тест, фиксирующий общий объём активной полимеразы в клеточных экстрактах, что показало не только когда полимеразы покидают ДНК, но и когда клеточная система утилизации разлагает их.
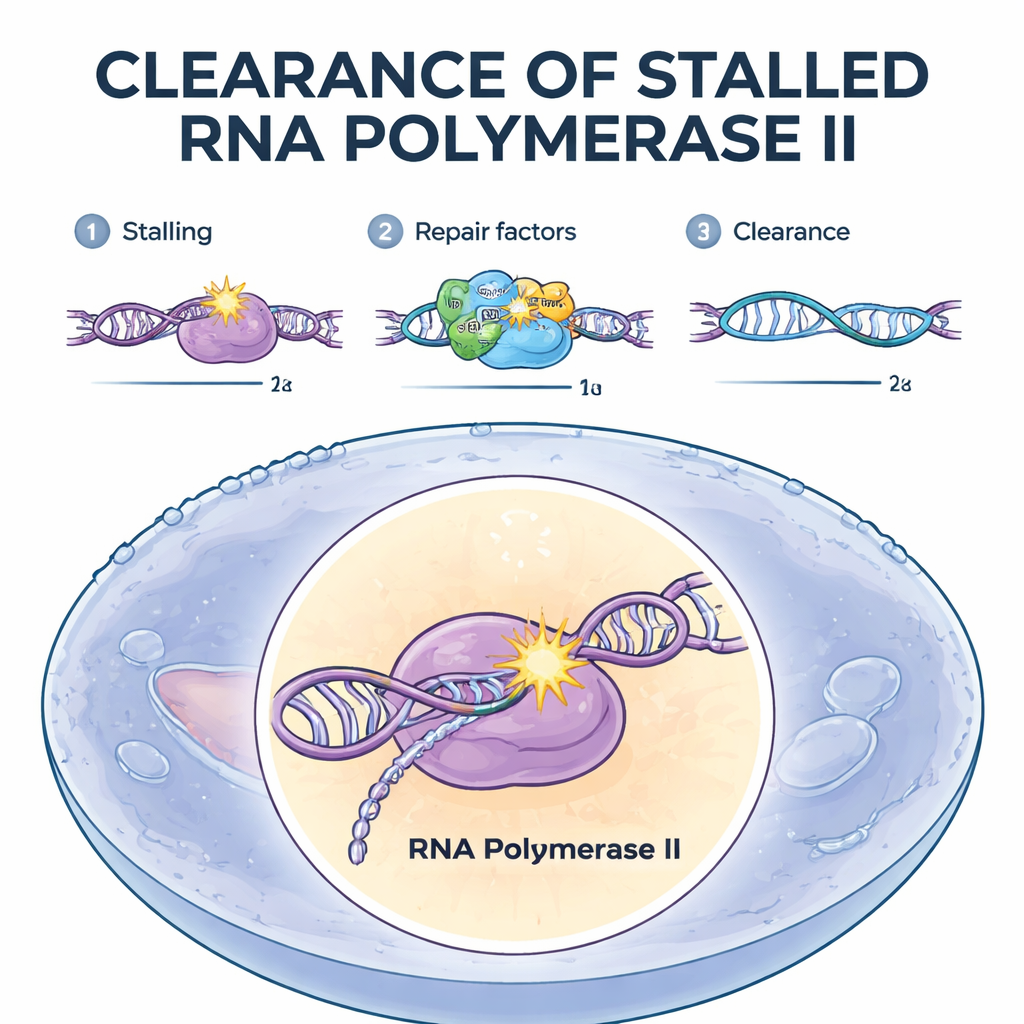
Маркёры для удаления застрявших машин
Авторы сосредоточились на репарации, связанной с транскрипцией, — специализированной системе, которая исправляет повреждения на активно читаемых генах. Они использовали набор штаммов человеческих клеток, каждый из которых лишён различного фактора репарации. Две белковые компоненты, CSB и CSA, оказались решающими вратами. При отсутствии любого из них РНК-полимераза II накапливалась и упорно оставалась в местах повреждений, а клетка не могла её деградировать. Биохимически такие клетки также не прикрепляли малые убиквитиновые метки к ключевому участку полимеразы. Напротив, клетки, лишённые более поздних белков репарации — тех, что вырезают и заменяют повреждённую ДНК — всё равно нормально очищали полимеразу. Это показало, что начальная убиквитинизация застрявшей полимеразы является критическим триггером, определяющим её судьбу.
Две бригады уборки: одна быстрая, другая — запасная
После маркировки полимеразы клетка может выбрать один из двух путей её удаления. Основной, быстрый путь опирается на большой ремонтный комплекс TFIIH и в частности на его геликазную субъединицу XPD, которая использует энергию для разворачивания ДНК. Вспомогательные белки, включая ELOF1, UVSSA и STK19, привлекают TFIIH к застрявшей полимеразе и располагают XPD на ДНК непосредственно перед ней. С помощью новых тестов на клетках пациентов с мутацией, приводящей к утрате геликазной активности XPD, авторы показали, что когда XPD не может раскручивать ДНК, очистка полимеразы существенно замедляется, даже при наличии прочего ремонтного аппарата. Это указывает на то, что механическое «вытягивание» или «сотрясение» полимеразы со стороны XPD обычно освобождает её от места повреждения, давая доступ ремонтным ферментам.
Медленный, но важный запасной план
Исследование также выявило более медленный аварийный путь удаления застрявшей полимеразы. Этот маршрут зависит от белка VCP (также известного как p97), который распознаёт убиквитиновые метки и способен принудительно извлекать белки из хроматина. В здоровых клетках с полнофункциональным TFIIH блокада VCP оказывала лишь незначительное влияние. Но в клетках, где TFIIH отсутствовал, был неверно ориентирован или лишён геликазной активности, очистка полимеразы становилась практически полностью зависимой от VCP. В таких условиях VCP всё ещё мог выдергивать помеченную полимеразу с ДНК, даже когда нормальная репарация была невозможна. Важно, что этот запасной путь также требовал некоторой убиквитинизации, что объясняет, почему клетки без CSB или CSA — и, следовательно, без убиквитиновых меток — терпят неудачу и в основном, и в резервном механизме.
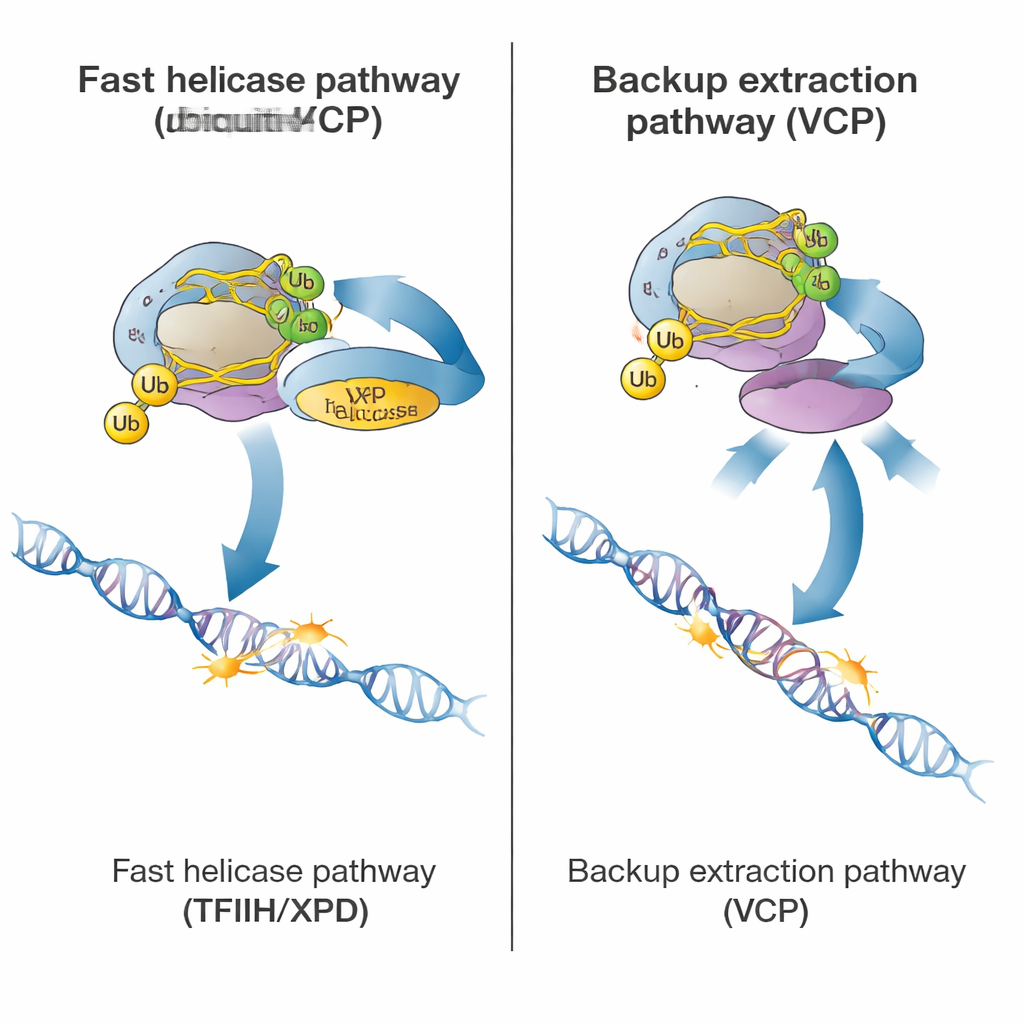
Почему это важно для здоровья и болезни
В совокупности работа описывает иерархическую систему безопасности, которую клетки запускают, когда РНК-полимераза II сталкивается с повреждением ДНК. Сначала CSB и CSA помечают застрявшую машину убиквитином. Если всё работает правильно, TFIIH и его геликаза XPD быстро сдвигают полимеразу, чтобы участок повреждения можно было вырезать и восстановить. Если TFIIH не справляется, VCP вступает в дело, извлекая полимеразу и направляя её на деградацию, предотвращая «засорение» экспрессии генов, хотя само повреждение ДНК остаётся. Эта схема помогает объяснить, почему наследственные дефекты в CSB или CSA приводят к особенно тяжёлым неврологическим проблемам: без убиквитиновой маркировки клетки теряют и основной путь, и резервный механизм извлечения, оставляя застрявшие полимеразы на повреждённых генах и вызывая хроническую блокаду транскрипции.
Цитирование: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Ключевые слова: репарация ДНК, связанная с транскрипцией, РНК-полимераза II, ультрафиолетовое повреждение ДНК, убиквитинирование белков, синдром Кокейна