Clear Sky Science · ru
Визуализация фенотипической неоднородности и морфологии отдельных клеток Clostridioides difficile in situ во время инфекции кишечника
Почему кишечные микробы ведут себя по‑разному
Clostridioides difficile, часто называемая C. diff, — печально известный внутрибольничный патоген, который может вызывать тяжёлую, иногда угрожающую жизни диарею после того, как антибиотики нарушают нормальную микрофлору кишечника. Однако даже при генетической идентичности и одинаковой среде отдельные клетки могут вести себя очень по‑разному. В этом исследовании с беспрецедентной детализацией показано, как отдельные клетки C. diff включают или выключают производство токсинов и даже меняют форму во время инфекции в кишечнике мыши, что даёт подсказки о том, почему болезнь может быть настолько упорной и трудно поддающейся лечению.
Отслеживание опасного захватчика кишечника в реальном времени
Чтобы понять поведение отдельных клеток C. diff в организме, исследователям потребовалось средство, позволяющее чётко видеть их среди плотного и разнообразного сообщества микробов кишечника. Они создали штаммы C. diff, которые постоянно светятся яркими цветами под микроскопом, используя специальные флуоресцентные белки, не мешающие росту бактерий или их патогенности. Инфицируя мышей, обработанных антибиотиками, этими светящимися штаммами и затем режа и окрашивая ободочную кишку, учёные могли точно определить местоположение и поведение тысяч отдельных бактериальных клеток в сохранённой ткани кишечника. 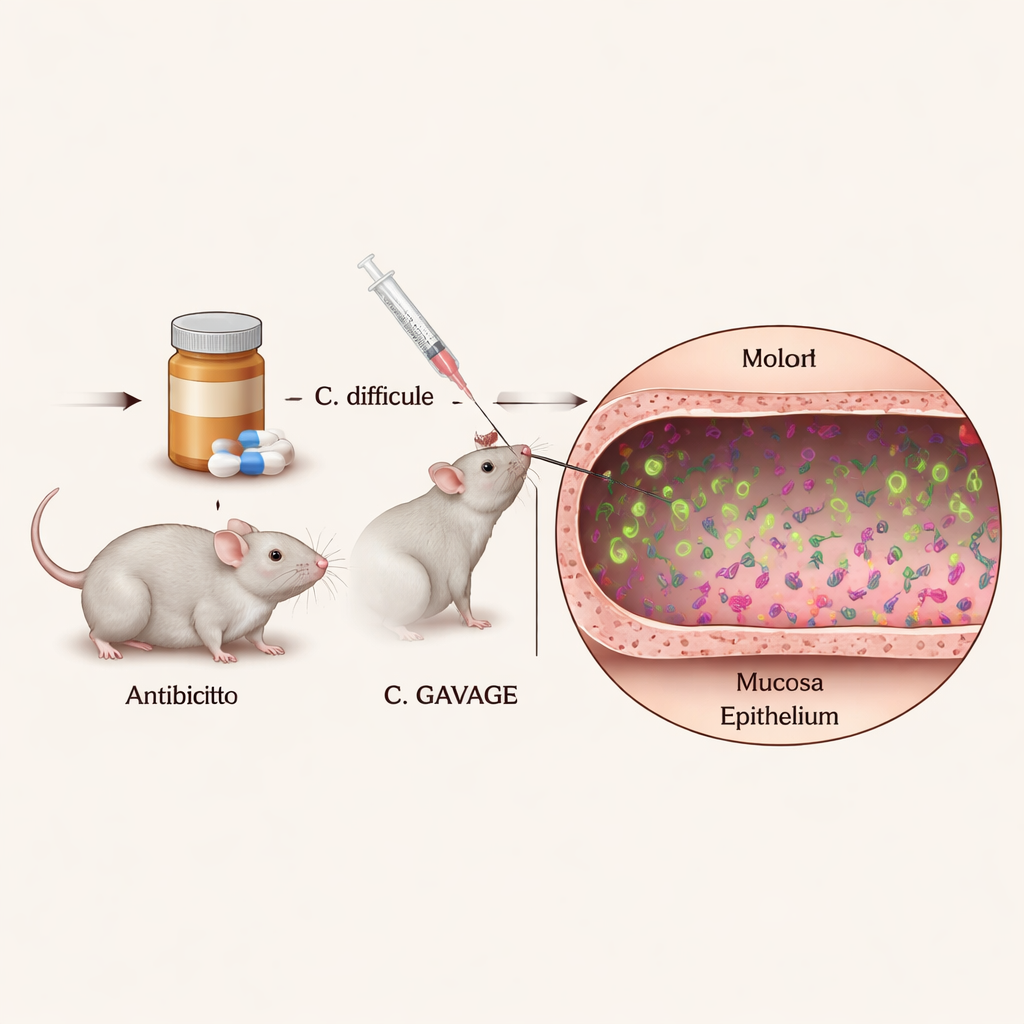
Где бактерии живут в ободочной кишке
Снимки показали, что большинство клеток C. diff обитает в центре содержимого кишки, называемом просветом (lumen), подтверждая, что этот организм в основном является свободно‑плавающим «люминальным» патогеном. Тем не менее заметное меньшинство клеток последовательно обнаруживалось рядом со слизистым слоем и непосредственно у эпителиальной поверхности — тонкого слоя клеток, выстилающего кишку и выполняющего барьерную функцию. Эта популяция в тесном контакте ранее не была явно видна у обычных мышей с нормальным иммунитетом. Важно, что внесённые флуоресцентные метки не ослабляли заметно бактерии в животных, что означает: полученные изображения, вероятно, отражают поведение C. diff в реалистичной инфекции.
Кто производит токсин и где?
Затем команда добавила второй флуоресцентный маркер, который включается только тогда, когда C. diff активирует гены токсинов. Токсины — это повреждающие белки, которые ранят слизистую кишечника и вызывают симптомы болезни; их также определяют в анализах кала при диагностике инфекции. Удивительно, но бактерии не производили токсины одновременно все вместе. Вместо этого только часть клеток в любой момент светилась как «токсин‑ON», как на ранних, так и на поздних стадиях инфекции. Доля таких клеток была выше в мутантном штамме, генетически настроенном на сверхпродукцию токсина, но и там не каждая клетка включалась. Не менее поразительно, положение клетки — плавающая в просвете, находящаяся в слизи или соприкасающаяся с эпителием — не сильно влияло ни на частоту включения синтеза токсина, ни на силу активации этих генов. 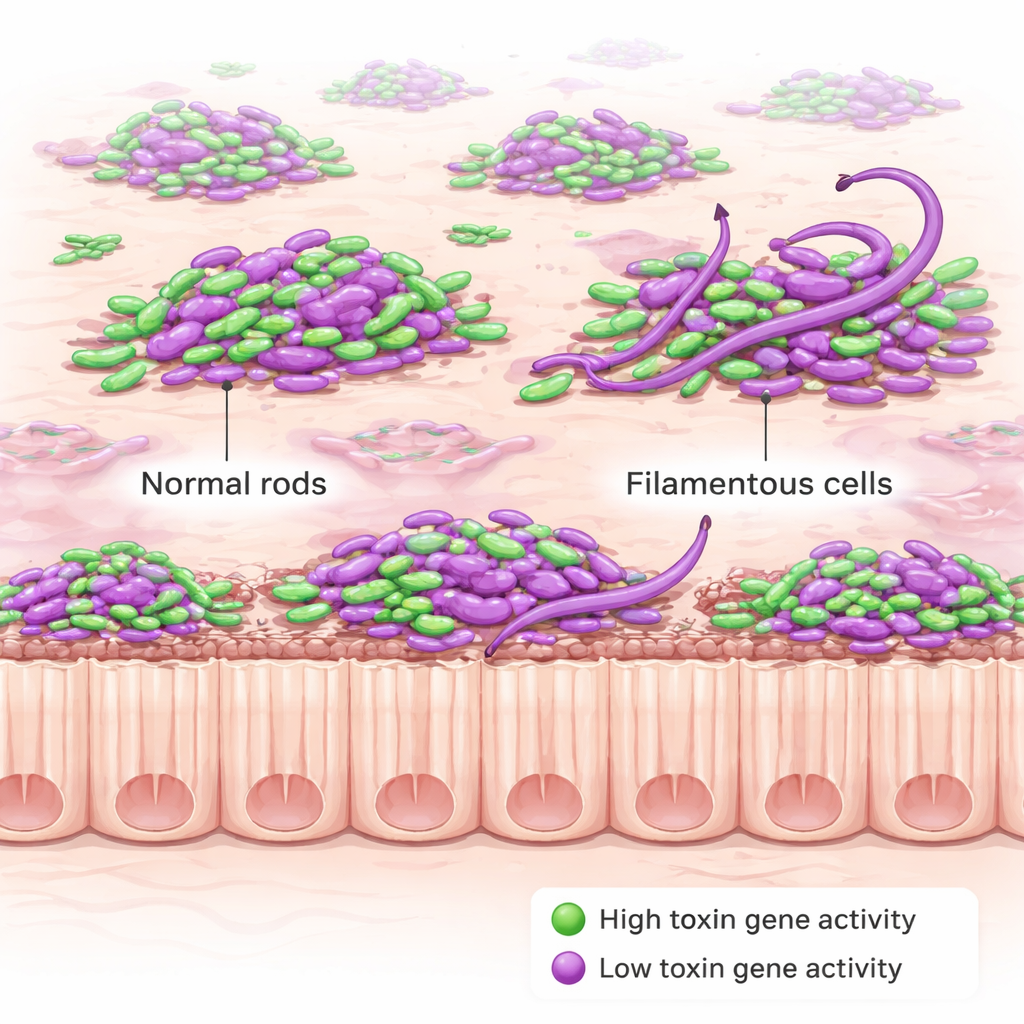
Изменяющие форму клетки под стрессом
Пока учёные картировали производство токсина, они наткнулись на неожиданное поведение. У мышей, инфицированных мутантом с повышенной продукцией токсина, многие клетки C. diff в острой фазе болезни становились необычно длинными, изогнутыми нитями, некоторые более чем в десять раз длиннее нормальных коротких палочек. Эта «нитевидная» морфология проявлялась преимущественно во время ранней, тяжёлой инфекции и затем исчезала; она не наблюдалась, когда тот же штамм выращивали в лабораторной среде. Это указывает на то, что стрессовые условия в воспалённом кишечнике — а не только генетические изменения — запускают эту драматическую перестройку. Последующие эксперименты показали, что утрата регуляторного белка RstA, который контролирует как гены токсинов, так и другие стресс‑ответы, способствует образованию таких филаментов.
Что это значит для болезни, вызываемой C. diff
Ключевая мысль для неспециалистов: даже один штамм C. diff ведёт себя как разделённая рабочая группа. Некоторые клетки несут энергетические затраты на производство токсина и повреждение кишки, высвобождая питательные вещества, которыми могут пользоваться их «бес‑токсинные» соседи. Такое общее «разделение труда» может способствовать тому, что инфекция сохраняется и возвращается, потому что не все клетки одинаково уязвимы для лечения, нацеленному на токсины или быстро растущие бактерии. Новая система светящихся репортеров даёт учёным мощный инструмент, чтобы наблюдать по одной клетке, как C. diff и родственные кишечные микробы приспосабливаются во времени и пространстве внутри организма. Эти знания в конечном счёте могут помочь разработать терапии, направленные не только на уничтожение бактерий, но и на разрушение вредных ролей отдельных субпопуляций, которые приводят к болезни и рецидивам.
Цитирование: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Ключевые слова: Clostridioides difficile, кишечный микробиом, бактериальные токсины, фенотипическая неоднородность, флуоресцентная визуализация