Clear Sky Science · ru
Механическое омоложение сенесцентных стволовых клеток и старой кости через ремоделирование хроматина
Почему важно сохранять кости молодыми
С возрастом наши кости постепенно теряют прочность, становясь тоньше и хрупче. Это повышает риск переломов, утраты самостоятельности и хронической боли. Большинство современных методов лечения направлены на замедление разрушения кости или восполнение минералов, но они не восстанавливают старение самих стволовых клеток, которые строят кость. В этом исследовании рассматривается другой подход: использование тщательно дозируемых физических сил — вместо лекарств — чтобы «омолодить» стареющие остеогенные стволовые клетки и улучшить здоровье костей и общую физическую форму у пожилых мышей.
Когда строители кости стареют
Глубоко внутри наших костей находятся мезенхимальные стволовые клетки костного мозга — главные строители, которые могут превращаться в клетки, формирующие кость. С возрастом эти клетки реже делятся, хуже формируют кость и демонстрируют классические признаки клеточного старения, такие как повреждения ДНК и провоспалительные сигналы. Исследователи сравнили клетки от молодых и пожилых доноров человека и обнаружили, что старые стволовые клетки отличаются не только биохимически — они механически слабее. Они генерировали меньше внутренних тянущих усилий, имели более «вялый» внутренний каркас и хуже передавали механические сигналы в ядро клетки. В костной ткани старых мышей наблюдалось похожее снижение: губчатая сеть кости истончилась, ключевые белки механической передачи были уменьшены, а маркеры старения повышены.
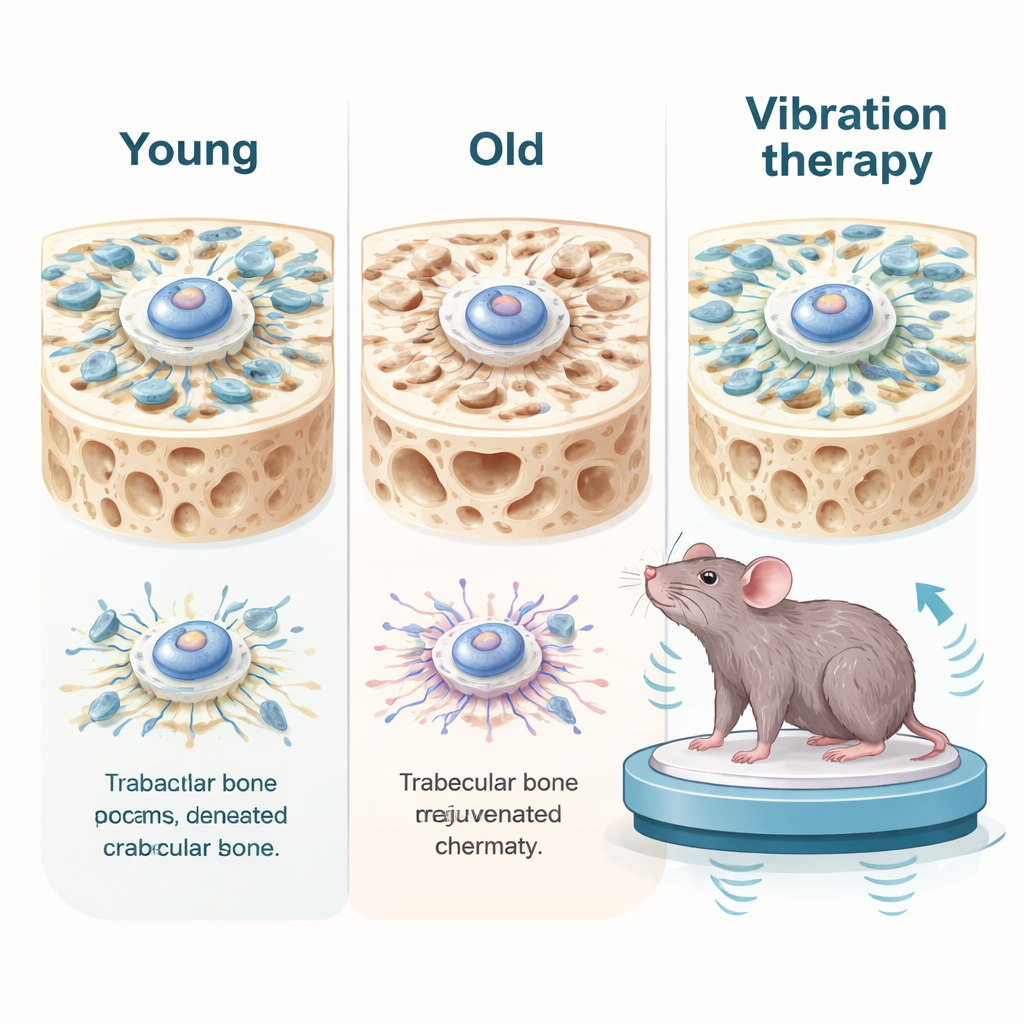
Нежно подтянуть клетки к молодости
Команда затем задала вопрос, может ли восстановление механической силы обратить эти признаки старения. В культурах клеток они применяли мягкое растяжение к сенесцентным стволовым клеткам или использовали препарат, повышающий активность молекулярных моторов. Эти воздействия усиливали тянущие силы в клетках и улучшали организацию внутреннего каркаса. Удивительно, но старые клетки начали выглядеть и вести себя моложе: снизились маркеры сенесценции, уменьшились повреждения ДНК, и клетки начали активнее размножаться. Обратный эффект тоже подтвердился — когда они размягчали окружение под молодыми клетками или химически ослабляли их сократительный аппарат, клетки переходили в подобное старению состояние, замедлялись и включали маркеры старения даже в трехмерном геле, имитирующем кость.
Как сила «разговаривает» с генами
Чтобы понять, как физические силы могут глубоко менять поведение клеток, исследователи обратились к хроматину — упакованной форме ДНК внутри ядра. В старых стволовых клетках хроматин был более конденсирован и менее доступен, что затрудняло включение полезных генов. Восстановление механической силы вызывало локальное расслабление хроматина и увеличение химических меток, связанных с открытой, активной ДНК. При геномном анализе доступности хроматина команда обнаружила, что мягкая механическая стимуляция открывает участки рядом с генами, участвующими в контроле старения. Один ген, называемый FOXO1, выделялся своей чувствительностью к силе. При увеличении механического воздействия регион ДНК вокруг FOXO1 становился более открытым, его активность росла, а клетки утоляли признаки сенесценции. Блокировка FOXO1 стирала преимущества механической стимуляции, показывая его как ключевой переключатель, связывающий физическую нагрузку с генетическими программами устойчивости и восстановления.
Поиск оптимальной дозы механической терапии
Затем исследователи проверили механическую стимуляцию на живых мышах. Пожилые животные помещались на платформу с низкоинтенсивной вибрацией на короткие ежедневные сеансы в течение месяца, тогда как другие подвергались разгрузке задних лап путем подвешивания за хвост, имитируя крайнюю неактивность. У старых мышей мягкая вибрация усиливала механические сигналы в кости, снижала маркеры старения и воспаления и частично восстанавливала губчатую сеть кости. Это также улучшило силу хвата, выносливость при нагрузке, выполнение задач, связанных с памятью, и снизило воспаление в крови, печени и почках. Однако при непрерывном применении вибрации без дней отдыха преимущества исчезали и даже обращались в обратный эффект: структура кости ухудшалась, повреждения ДНК увеличивались, а воспаление росло. В клеточных экспериментах чрезмерно сильное или частое растяжение вызывало разрывы ДНК и возвращало клетки к сенесценции, показывая, что механическая сила может исцелять или вредить в зависимости от дозы.
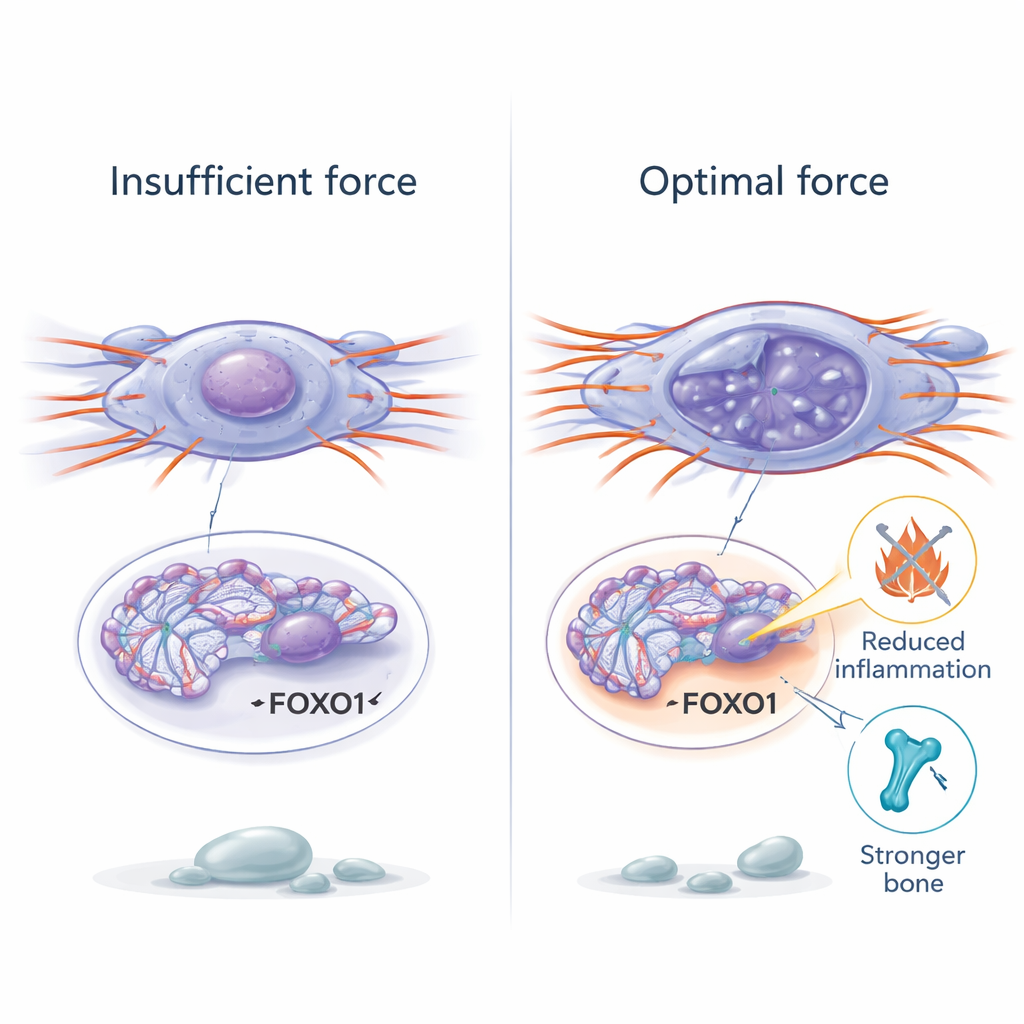
От имитации упражнений к будущим методам лечения
Для непрофессионала главный вывод в том, что наши клетки реагируют не только на гормоны и химические сигналы — они также внимательно «слушают» физические силы. В этой работе авторы показывают, что умеренная, хорошо продуманная механическая стимуляция может пробудить стареющие стволовые клетки кости, открыть защитные генетические программы, такие как FOXO1, восстановить ослабленную кость и успокоить хроническое воспаление у старых мышей. Одновременно слишком малая или слишком большая сила ускоряет износ клеток. Эти результаты намекают, что тщательно разработанные механические терапии — возможно, специфические режимы упражнений или безопасные устройства на основе вибрации — однажды могут дополнять лекарства в поддержании здоровья костей и, возможно, других тканей дольше.
Цитирование: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Ключевые слова: старение кости, механическая стимуляция, омоложение стволовых клеток, ремоделирование хроматина, FOXO1