Clear Sky Science · ru
Точная вырезка расширенных повторов GGC в NOTCH2NLC с помощью CRISPR/Cas9 для лечения нейронной интраядерной включенной болезни
Редактирование ДНК в борьбе с таинственным заболеванием мозга
Нейронная интраядерная включенная болезнь (NIID) — редкое, но разрушительное заболевание мозга, которое может вызывать деменцию, нарушения движений и даже преждевременную смерть. В настоящее время лекарства нет. В этой работе изучается, можно ли с помощью мощного инструмента генной редакции CRISPR вырезать крошечный, но токсичный участок ДНК, который вызывает NIID, что показывает, как в будущем лечение может переписывать наши гены для борьбы с болезнями мозга. 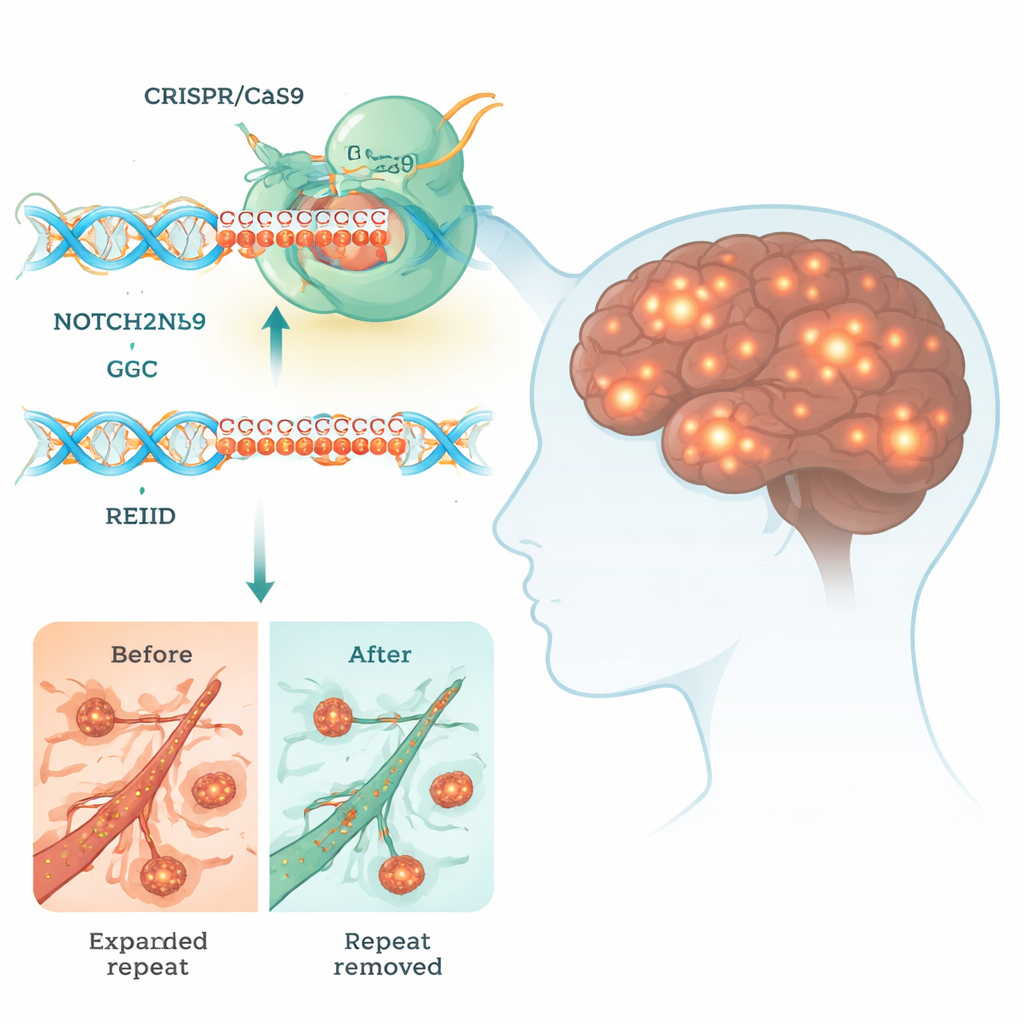
Скрытый генетический виновник
Многие наследственные заболевания мозга вызваны короткими сегментами ДНК, которые разрослись далеко за пределы нормальной длины. При NIID проблемой является чрезмерно удлинённый участок из трехбуквенных ДНК‑звеньев «GGC» в гене NOTCH2NLC. Хотя этот фрагмент находится в области, которая напрямую не кодирует классический белок, клеточные механизмы всё же могут считывать его и производить аномальные полиглициновые (polyG) цепочки. Эти липкие цепочки скапливаются в виде включений внутри ядра нейронов и других тканей, нарушая важные процессы, такие как производство энергии, процессинг РНК и транспорт молекул между ядром и цитоплазмой.
Сложность точной «генной хирургии»
Разработать терапию на основе генной редакции для NIID особенно трудно, потому что у NOTCH2NLC есть несколько почти идентичных «сестринских» генов, важных для развития человеческого мозга. Если CRISPR поразит не тот ген, это может причинить больше вреда, чем пользы. Исследователи тщательно просканировали ДНК вокруг повтора GGC и нашли мелкие различия в последовательности, которые отличают NOTCH2NLC от его родственных генов. Затем они разработали пары направляющих РНК CRISPR, которые направляют «молекулярные ножницы» Cas9 так, чтобы разрезать сразу перед и сразу после расширенного повтора. Эта стратегия двойного разреза позволяет системе репарации клетки удалить токсический сегмент, сохраняя при этом остальные члены семейства генов нетронутыми.
От клеток в чашке Петри до нейронов, полученных от пациента
Команда сначала испытала свою конструкцию CRISPR в стандартных человеческих клетках и в клетках, сконструированных так, чтобы нести большой повтор NOTCH2NLC. В этих моделях редактор эффективно вырезал повтор, и уровни агрегатов polyG снизились примерно вдвое или более. Затем исследователи перешли к индуцированным плюрипотентным стволовым клеткам (iPSCs), полученным от пациента с NIID, и превратили эти клетки в нейральные прогениторы — раннюю стадию клеток мозга. С помощью CRISPR они либо удаляли расширенный повтор, либо заменяли его вариантом нормальной длины. Детальный анализ ДНК и секвенирование всего генома показали, что редактирование было высокоточным, с незначительными признаками нежелательных разрезов, а отредактированные клетки по‑прежнему делились и созревали нормально. 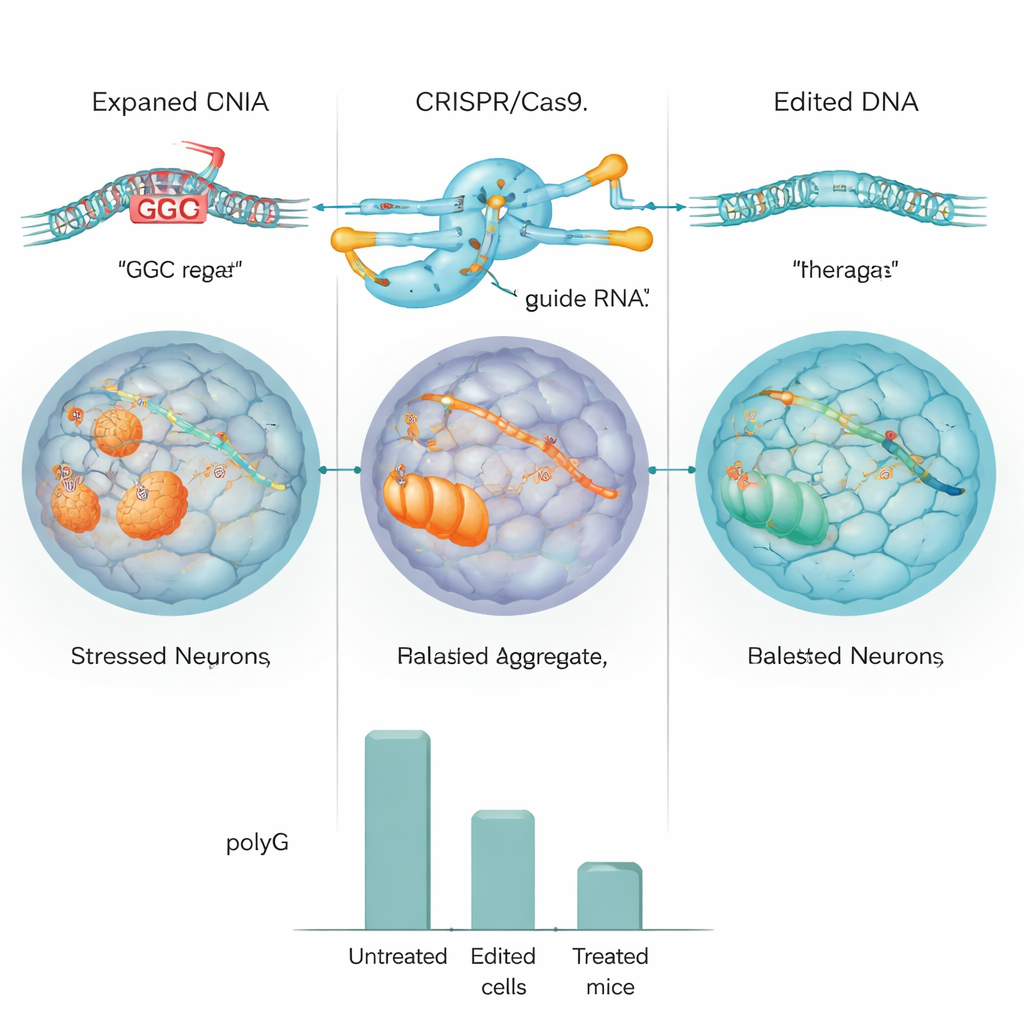
Восстановление работы мозга и тела на мышиной модели
Чтобы проверить, может ли этот подход действительно улучшить состояние при болезни, исследователи использовали мышей, модифицированных так, чтобы нести человеческий повтор NOTCH2NLC и развивать признаки, похожие на NIID, включая ядерные включения, нарушения движений и сокращённую продолжительность жизни. Они упаковали систему CRISPR в модифицированный вирус, который может распространяться по мозгу после простой инъекции в кровоток новорождённым мышам. У животных, получивших лечение, расширенный повтор был успешно удалён в тканях мозга. В результате уровни токсичного polyG резко снизились, маркеры здоровья нейронов улучшились, и уменьшилась аномальная активация поддерживающих клеток мозга. Тесты поведения показали, что лечёные мыши больше двигались, лучше держали равновесие и жили дольше, чем нелечёные потомки из того же помёта. Похожие преимущества наблюдались и в сердце, где в этой модели также накапливается polyG.
Что это может означать для будущих терапий
Для неспециалиста главный вывод таков: NIID, по-видимому, во многом обусловлена одним конкретным чрезмерно удлинённым повтором ДНК, и точное удаление этого повтора может обратить многие признаки болезни в клетках и у мышей. Эта работа ещё не превращается в готовую терапию для людей: исследователям предстоит уточнить долгосрочную безопасность, улучшить методы доставки и опробовать подход на более крупных и более похожих на человека животных. Тем не менее исследование даёт убедительное доказательство принципа, что тщательно нацеленная генная редакция может безопасно выключить токсичный повтор, не затрагивая близкородственные гены. Эту стратегию однажды могут адаптировать не только для NIID, но и для других заболеваний мозга и мышц, вызванных аналогичной экспансией повторов.
Цитирование: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Ключевые слова: Генная редакция CRISPR, нейронная интраядерная включенная болезнь, заболевания, вызванные экспансией повторов, NOTCH2NLC, нейродегенерация