Clear Sky Science · ru
Проектирование универсальных триптофансинтаз на основе последовательностей с помощью генеративного ИИ
Обучая ферменты новым трюкам с помощью ИИ
Современное общество работает на молекулах — лекарствах, материалах и специальных химикатах, которые часто получают с помощью энергозатратных и загрязняющих процессов. Катализаторы природы, ферменты, способны выполнять похожие задачи чисто и эффективно, но найти или создать подходящий фермент для новой промышленной задачи медленно и с неопределённым результатом. В этом исследовании показано, что генеративный искусственный интеллект — тот же класс технологий, что стоит за текстовыми чат‑ботами — можно использовать для проектирования совершенно новых ферментов, которые не только хорошо работают в лаборатории, но иногда превосходят лучшие образцы, достигнутые эволюцией и годами инженерной работы.
Почему ферменты важны в повседневной жизни
Ферменты — это крошечные белковые машины, ускоряющие химические реакции в живых клетках. Химики научились использовать их для производства лекарств, пищевых ингредиентов и других ценных продуктов с меньшими энергозатратами и с применением менее токсичных реагентов по сравнению с традиционной химией. Проблема в том, что для каждого нового применения требуется фермент с «точно подходящими» свойствами — способный принимать определённые исходные вещества, выдерживать условия обработки и давать высокий выход. Классическая «направленная эволюция» улучшает ферменты путём создания и тестирования множества мутантов из поколения в поколение. Это работает, но требует приличного исходного фермента и может занимать месяцы или годы проб и ошибок, оставляя многие полезные реакции неизученными.
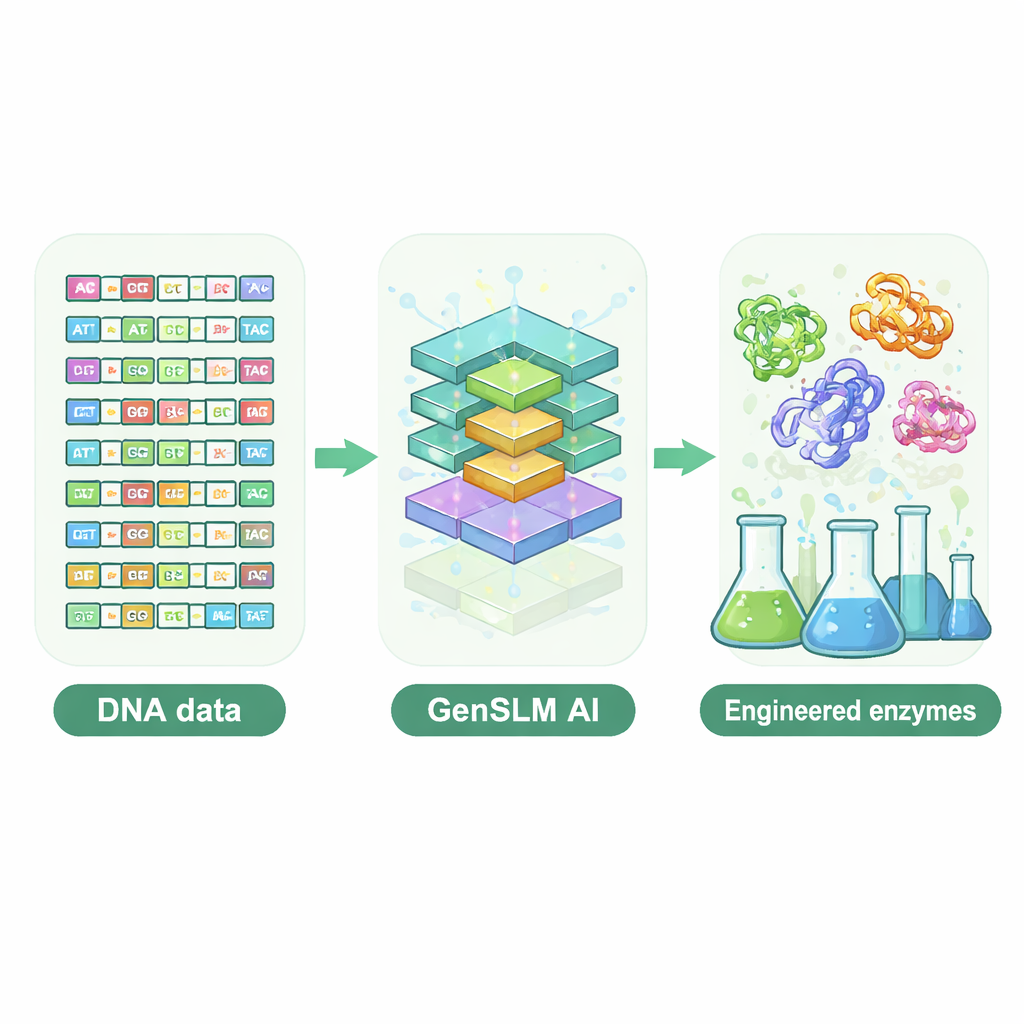
Позволив языковой модели писать ДНК
Исследователи обратились к языковой модели на геномном масштабе, названной GenSLM, которая учится закономерностям в ДНК так же, как языковая модель изучает грамматику и стиль текста. Вместо работы с готовыми белковыми последовательностями GenSLM читает и пишет ДНК триплетами кодонов, отражая то, как клетки транслируют гены в белки. Команда сначала донастроила GenSLM на десятках тысяч естественных генов для одной особенно сложной субъединицы фермента — TrpB, участвующей в синтезе аминокислоты триптофан. Затем они попросили модель сгенерировать тысячи полностью новых генов trpB. Простые вычислительные фильтры отсеяли последовательности слишком короткие или слишком длинные, вряд ли правильно сворачивающиеся или почти идентичные известным природным ферментам, оставив для экспериментальной проверки в бактериях 105 разнообразных кандидатов.
От компьютерных проектов до работающих катализаторов
Когда эти 105 спроектированных ИИ ферментов TrpB были произведены в E. coli, многие правильно сворачивались и синтезировались в больших количествах. Десятки смогли выполнить свою основную функцию: превращать индол и природного партнёра — серин — в триптофан. Некоторые работали устойчиво даже при повышенных температурах, несмотря на отсутствие явной целенаправленной работы над термоустойчивостью. В параллельных тестах часть GenSLM‑TrpB сравнялась или превзошла эталонный фермент, который годами тщательно эволюционировали в лаборатории, чтобы он функционировал самостоятельно при 75 °C. Один выдающийся дизайн, обозначенный как 230, произвёл больше триптофана, чем этот промышленный эталон как при комнатной температуре, так и при высокой, показывая, что модель, обученная только на данных о последовательностях, может сразу достигать высочайших показателей.
Новая гибкость, превосходящая природные возможности
Команда затем опробовала ферменты на панели непригодных природных субстратов — производных индола, другом алкогольподобном партнёре и фторированном соединении, используемом в производстве лекарств. Природные версии TrpB обычно разборчивы: они сильно предпочитают свои нативные субстраты и почти не активны на таких альтернативах. Удивительно, но сгенерированные ИИ ферменты часто оказались более «авантюрными». Для каждого протестированного непригодного субстрата как минимум один дизайн GenSLM продемонстрировал измеримую активность, и многие работали лучше, чем природные ферменты. Снова вариант 230 выделялся, превращая все семь альтернативных субстратов с выходами от умеренных до почти полных — широта «попустительства», не бывшая ранее описана в этом семействе ферментов. При этом при сравнении 230 с его ближайшим природным родственником — отличающимся всего в 78 из ~400 аминокислот — выяснилось, что природный фермент лишён этой универсальности, хотя его общая структура и ключевые остатки в активном центре почти идентичны.
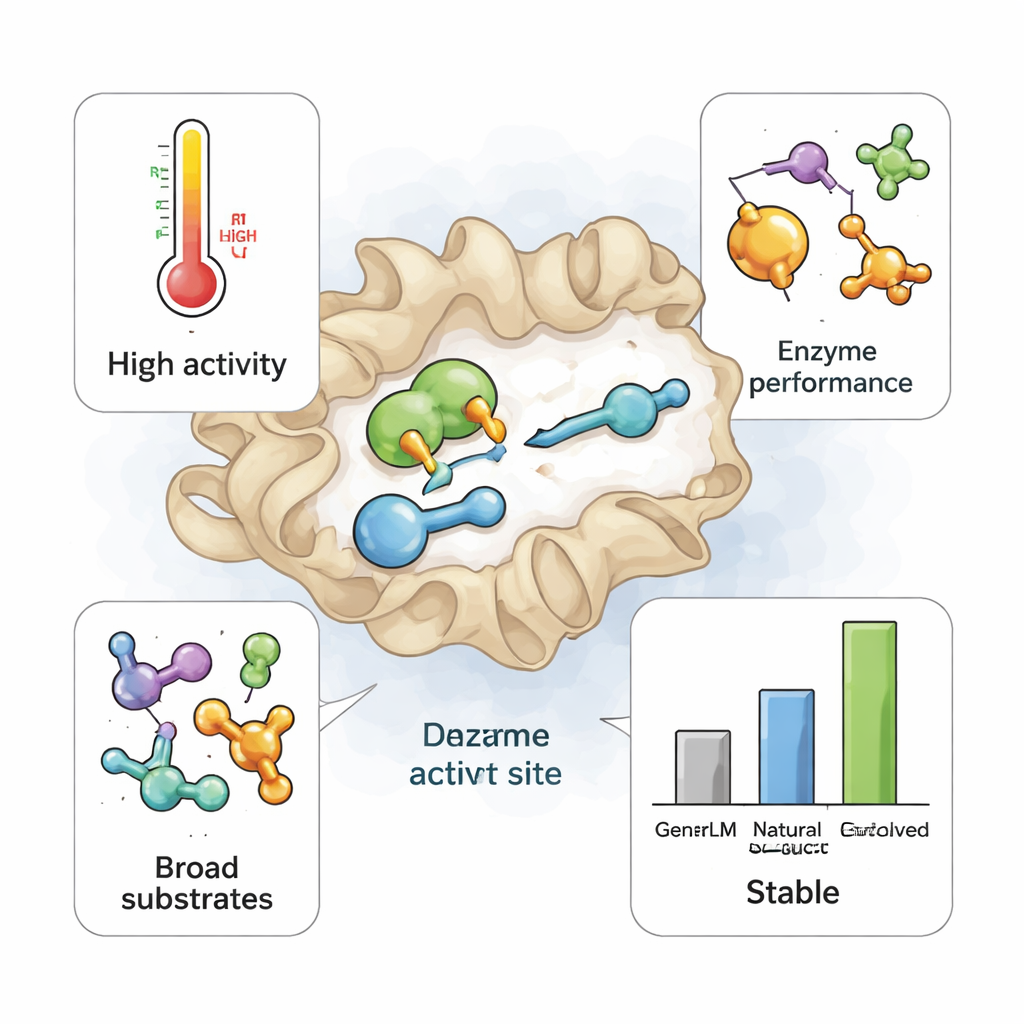
Что это значит для будущей «зеленой» химии
Для неспециалиста ключевая мысль в том, что ИИ‑модель, обученная только на существующих ДНК‑последовательностях, может представить реалистичные новые ферменты, которые природа не пробовала, и некоторые из них оказываются лучшими инструментами для химии, чем те, что мы используем сегодня. Эти спроектированные ИИ варианты TrpB сохраняют основную форму и функцию своих природных родственников, но приобретают необычную способность работать со множеством разных исходных материалов. Такая гибкость может существенно сократить объём лабораторной работы, необходимой для обнаружения ферментативных путей к новым лекарствам и другим продуктам. По мере того как дизайн, синтез ДНК и тестирование становятся быстрее и дешевле, аналогичные генеративные модели могут превратить поиск ферментов из меданной охоты за сокровищами в быструю рутинную задачу разработки, способствуя переносу большей части промышленной химии на более чистые, фермент‑основанные процессы.
Цитирование: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Ключевые слова: инжиниринг ферментов, генеративный ИИ, дизайн белков, триптофансинтаза, биокатализ