Clear Sky Science · ru
Tmem110 регулирует конформацию TRPML1 для поддержания эндолизосомального гомеостаза и предотвращения утечки митохондриальной ДНК и патологической переработки собственной ДНК
Почему утечка ДНК после травмы имеет значение
Когда мы переживаем тяжёлую травму, например сильный удар по голове, повреждения не ограничиваются местом удара. У многих пациентов развивается опасная системная реакция, при которой начинаются сбои в работе лёгких, печени, почек и других органов. В этом исследовании показано, как крошечные структуры внутри клеток — лизосомы, митохондрии и иммунные сенсоры — взаимодействуют, чтобы решить, будет ли организм тихо убирать мусор или скатится в самоцелевой иммунный ответ. Понимание этой скрытой системы уборки может открыть новые пути предотвращения отказа органов после травмы и лечения аутоиммунных и воспалительных заболеваний.
От черепно‑мозговой травмы к системному кризису
Черепно‑мозговая травма (ЧМТ) может вызвать мощную воспалительную бурю, называемую синдромом множественной органной дисфункции (MODS), но то, как повреждение в мозге распространяется на отдалённые органы, оставалось неясным. Авторы сосредоточились на моноцитах и макрофагах — иммунных клетках, патрулирующих кровь и ткани и выступающих в роли профессиональных сборщиков мусора. После ЧМТ клетки гибнут неконтролируемо и выбрасывают в циркуляцию целые митохондрии — крошечные энергетические фабрики, содержащие собственную ДНК. Эта митохондриальная ДНК (мтДНК) по виду напоминает бактериальную ДНК для иммунной системы и при отсутствии быстрого удаления может включать мощные антивирусные защитные механизмы. Обычно клетки поглощают попавшие митохондрии в кислые отсеки — лизосомы, где ферменты переваривают ДНК до того, как она просочится в цитозоль. 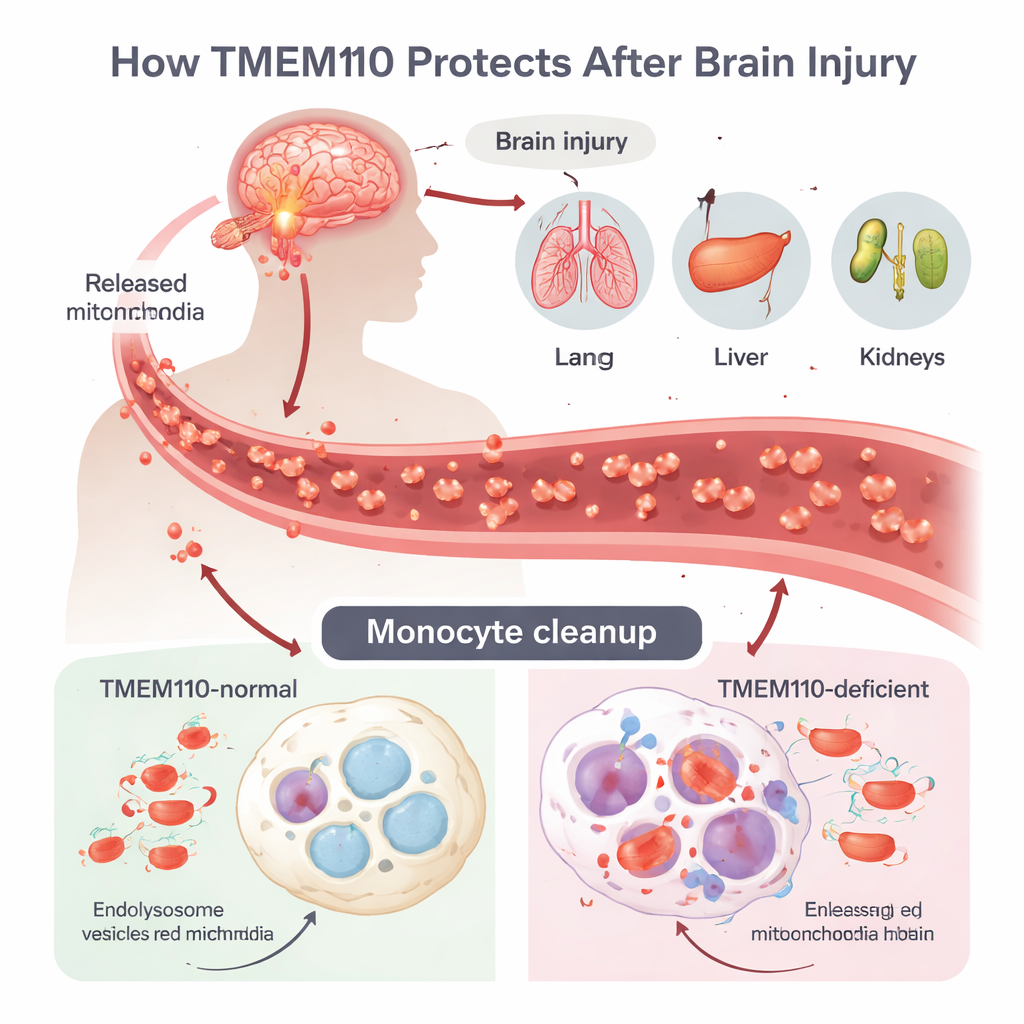
Белок‑шлюз, который стабилизирует лизосомы
Команда обнаружила TMEM110 — белок, проходящий через мембрану эндоплазматического ретикулума (важной внутриклеточной мембранной сети) — как ключевой шлюз в этом процессе. Используя генетически модифицированных мышей, у которых TMEM110 отсутствовал только в моноцитах и макрофагах, они создали контролируемую модель травмы мозга. По сравнению с нормальными мышами животные с дефектом TMEM110 демонстрировали намного более высокие уровни интерферонов типа I — мощных антивирусных сигнальных молекул — в крови и спинномозговой жидкости. Лёгкие, печень, почки и лимфоузлы у них были более повреждены, а долгосрочная выживаемость после ЧМТ существенно снижена. Блокирование рецептора интерферонов типа I или замена мутантного костного мозга нормальными клетками уменьшали повреждение органов и смертность, что указывает на то, что чрезмерная интерферонная сигнализация периферических моноцитов является ключевым драйвером MODS в этой модели.
Как нарушение ионного гомеостаза позволяет ДНК ускользнуть
Изучая эти иммунные клетки детальнее, авторы обнаружили, что у клеток без TMEM110 лизосомы были химически дисбалансированы: они были менее кислыми и перегружены кальцием. В таких условиях фермент DNase II — который обычно расщепляет ДНК в лизосомах — терял активность, мембраны лизосом становились хрупкими, и мтДНК просачивалась в окружающий цитозоль. Лабораторные эксперименты с человеческими моноцитами, поглощающими меченные донорские митохондрии, подтвердили: при отсутствии TMEM110 больше мтДНК вытекало в цитозоль и вызывало всплеск генов, стимулируемых интерфероном. Исследование показывает, что TMEM110 действует через регуляцию другого белка — ионного канала лизосом TRPML1. В присутствии TMEM110 он физически контактирует с TRPML1 и переводит его в «открытую» конформацию, создавая на поверхности лизосомы микрогорячие точки высвобождения кальция. Эти контролируемые потоки кальция поддерживают нужную кислотность, способствуют ремонту мембраны и удержанию мтДНК для её деградации внутри лизосом. 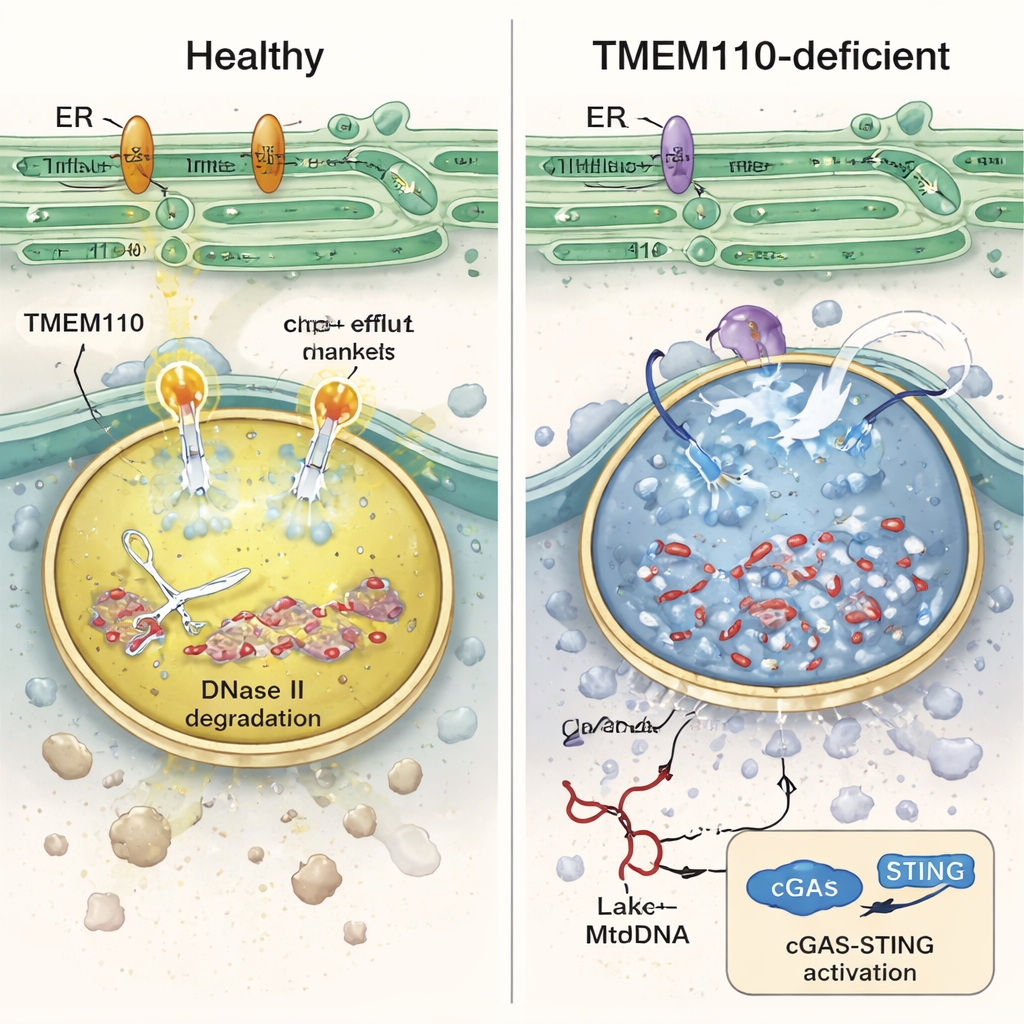
Обратная связь с системой распознавания ДНК клетки
Как только мтДНК попадает в цитозоль, её распознаёт путь cGAS–STING — основной клеточный «тревожный» механизм для чужеродной ДНК. Интересно, что TMEM110 также связывается со STING в покое и удерживает его в эндоплазматическом ретикулуме, предотвращая лишние срабатывания тревоги. Когда цитозольной ДНК становится больше, STING активируется и ослабляет связь с TMEM110. Это, в свою очередь, открывает другую область TMEM110, которая взаимодействует с TRPML1 и усиливает выброс кальция из лизосом, создавая петлю обратной связи: обнаружение собственной ДНК активирует механизм, улучшающий её очистку. Мутации в STING, связанные с ауто‑воспалительными синдромами у людей, нарушают эту передачу, запирая TMEM110 в неактивном состоянии и способствуя хронической интерферонной активации. У мышей с такой мутацией STING ЧМТ приводила к более тяжёлому повреждению органов и более высокой смертности, но доставка небольшого фрагмента TMEM110 в лизосомы с помощью мРНК–липидных наночастиц частично восстанавливала контроль над мтДНК и улучшала выживаемость.
Подсказки от пациентов и пути к новым лечениям
Авторы затем изучили клиническую когорту из 143 человек с травматической ЧМТ и MODS. Пациенты, у которых моноциты в ранний посттравматический период содержали больше TMEM110, с большей вероятностью восстанавливали функцию органов и выживали. У тех, у кого TMEM110 был снижен, наблюдалось больше циркулирующей мтДНК и деклетаризованных митохондрий, более выраженные интерферонные ответы, более высокие показатели органной недостаточности и более широкий профиль аутоантител, включая антитела к ДНК и ядерным белкам. Эти паттерны тесно соответствовали результатам у мышей, поддерживая идею о том, что контроль стабильности лизосом и утилизации мтДНК, управляемый TMEM110, является общим механизмом в человеческом заболевании.
Что это значит для пациентов с тяжёлыми травмами
Проще говоря, эта работа говорит о том, что после серьёзной травмы иммунной системе приходится делать тонкий выбор: бесшумно переварить поток собственной ДНК, высвобождённой из погибших клеток, или принять её за вирусное вторжение и развернуть тотальную атаку, которая может повредить собственные органы. TMEM110, настраивая ионный канал лизосомы и координируя работу с датчиком ДНК STING, помогает клеткам выбрать более безопасный путь. Когда эта система даёт сбой — из‑за отсутствия TMEM110, мутаций в STING или перегрузки лизосом — мтДНК утекает, сигнал тревоги не стихает, и развивается множественное повреждение органов. Нацеленная терапия на ось TMEM110–TRPML1–STING, например с применением мРНК‑терапии, направленной в лизосомы, может предложить новый подход к профилактике или лечению отказа органов и осложнений, похожих на аутоиммунные, после тяжёлой травмы.
Цитирование: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Ключевые слова: черепно‑мозговая травма, митохондриальная ДНК, лизосомы, интерферон типа I, путь cGAS‑STING