Clear Sky Science · ru
Крио-ЭМ структура человеческого убиквитин-лигазирующего комплекса COP1-DET1
Как клетки решают, какие белки разрушать
Внутри каждой клетки тысячи белков должны постоянно синтезироваться, перестраиваться или разрушаться в нужный момент. В этой статье рассматривается одна из ключевых машин клеточного «контроля качества» — молекулярная дробилка, решающая, когда удалять мощные регуляторы генов, связанные с раком и развитием. Получив её трёхмерную структуру с близкой к атомной детализацией, авторы показывают, как эта машина переключается между неактивным, сложенным состоянием и активной формой, обрабатывающей субстрат — понимание, которое в перспективе может помочь в разработке лекарств для её активации или подавления.
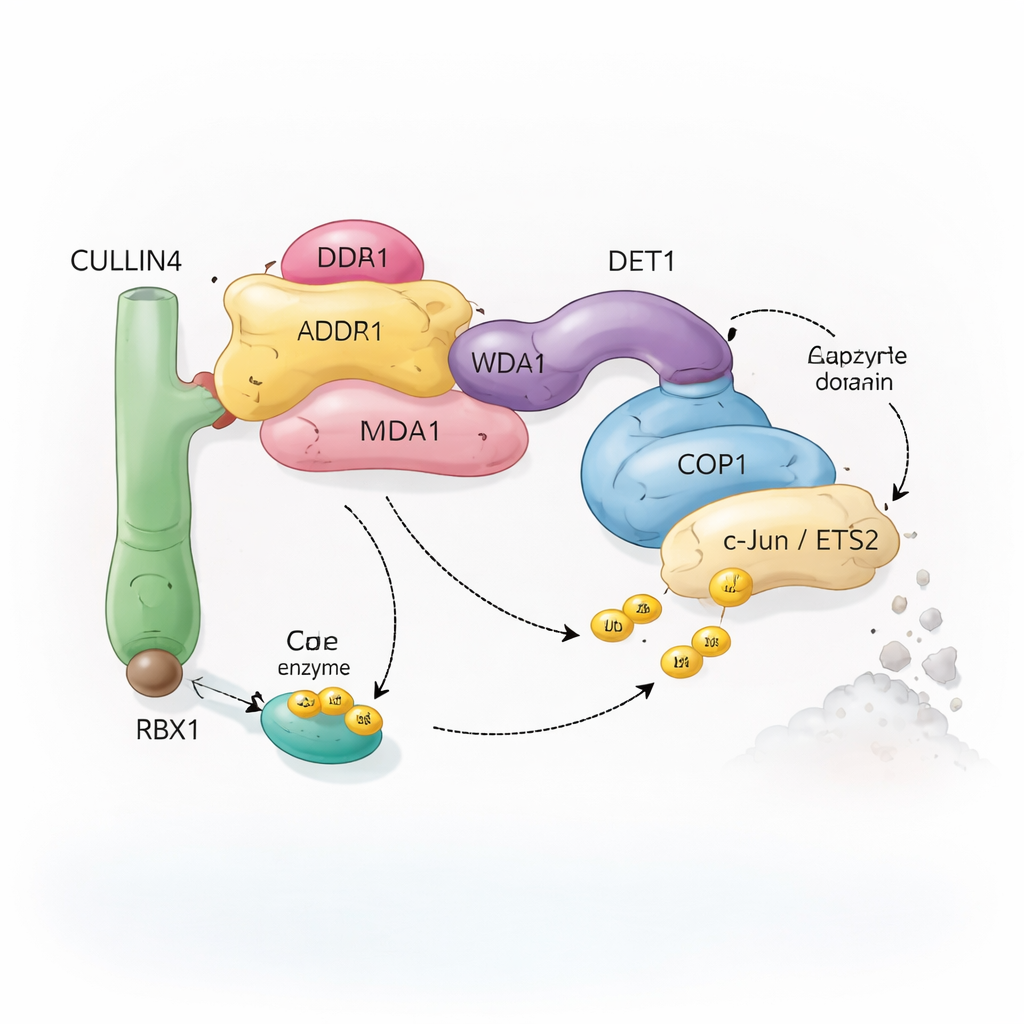
Молекулярная команда по переработке со множеством компонентов
Клетки полагаются на систему убиквитинирования, чтобы помечать белки для переработки. Молекулы убиквитина действуют как съёмные флажки, указывающие клетке, нужно ли изменить белок, переместить его или разрушить. Специальные ферментные комплексы, известные как убиквитин-лигазы, прикрепляют эти метки к выбранным мишеням. Исследуемый здесь комплекс сосредоточен вокруг COP1 — белка, встречающегося от растений до человека, который помогает помечать важные факторы транскрипции, контролирующие, какие гены включаются или выключаются. COP1 не действует в одиночку: он входит в более крупную сборку, построенную вокруг каркасного белка CULLIN4 и нескольких адаптеров, называемых DDB1, DDA1 и DET1. Вместе эти компоненты образуют гибкую «команду по переработке», которая распознаёт специфические факторы транскрипции, такие как c‑Jun и ETS2, многие из которых участвуют в росте клеток и раке.
Запечатление комплекса в 3D
Чтобы понять, как действует эта команда, исследователи использовали крио‑электронную микроскопию одиночных частиц — метод, который позволяет получать изображения быстро замороженных белков и реконструировать их формы с высоким разрешением. Они воссоздали систему COP1–DET1 человека в культурах клеток, очистили комплексы и визуализировали несколько различающихся структурных состояний. Сначала они решили структуру модуля DDB1–DDA1–DET1, выступающего в роли центрального узла. DET1 принимает необычную, частично гибкую форму, а не жёсткий диск, с выступающей «лапой», которая может захватывать партнёрные ферменты. Затем, добавив COP1 и класс вспомогательных ферментов, известных как E2, они получили более крупные сборки, показывающие, как все части сочетаются, раскрывая как компактные стопки, так и более открытые димерные (состоящие из двух COP1) варианты.
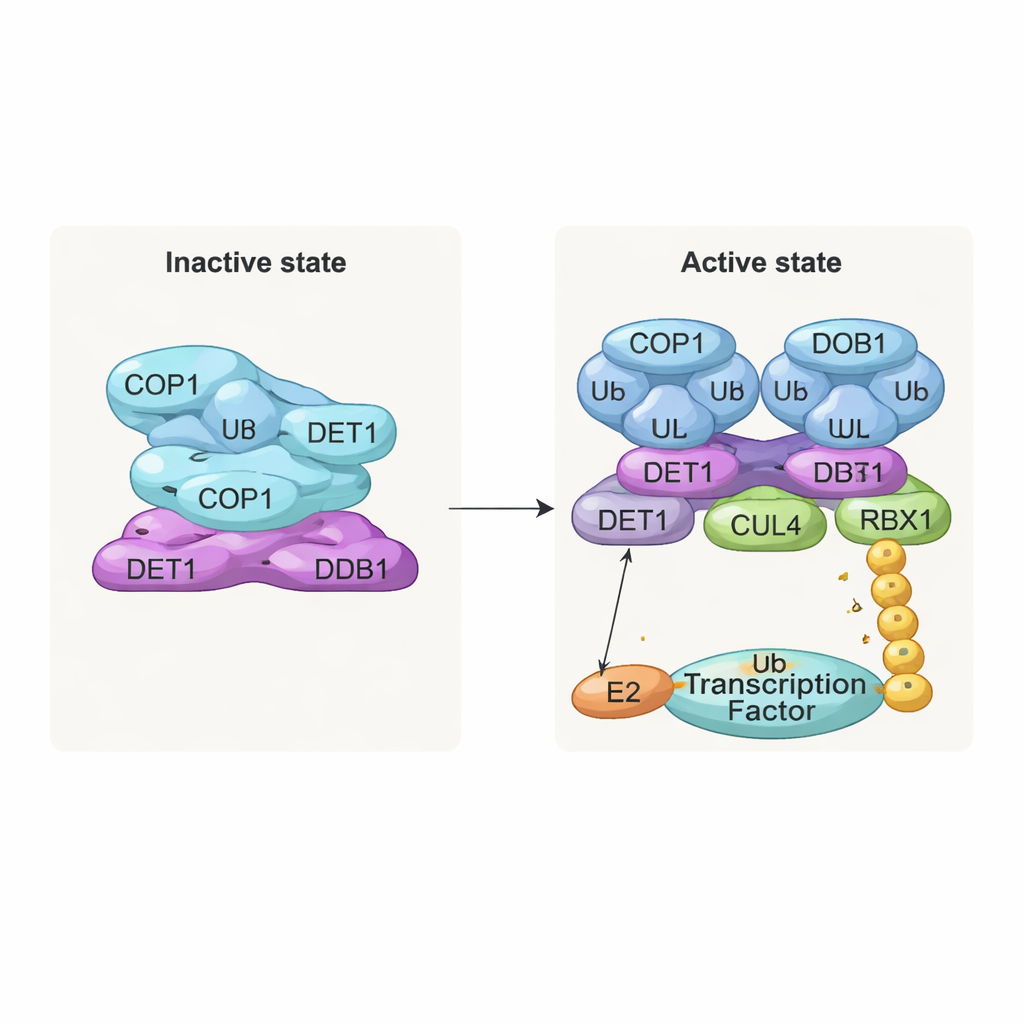
Неактивная стопка и активный димер
Одно из наиболее поразительных наблюдений — стопчатая, нитеподобная структура, состоящая из повторяющихся слоёв комплекса. В каждом слое восемь молекул COP1 переплетаются через свои коил‑коил сегменты, образуя ромбовидное кольцо. Их области распознавания субстрата, называемые доменами WD40, все направлены в одну сторону и частично экранированы соседними слоями. Такая плотная упаковка, вероятно, представляет «выключенное» состояние, при котором доступ для целевых белков ограничен. Напротив, при изучении комплексов, ко‑экспрессированных с субстратами COP1, такими как c‑Jun или ETS2, они увидели другую, димерную форму: две молекулы COP1, расположенные рядом, с внешне обращёнными доменами WD40, доступными для связывания коротких «VP» мотивов, встречающихся во многих факторах транскрипции. Биохимические тесты подтвердили, что только это димерное состояние эффективно поддерживает наращивание длинных цепочек убиквитина на c‑Jun.
DET1 как гибкий мост и регулятор трафика
DET1 выступает ключевым организатором, связывающим все части машины. Его N-концевой участок вклинивается в DDB1, якоря комплекс к каркасу CULLIN4, в то время как «лапа» обвивает семейство ферментов E2, называемых Ube2e. Детальные мутационные эксперименты показывают, что именно DET1, а не COP1, непосредственно захватывает эти E2, позиционируя их близко к каталитическому RING‑региону COP1. В таком расположении Ube2e, по‑видимому, помогает поместить первые молекулы убиквитина на субстрат. Затем второй фермент E2, Ube2d3, привлекается через плечо CULLIN4–RBX1 для удлинения этих меток в длинные цепочки, сигнализирующие о полном разрушении. Иными словами, DET1 действует как гибкий мост, подающий один E2 к COP1, тогда как крупный каркас привлекает второй E2 для завершения работы.
Почему это важно для здоровья и болезней
Сопоставляя эти структурные состояния и их функции, исследование объясняет, как один и тот же набор белков может чередоваться между простоявшей, стопчатой формой и активным димером, нацеленным на уничтожение факторов транскрипции. Это переключение особенно важно для факторов вроде c‑Jun, которые стимулируют деление клеток и тесно связаны с раком при нарушении регуляции. Понимание того, как COP1 и DET1 сотрудничают — как «лапа» DET1 выбирает специфические E2, как поверхность WD40 COP1 распознаёт субъекты, содержащие VP‑мотивы, и как формируется активный димер — даёт схему для дальнейших исследований. В перспективе лекарства, стабилизирующие неактивную стопку или смещающие равновесие в пользу активного димера, могли бы дать новые способы регулировать пути контроля генов при раке и других заболеваниях, где переработка белков нарушена.
Цитирование: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Ключевые слова: убиквитин-лигаза, COP1, распад белков, крио-ЭМ структура, c-Jun