Clear Sky Science · ru
К48-убиквитин-зависимые протеазы расщепляют белки после выхода из ЭР
Как клетки решают, какие белки уничтожить
Наши клетки постоянно удаляют изношенные или повреждённые белки, особенно те, которые встроены в мембраны и выполняют функции ворот и сенсоров. В этой работе показано, что клетки используют крошечную метку — убиквитин — не просто как универсальную «мусорную» метку, а как код, который указывает мембранным белкам точный способ их утилизации. Понимание этого кода помогает объяснить, как клетки поддерживают здоровье, и может направить будущие терапевтические подходы, нацеленные на разрушение болезнетворных белков.
Клеточный штрих-код для утилизации белков
Клетки помечают нежелательные белки цепочками небольшого белка убиквитина. Эти цепочки могут связываться по-разному, подобно нитям, продетым через разные отверстия, и каждый узор может сигнализировать о разной судьбе белка. Авторы сосредоточились на мембранных белках, которые уже покинули эндоплазматический ретикулум (ЭР) и перемещаются через такие отделы, как Гольджи и эндосомы. Они спросили, являются ли два распространённых типа цепочек — K48-связанные и K63-связанные убиквитины — взаимозаменяемыми ярлыками или же направляют груз в разные пути разрушения.
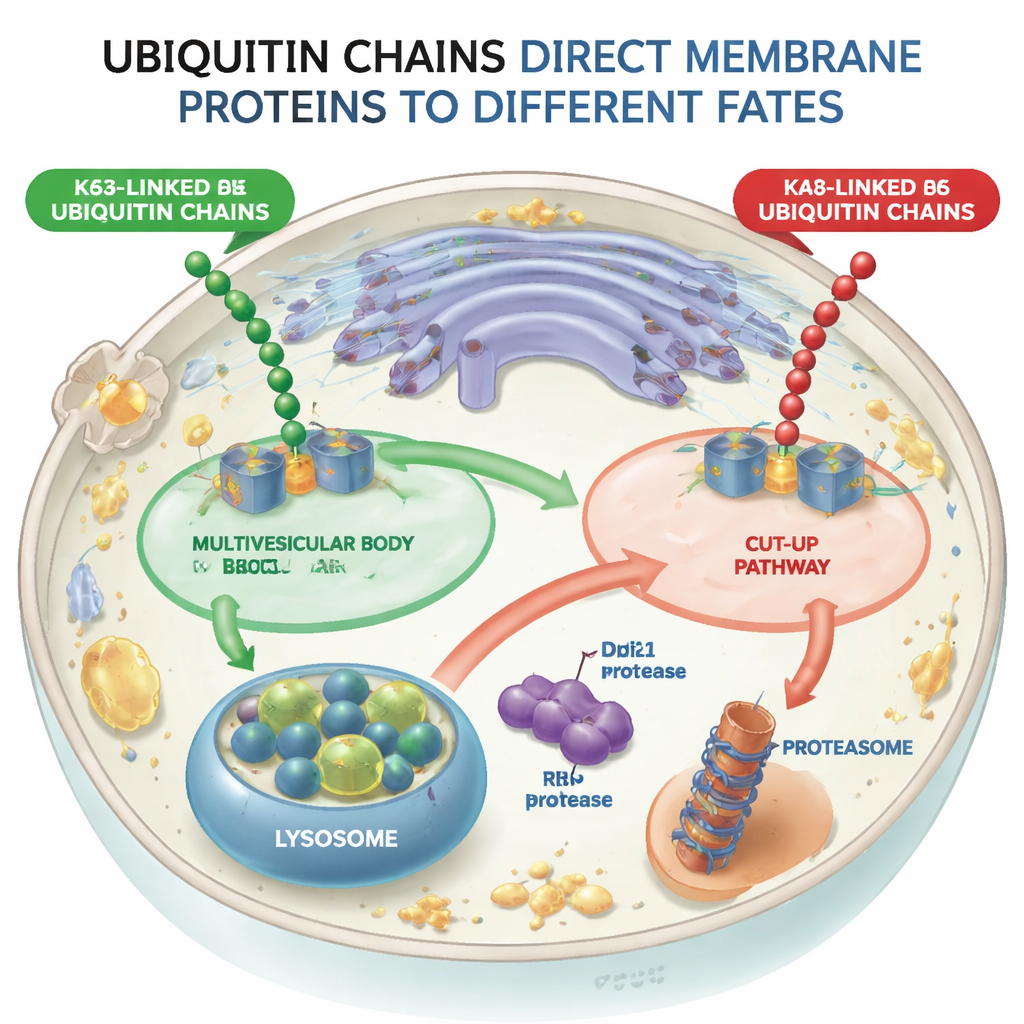
Два расходящихся пути для промаркированных белков
Используя дрожжи в качестве модели, исследователи сконструировали молекулярные машины (лигазы убиквитина), которые могли прикреплять либо K48-связанные, либо K63-связанные цепочки к одному и тому же тестовому мембранному белку — сортировочному рецептору Vps10. Когда Vps10 получал K63-цепочки, он направлялся во внутренние везикулы внутри эндосом — структуры, известные как мультивезикулярные тельца, которые в конечном итоге сливаются с лизосомами, пищеварительными отделами клетки. Напротив, когда Vps10 нес K48-цепочки, он не следовал по этому мультивезикулярному пути. Вместо этого он разрушался иначе, что показывает: клетка различает эти два типа цепочек и что путь через мультивезикулярные тельца по сути отвергает грузы, помеченные K48.
Путь «CUT-UP», который разрезает белки на части
Команда обнаружила, что K48-связанные цепочки запускают путь срезания белков, который они назвали CUT-UP, сокращение от Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases (расщепление убиквитинированных мишеней убиквитин-зависимыми протеазами). Вместо того чтобы вытаскивать весь белок из мембраны целиком, CUT-UP разрезает его на фрагменты, которые затем добираются до обычных систем утилизации клетки. Один ключевой фермент, Ddi1, плавает в цитозоле и отрезает ту часть мембранного белка, которая обращена в цитоплазму. Этот фрагмент затем расщепляется протеасомой — главным шредером белков в клетке. Одновременно другой фермент, Rbd2, локализован в самой мембране и отрезает ту часть белка, обращённую в просвет компартмента, освобождая её в пространство, которое в конечном счёте соединяется с лизосомой. Для полного сохранения K48-меченного Vps10 от разрушения требовалось блокирование Ddi1, Rbd2, протеасомы и лизосомных ферментов одновременно, что подтверждает кооперацию всех этих компонентов в пути CUT-UP.
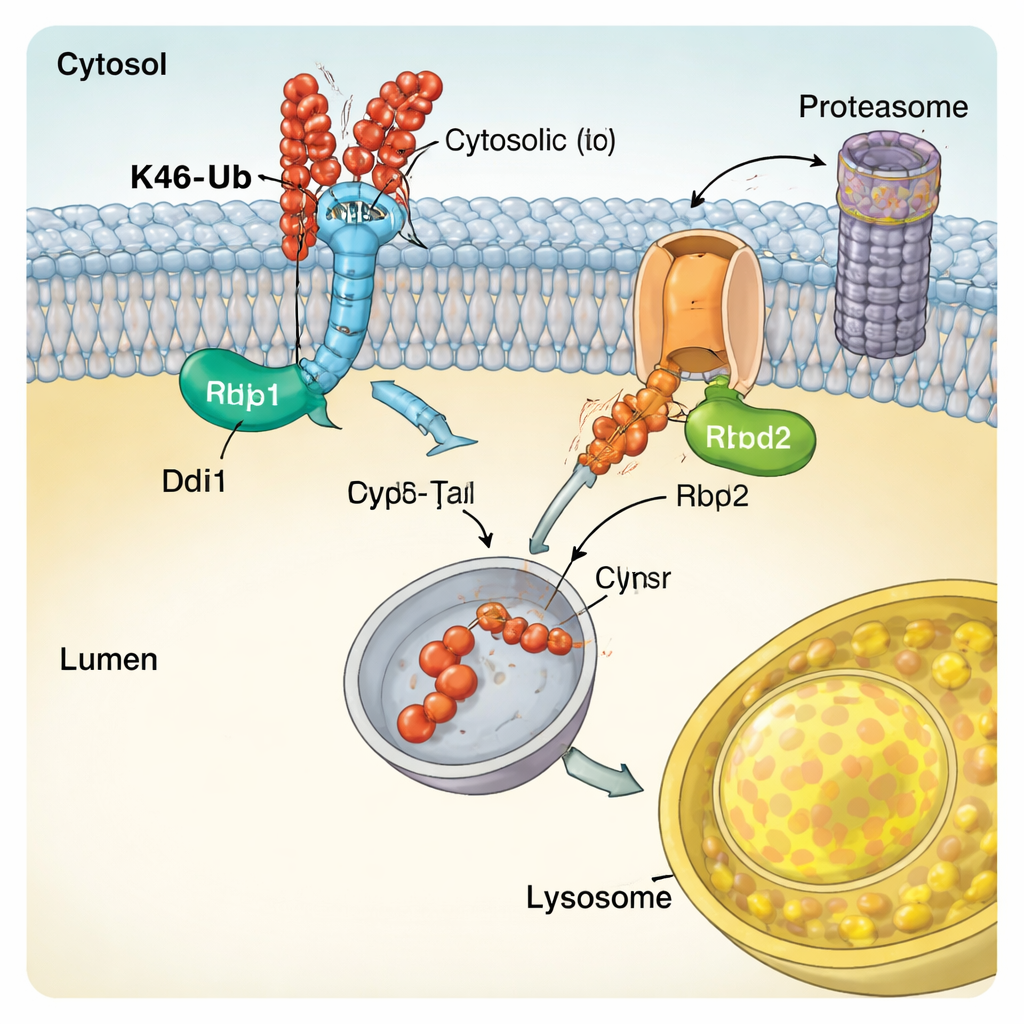
Специализированные ферменты, читающие убиквитиновый код
Чтобы понять, как CUT-UP распознаёт свои мишени, авторы изучили молекулярные особенности Ddi1. Они показали, что центральное каталитическое ядро Ddi1 не только расщепляет белки, но и может напрямую связывать убиквитин, а его активность регулируется дополнительными областями, которые цепляются за убиквитиновые цепочки. Ddi1 продемонстрировал особую зависимость от K48-связанных цепочек, что согласуется с его ролью в CUT-UP. Rbd2, в свою очередь, является ромбоидной протеазой, пронизывающей мембрану. Исследование показало, что активный центр Rbd2 необходим для разрезания просвет-ориентированных частей Vps10 и что фермент перемещается через несколько секреторных компартментов, что позволяет ему действовать в разных участках клетки. Похожие ферменты присутствуют в клетках человека и связаны с состояниями от нейродегенерации до рака, что указывает на то, что механизмы, подобные CUT-UP, могут иметь широкое значение.
Почему это важно для здоровья и терапии
Показав, что разные типы убиквитиновых цепочек направляют один и тот же мембранный белок в резко различные судьбы — либо в сортировку в мультивезикулярные тельца, либо в расщепление посредством CUT-UP — эта работа даёт убедительные доказательства того, что клетки используют подлинный «убиквитиновый код» для тонкой настройки утилизации белков. Открытие CUT-UP проясняет, как упрямые мембранные белки могут быть разобраны по кусочкам, и выделяет Ddi1 и Rbd2 как ключевых участников, которые читают и реализуют этот код. Для неспециалистов главный вывод таков: клетки не просто помечают белки как мусор; они указывают, каким образом этот мусор будет вывезен. По мере того как разработчики лекарств создают инструменты, помечающие вредоносные белки убиквитином для их удаления, понимание путей вроде CUT-UP будет необходимо, чтобы предсказывать, какие фрагменты образуются и как это может влиять на поведение клетки.
Цитирование: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Ключевые слова: убиквитиновый код, разрушение белков, мембранные белки, протеасома, лизосома