Clear Sky Science · ru
Потеря кворм‑сенсора Fsr способствует образованию биопленок и ухудшает исходы при энтерококковом инфекционном эндокардите
Тихие диверсанты на сердечных клапанах
Инфекционный эндокардит — это потенциально смертельная инфекция сердечных клапанов, и она становится всё более распространённой во всём мире. В этом исследовании внимание сосредоточено на главном виновнике — кишечной бактерии Enterococcus faecalis — и на том, почему одни инфекции особенно трудно лечить. Раскрывая, как эти бактерии обмениваются сигналами и возводят защитные биопленки на клапанах сердца, учёные объясняют, почему некоторые штаммы вызывают более тяжёлое заболевание и сопротивляются антибиотикам, и почему одна система бактериальной связи, называемая Fsr, оказывается не ускорителем повреждений, а неожиданным тормозом.
Как бактерии строят крепости в сердце
Клапаны сердца обычно выдерживают одни из самых быстрых потоков крови в организме, но если поверхность клапана повреждена, тромбоциты и белки свертывания могут образовать крошечный сгусток или вегетацию. Этот сгусток становится посадочной площадкой для бактерий в кровотоке. При прикреплении бактерии размножаются и переплетаются в биопленку — слизистое, структурированное сообщество, которое защищает их от иммунных клеток и лекарств. Команда использовала микрофлюидные устройства, чтобы имитировать кровоток в лаборатории, и модель на крысах, чтобы воссоздать эндокардит в живом организме, что позволило наблюдать, как E. faecalis адаптируется по мере того, как инфекция переходит от нескольких разрозненных клеток к плотным зрелым биопленкам. 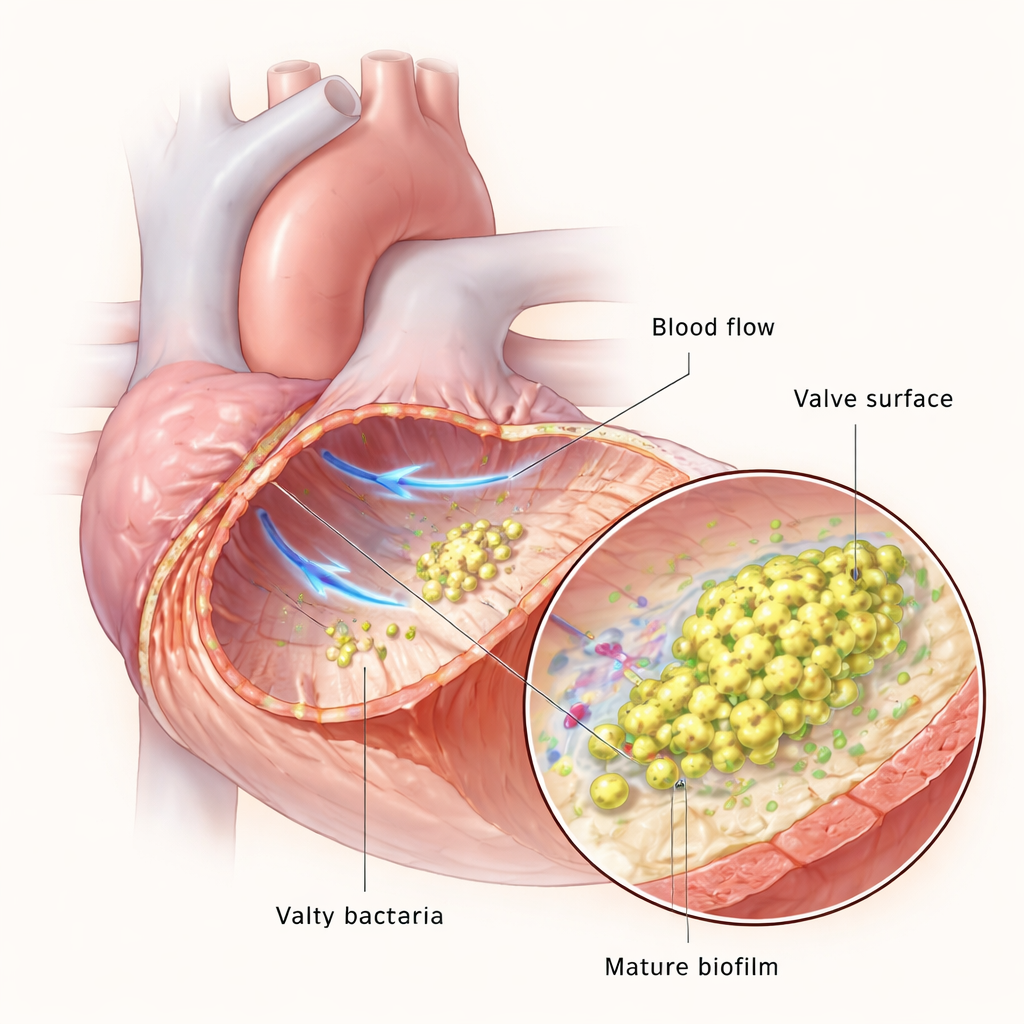
Когда быстрый кровоток глушит бактериальную «болтовню»
Бактерии часто координируют своё поведение с помощью кворум‑сенсинга — химической «голосовалки», которая включает или выключает гены, когда присутствует достаточное число клеток. Fsr — это система кворум‑сенсинга у E. faecalis. Удивительно, но исследователи обнаружили, что сильный поток жидкости фактически смывает сигнальные молекулы, необходимые для активации Fsr. На ранней стадии инфекции, когда бактерии прикреплены к оголённой поверхности вегетации и испытывают полное давление кровотока, Fsr в основном молчит. Только позже, когда микроколонии вырастают и оказываются глубже внутри вегетации — защищённые от течения, — Fsr активируется. Это означает, что в реальном сердце кворум‑сенсинг определяется не только числом бактерий, но и их положением внутри трёхмерной структуры.
Отключение Fsr даёт биопленкам возможность разрастаться
Чтобы проверить, что именно делает Fsr в инфекции, команда сравнила нормальные бактерии с мутантами, лишёнными всей системы Fsr. На ранних этапах оба варианта одинаково колонизировали клапаны. Но к третьему дню у животных, инфицированных штаммами без Fsr, вегетации были крупнее и содержали гораздо больше упакованных в них бактерий. Детальное визуализирование показало, что их биопленки покрывали большую часть поверхности сгустка, а микроколонии были больше. Потеря Fsr также отключала два ключевых секретируемых фермента, GelE и SprE, которые обычно помогают формировать биопленку и, возможно, ограничивают чрезмерный рост. Животные, инфицированные мутантами, лишёнными лишь этих ферментов, также развивали более объёмные биопленки, хотя не столь выраженно, как у штаммов без Fsr, что указывает на участие других контролируемых Fsr факторов. 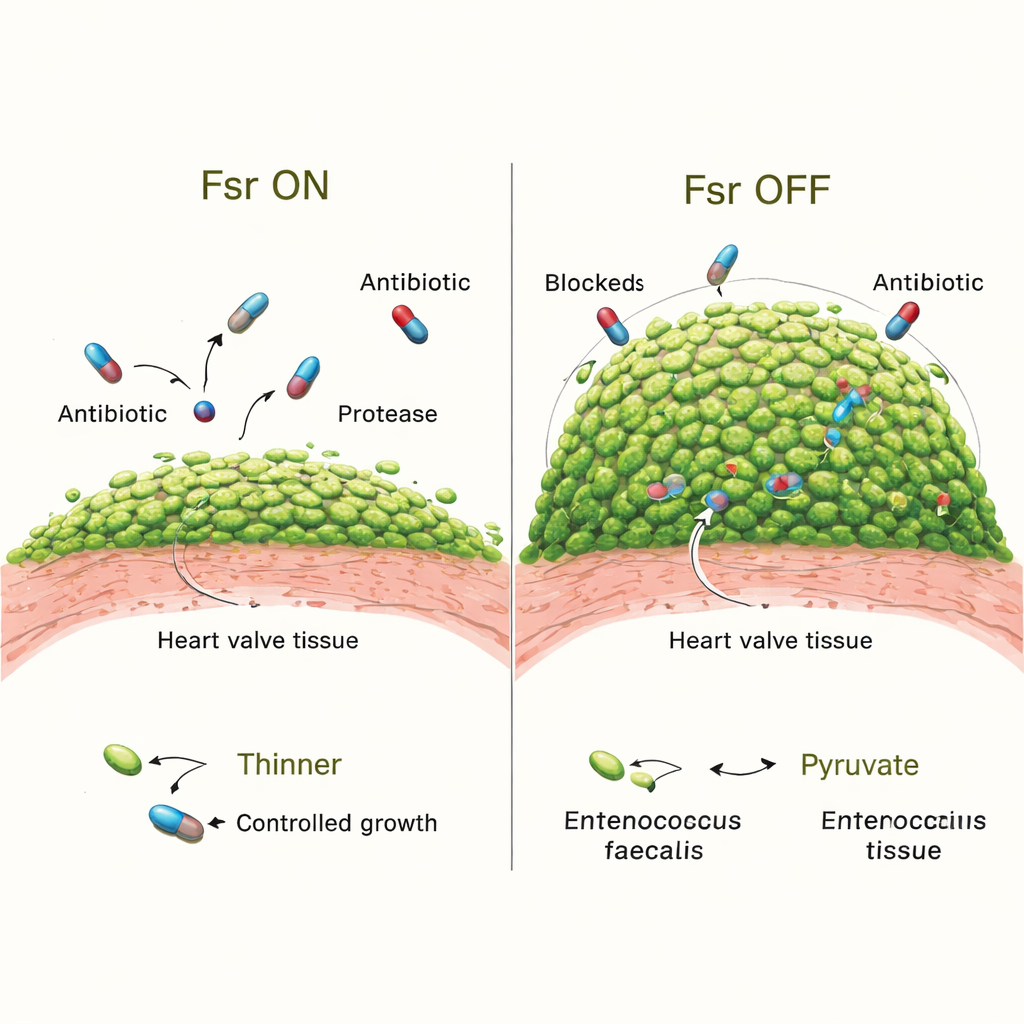
Метаболическая перенастройка и повышенная устойчивость к антибиотикам
Профилирование экспрессии генов бактерий внутри инфицированных клапанов показало, что Fsr контролирует не только пару ферментов. При отсутствии Fsr изменяла активность сотня генов, особенно тех, что связаны с захватом сахаров и производством энергии. Пара генов lrgA и lrgB выделялась: они сильно включались у бактерий без Fsr и помогали клеткам эффективнее использовать пируват — небольшой богатый энергией метаболит, присутствующий в крови. Когда исследователи удалили lrgAB вместе с Fsr, избыточный рост биопленки исчез, указывая на ключевую роль этого метаболического пути в подпитке разросшейся инфекции. Примечательно, что биопленки без Fsr были труднее поддающимися лечению. У крыс, получивших антибиотик гентамицин, инфекции нормальными бактериями сокращались, а количество тромбоцитов — маркер тяжести болезни — улучшалось. В отличие от этого, инфекции без Fsr почти не реагировали, хотя в стандартных лабораторных тестах бактерии не проявляли повышенной лекарственной резистентности.
Человеко‑специфическая особенность воспаления
Исследование также выявило потенциальный путь, с помощью которого эти бактерии могут усиливать воспаление у людей. Фермент GelE способен расщеплять человеческий предшественник иммунного сигнала IL‑1β до активной формы, которая запускает воспалительную реакцию. Любопытно, что GelE по‑другому разрезал крысиный IL‑1β, разрушая его, а точный «активирующий» разрез отсутствовал у белков крыс и мышей. Этот видоспецифический эффект указывает на то, что у людей GelE может усиливать воспаление непосредственно на границе биопленки, возможно усугубляя повреждение тканей при эндокардите.
От лаборатории к клинике: почему потеря Fsr важна для пациентов
Чтобы выяснить, имеют ли эти экспериментальные результаты значение в реальной практике, исследователи проанализировали изоляты E. faecalis от 81 пациента с инфекционным эндокардитом в Швейцарии и США. Почти половина штаммов естественно лишалась системы Fsr. Пациенты, инфицированные такими Fsr‑отрицательными штаммами, дольше имели бактериемию — больше дней с обнаруживаемыми бактериями в крови — и с большей вероятностью попадали в группу высокого риска, включающую интенсивную терапию, длительную госпитализацию, крупные сердечные операции или смерть. Другие гены вирулентности не объясняли эту картину, указывая прямо на потерю Fsr как ключевой маркер более агрессивного течения болезни.
Почему это важно для будущих терапий
Вместе эти результаты опровергают простую идею о том, что блокирование бактериальной коммуникации всегда ослабляет инфекции. При эндокардите, вызванном E. faecalis, система Fsr на самом деле сдерживает расширение биопленки и делает бактерии более уязвимыми к антибиотикам. Когда Fsr отсутствует, бактерии формируют более плотные биопленки, эффективнее используют питательные вещества крови и способствуют упорным, продолжительным инфекциям. Для пациентов это означает, что штаммы, лишённые Fsr, могут предвещать более труднолечимое заболевание, а терапии, которые без разбору подавляют кворум‑сенсинг, в этом контексте могут дать обратный эффект. Вместо этого целенаправленная работа с метаболическими путями, например использованием пирувата, или мониторинг статуса Fsr и GelE в качестве прогностических маркеров, могут предложить лучшие подходы к управлению этими опасными сердечными инфекциями.
Цитирование: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Ключевые слова: инфекционный эндокардит, бактериальные биопленки, кворум‑сенсинг, Enterococcus faecalis, толерантность к антибиотикам