Clear Sky Science · ru
Инженерный VPg saRNA обеспечивает безкапный, низкоиммуногенный и точный синтез терапевтических белков in vivo
Переписывая правила для РНК‑лекарств
Вакцины на основе матричной РНК (мРНК) помогли переломить ход пандемии COVID-19, но применять схожие молекулы для замены или дополнения отсутствующих белков при хронических заболеваниях гораздо сложнее. Организм быстро разрушает чужую РНК и запускает сильные иммунные реакции, а многие существующие конструкции самоамплифицирующей РНК склонны к ошибкам при копировании. В этом исследовании описан новый тип самоамплифицирующей РНК, созданный на основе фрагментов человеческого норовируса, который сконструирован так, чтобы быть долговечнее, менее воспалительным и необычайно точным — что открывает путь к более точным и долговременным РНК‑лекарствам.
Более умная самокопирующаяся РНК
Обычные мРНК‑лекарства несут одну «рецептуру» белка и один раз считываются клеткой, после чего разрушаются. Самоамплифицирующая РНК (saRNA) включает дополнительные вирусные элементы, которые позволяют РНК копировать себя внутри клетки, резко увеличивая выход белка при малой дозе. Наиболее изученные системы saRNA основаны на альфавирусах, но они громоздки, вызывают сильные противовирусные реакции и копируют последовательности с относительно низкой точностью. Авторы обратились к человеческому норовирусу — частой причине гастроэнтеритов. Они выделили компактный участок генетического материала норовируса и перестроили его как носитель терапевтических генов. В центре конструкции находится VPg — небольшой вирусный белок, химически связанный с 5'-концом РНК. VPg заменяет обычную «шапочку» (cap), присущую человеческим мРНК, и позволяет РНК транслироваться при участии другого набора клеточных факторов, которые менее чувствительны к определённым сигналам стресса. 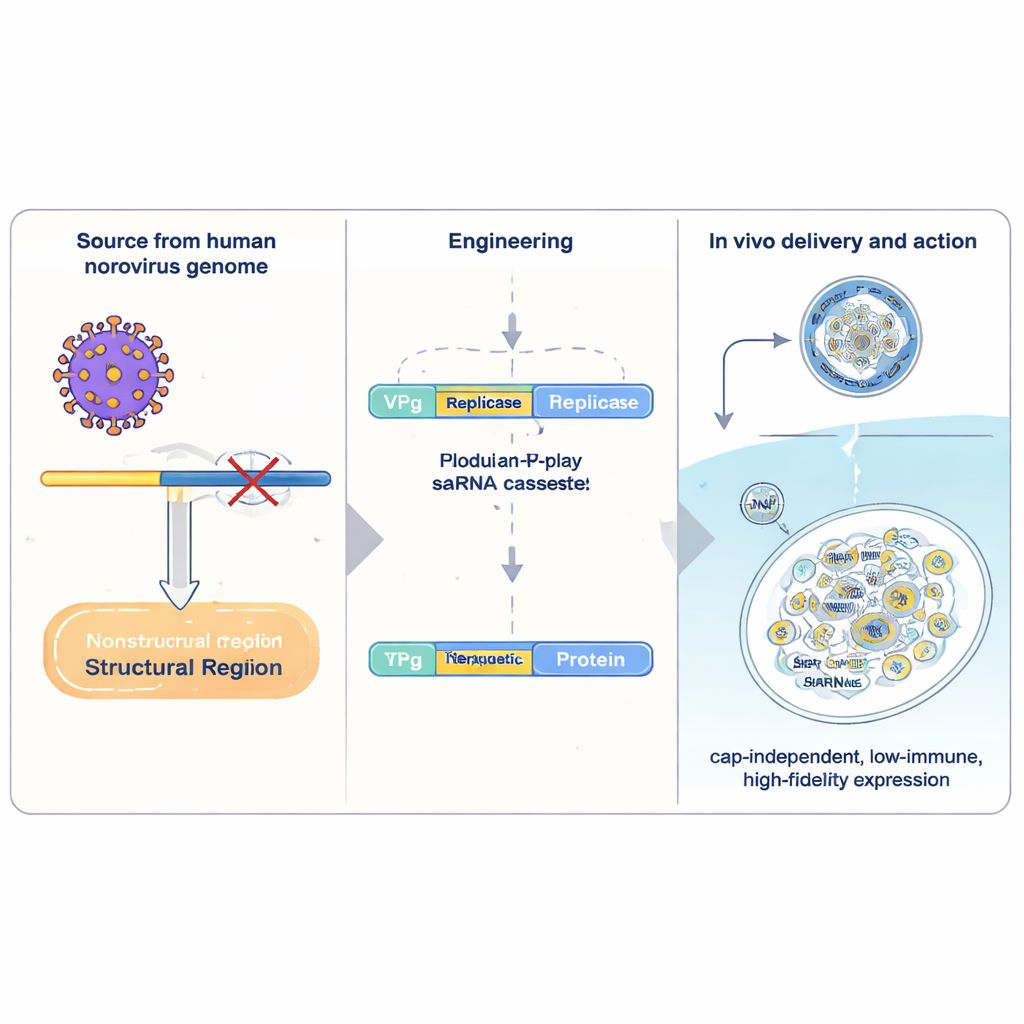
Высокая точность без раздувания иммунитета
Для белковых терапий точность важна: даже небольшие ошибки копирования могут изменить действие препарата или привести к токсичным побочным продуктам. Команда показала, что когда VPg норовируса связывается с полимеразой — ферментом, копирующим РНК — это замедляет включение неправильных нуклеотидов и резко снижает частоту ошибок. Они идентифицировали конкретные аминокислоты в VPg, контактирующие с ключевой контрольной областью полимеразы, и продемонстрировали, что нарушение этого интерфейса ухудшает точность копирования. Одновременно классические конструкции saRNA образуют большие количества двуспиральной РНК — молекулярного сигнала тревоги, который активирует противовирусные ответы и блокирует синтез белка. Перепроектировав полимеразу так, чтобы она предпочитала один специфический VPg‑связанный стартовый вариант, и реорганизовав геном так, чтобы эффективно производилась только терапевтическая нить, авторы значительно уменьшили образование двуспиральной РНК. Они также настроили хвостовую область РНК так, чтобы VPg присоединялся в нужном месте, предотвращая появление коротких непреднамеренных фрагментов, которые могли бы транслироваться в посторонние пептиды.
Работает там, где стандартная мРНК терпит неудачу
Новый VPg‑основной saRNA протестировали в сложных моделях заболеваний, где обычная кэпированная мРНК оказывается неэффективной. При раково‑ассоциированной кахексии — синдроме истощения, при котором мышцы и жир стремительно уменьшаются — ключевые факторы трансляции, распознающие стандартный мРНК‑кэп, выключаются, делая кэп‑зависимые мРНК неэффективными. Поскольку VPg использует альтернативный путь входа в машинерию трансляции клетки, он продолжал стимулировать синтез гормона аппетита и метаболизма грелина в модели панкреатического рака у мышей. Ежемесячные низкодозовые инъекции помогали сохранять мышечную массу и жировую ткань, улучшали питание и обмен веществ и умеренно продлевали выживание, без очевидной токсичности или признаков хронической активации иммунитета.
Точный удар по раку и спокойнее при аутоиммунитете
Чтобы проверить, действительно ли важна высокая точность копирования, исследователи загрузили VPg‑вектор сложным онколитическим конструктом GSDMDENG, предназначенным для разрушения митохондрий раковых клеток и стимуляции опухоле‑специфического иммунного ответа. Когда тот же конструкт поместили на классическую saRNA на основе альфавируса, в процессе многократного копирования накапливались мутации, ослаблявшие избирательное убийство раковых клеток и функцию иммуноинициации. В отличие от этого, система на базе VPg сохраняла задуманную последовательность, обеспечивала сильное уничтожение опухолевых клеток и вызывала длительные T‑клеточные ответы, которые замедляли или предотвращали рост панкреатической опухоли в моделях на мышах. Наконец, они применили VPg saRNA к другой задаче: хронической болезни «трансплантат против хозяина», когда иммунные клетки атакуют лёгкие после пересадки костного мозга. VPg saRNA, кодирующая активированный белок C, уменьшала образование вредных антител, предотвращала развитие лёгочного фиброза и улучшала дыхание у мышей, тогда как сопоставимый альфавирусный конструк вызывал более сильную врождённую иммунную реакцию и ухудшал исходы.
Почему это важно для будущих РНК‑препаратов
В сумме работа описывает компактную «plug‑and‑play» РНК‑платформу, объединяющую три желаемых свойства: точное самокопирование, дизайн, минимизирующий иммунные тревоги, и обход некоторых ограничений стандартной мРНК‑трансляции. Поскольку терапевтический ген просто замещают в фиксированном норовирусном каркасе, на одной и той же основе можно тестировать разные белки — от гормонов до факторов свертывания и онколитических агентов. Хотя перед применением у людей остаётся ещё много работы, подход VPg saRNA указывает путь к РНК‑лекарствам, которые действуют скорее как стабильные инфузии белков: низкие дозы, более длительный эффект и работоспособность даже в поражённых тканях, где обычные мРНК‑сообщения не могут надёжно читаться. 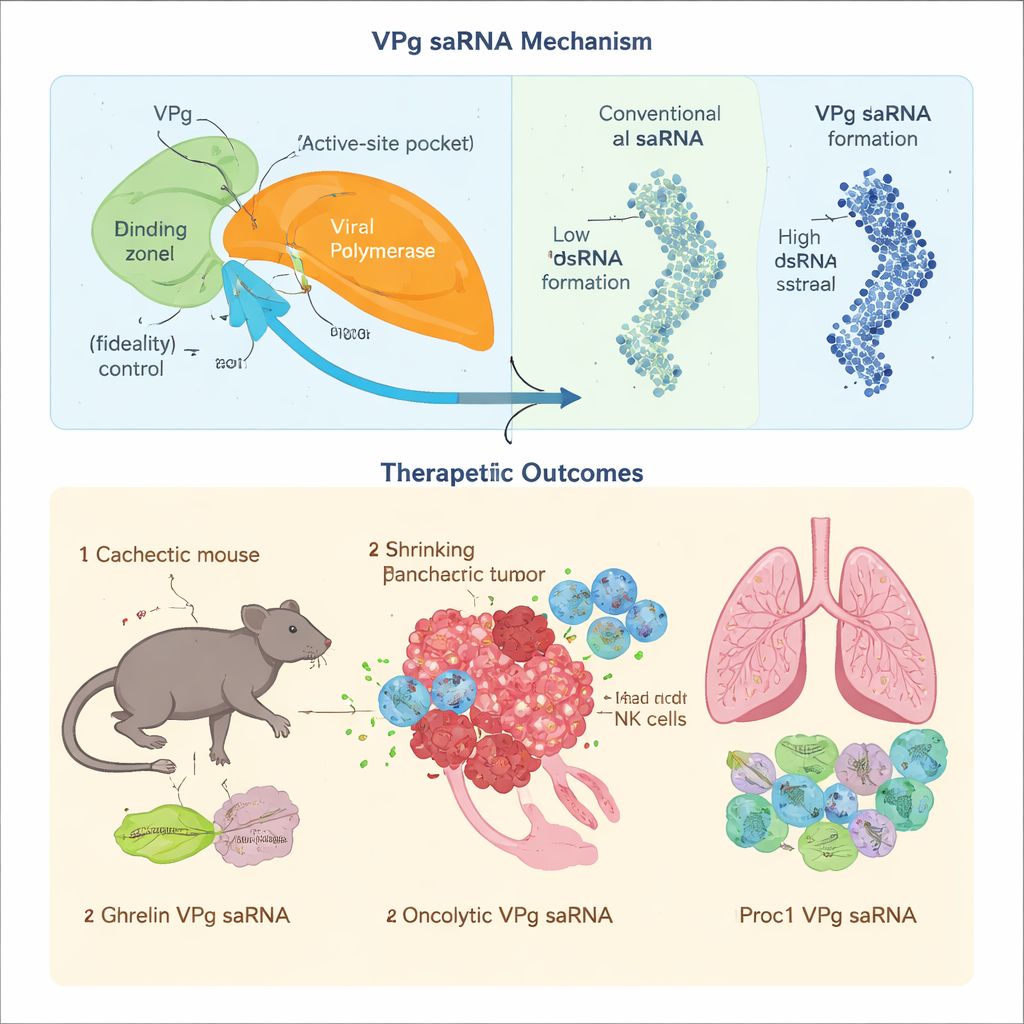
Цитирование: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Ключевые слова: самоамплифицирующая РНК, мРНК-терапия, VPg норовируса, раковая кахексия, трансплантация: болезнь «трансплантат против хозяина»