Clear Sky Science · ru
Роль низкокомплексных повторов в взаимодействиях РНК–РНК и глубокая нейросетевая платформа для предсказания дуплексов
«Липкие» последовательности РНК, формирующие поведение клетки
Внутри каждой клетки молекулы РНК постоянно сталкиваются друг с другом, образуя мимолётные союзы, которые помогают контролировать, какие гены включаются, как синтезируются белки и как развиваются клетки. В этом исследовании показано, что многие такие взаимодействия РНК–РНК не случайны: их направляют короткие, простые, сильно повторяющиеся последовательности, действующие как молекулярный «велкро». Авторы также создают инструмент искусственного интеллекта, способный обнаруживать участки, где вероятно формирование таких пар РНК, что открывает новые возможности для изучения работы клеток в норме и при заболеваниях.
Простые повторы с мощным эффектом
РНК часто описывают как посланника, переносающего генетическую информацию от ДНК к белкам, но она также служит каркасом, регулятором и направляющей. Многое из этой функции зависит от связывания двух цепей РНК друг с другом. Объединив данные нескольких крупных экспериментальных обзоров в клетках человека и мыши, авторы показывают, что регионы РНК, действительно принимающие участие в таких парных контактах, заметно обогащены тем, что они называют низкокомплексными повторами. Это участки, построенные из коротких мотивов — например, чередований оснований G и C — повторяющихся снова и снова. Вместо того чтобы быть геномным «мусором», эти повторяющиеся фрагменты оказываются первичными докинговыми площадками, где одна РНК может прикрепляться к множеству других, формируя плотные центры взаимодействий по всему транскриптому. 
РНК‑хабы для развития и регуляции
Когда команда проанализировала, какие гены несут эти контактные сайты, богатые повторами, выявилась яркая закономерность: многие из них кодируют белки, контролирующие развитие и идентичность клетки, такие как факторы транскрипции. Даже в линиях раковых клеток, которые не проходят активную дифференцировку, РНК, связанные с программами развития, были сильно вовлечены в контакты на основе повторов. Авторы также подробно рассмотрели отдельные длинные некодирующие РНК (lncRNA) — молекулы РНК, не кодирующие белки, но часто их регулирующие. Например, мишени lncRNA TINCR и другой lncRNA, важной для формирования мотонейронов, Lhx1os, обе показали избыток комплементарных повторов. В этих случаях простые повторы на lncRNA соответствуют комплементарным повторам в партнёрных РНК, что обеспечивает стабильное спаривание и может помогать настраивать уровень или трансляцию ключевых генов развития.
Где подключаются белки и ферменты редактирования
Эти контакты, опосредованные повторами, редко действуют в одиночку. Авторы наложили карты связывания белков на свои данные по взаимодействиям и обнаружили, что многие контактные сайты с повторами также узнаются РНК‑связывающими белками, вовлечёнными в контроль трансляции, распад РНК и формирование цитоплазматических гранул, таких как P‑тела и стресс‑гранулы. Один белок в частности, STAU1, способный вызывать разрушение своих РНК‑мишеней, часто связывается с дуплексами, сформированными через низкокомплексные повторы. Понижение уровня STAU1 приводило к повышению уровней РНК, участвующих в этих дуплексах, особенно несущих повторы, что указывает на то, что спаривание РНК через повторы может маркировать транскрипты для контролируемого разрушения. Те же регионы, богатые повторами, привлекают и ферменты редактирования РНК, такие как ADAR1, которые химически модифицируют отдельные основания в двуцепочечной РНК, намекая на то, что низкокомплексные повторы помогают локализовать сайты редактирования, тонко регулирующие поведение РНК.
Обучение нейросети «читать» контакты РНК
Стандартные компьютерные программы пытаются предсказать связывание РНК–РНК главным образом по термодинамической стабильности — сколько энергии потребуется, чтобы образовать или разорвать дуплекс. Хотя это полезно, такие модели часто упускают реальные взаимодействия, наблюдаемые в клетках, особенно между длинными РНК. Чтобы выйти за рамки простых энергетических правил, авторы обучили модель глубокого обучения под названием RIME, которая использует встраивания в стиле «языковой модели»: числовые представления последовательностей РНК, кодирующие паттерны, усвоенные на основе огромных наборов данных нуклеиновых кислот. RIME показывали пары сегментов РНК и обучали классифицировать, взаимодействуют ли они, используя множество реальных спариваний из псорален‑основанных реакций кросслинкинга в качестве положительных примеров и тщательно сконструированные непересекающиеся пары как негативные. 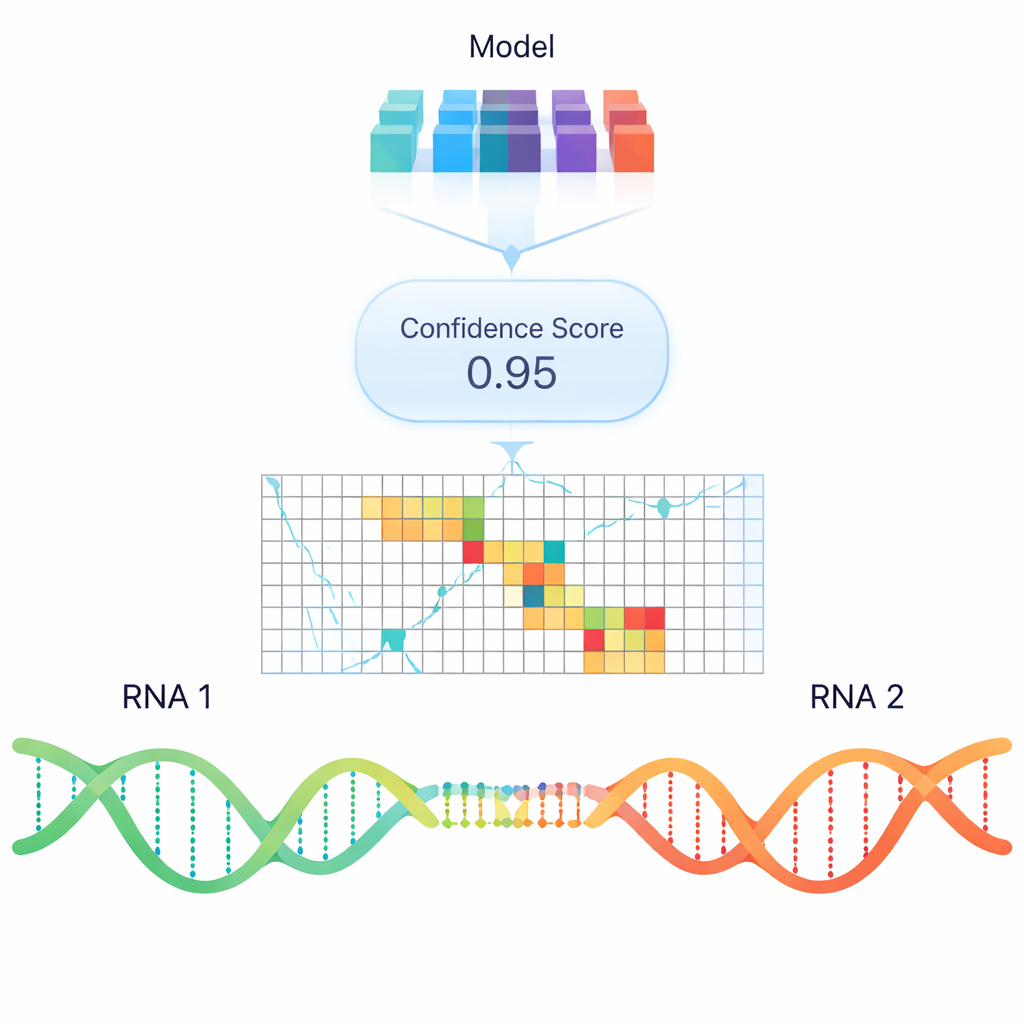
Более умные предсказания и новые биологические подсказки
При сравнительном тестировании с ведущими инструментами, основанными на термодинамике, и другой нейросетевой методикой RIME последовательно показывает лучшие результаты в различении истинных контактов РНК–РНК от подделок, особенно для взаимодействий с высокой доверительной оценкой экспериментальных данных. Модель не только предсказывает, будут ли две РНК спариваться, но и обычно указывает точные регионы, вовлечённые в контакт, и естественным образом усваивает, что низкокомплексные повторы являются сильными предикторами взаимодействия. Примечательно, что та же модель, обученная лишь на взаимодействиях между разными РНК, также хорошо работает для предсказания внутреннего спаривания внутри одной молекулы РНК, согласуясь как со структурными экспериментами, так и с классическими алгоритмами сворачивания. Для некодирующих регуляторов, таких как TINCR, NORAD и SMaRT, RIME успешно заново обнаруживает известные функциональные сайты взаимодействия и предлагает дополнительные кандидаты.
Почему это важно
Для неспециалиста ключевая мысль такова: короткие повторяющиеся участки в РНК — когда‑то легко списываемые как бесполезный шум — действуют как центральные точки соединения в «проводке» РНК клетки. Они помогают сближать РНК, привлекать регуляторные белки и ферменты редактирования и широко используются в путях, контролирующих развитие клеток и ответ на стресс. Новая модель RIME даёт исследователям мощный инструмент для поиска таких РНК–РНК партнёрств в геномах, включая те, которые могут давать сбой при неврологических и других заболеваниях, связанных с расширением повторов. По сути, работа показывает, что понимание и предсказание того, как простые РНК‑повторы «прилипают» друг к другу, может открыть скрытые уровни регуляции генов.
Цитирование: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
Ключевые слова: взаимодействия РНК–РНК, низкокомплексные повторы, длинные некодирующие РНК, глубокое обучение, регуляция генов