Clear Sky Science · ru
Очищение промежуточных альвеолярных эпителиальных клеток, направляемое транскриптомным подписью, улучшает легочный фиброз у мышей
Почему рубцевание лёгких имеет значение
Лёгочный фиброз — серьёзное заболевание, при котором тонкие воздушные мешочки постепенно превращаются в жёсткую рубцовую ткань, и каждый вдох становится тяжёлым трудом. Врачи знают, что это рубцевание начинается, когда нормальные процессы восстановления идут неправильно, но до сих пор было неясно, какие именно клетки виноваты и как удалить их, не повредив здоровую ткань лёгких. В этом исследовании изучается новый способ «считывать» молекулярные сообщения внутри клеток лёгкого, использовать эту информацию, чтобы выявлять вредоносные переходные клетки, и выборочно уничтожать их, чтобы уменьшить рубцевание у мышей.
Клетки, пойманные при неверном восстановлении
После повреждения лёгкого специальные продуцирующие сурфактант клетки типа II обычно размножаются, а затем созревают в тонкие клетки типа I, выстилающие альвеолы и обеспечивающие переход кислорода в кровь. При фиброзе многие из этих клеток застревают в промежуточном, или переходном, состоянии вместо того, чтобы завершить этот путь. Предшествующие исследования с использованием single-cell RNA sequencing обнаружили эти промежуточные клетки у мышей и людей, но было неясно, являются ли они просто свидетелями процесса или ключевыми движущими силами болезни. Авторы сосредоточились на мышином переходном типе, называемом Krt8+ альвеолярными промежуточными клетками дифференцировки, и на их человеческих аналогах — так называемых аберрантных базалоидных клетках, которые встречаются в большом количестве в рубцованных лёгких.
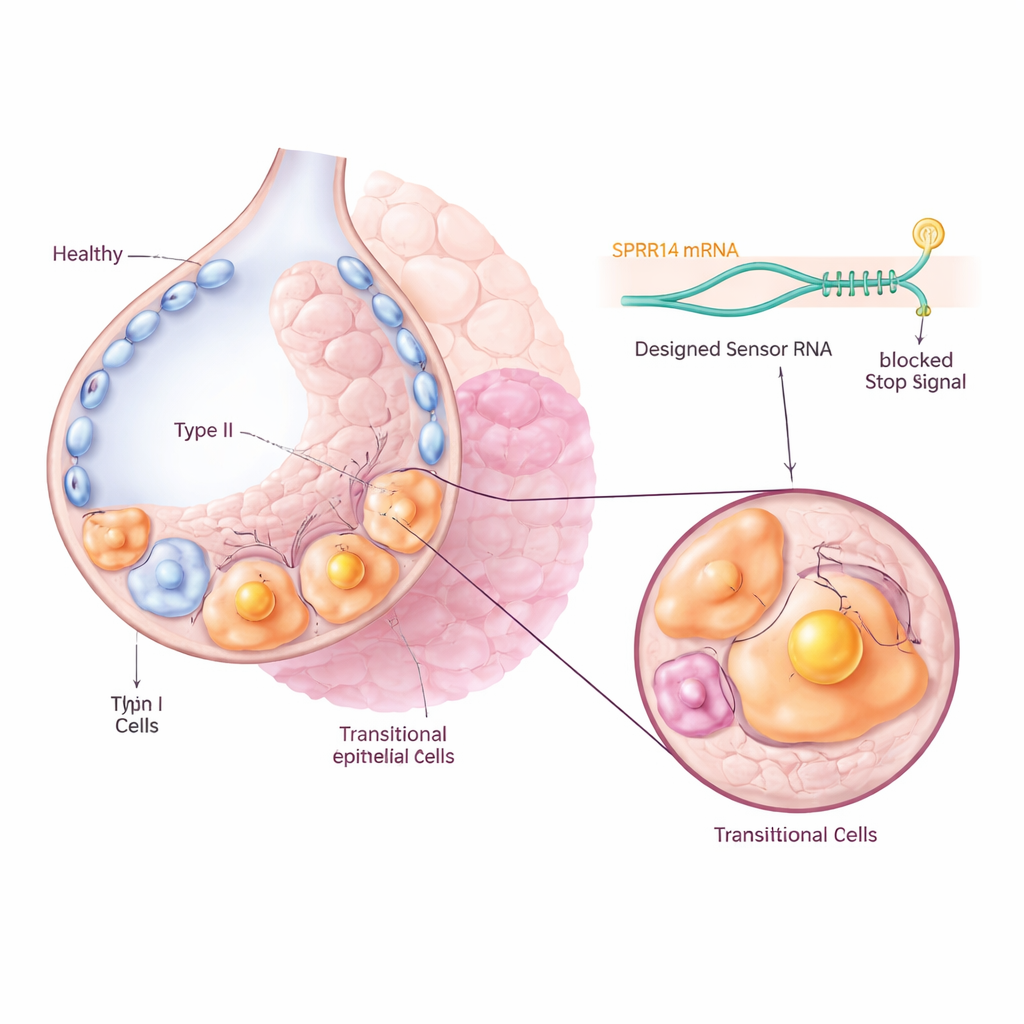
Поиск уникального молекулярного бейджа
Чтобы нацелиться на эти проблемные клетки, не затронув соседние здоровые, команда сначала просеяла большие наборы данных экспрессии генов в поисках маркера, который был бы сильно и специфично включён в переходной популяции. Они выделили молекулу SPRR1A как выдающийся «именной ярлык»: она была значительно обогащена в Krt8+ промежуточных клетках в фибротических лёгких мышей и в KRT5-/KRT17+ аберрантных базалоидных клетках у пациентов с идиопатическим лёгочным фиброзом, но в значительной степени отсутствовала в нормальных клетках лёгкого. Микроскопия как мышечной, так и человеческой ткани лёгкого подтвердила, что SPRR1A проявляется преимущественно в повреждённых, перестроенных областях, а не в здоровых альвеолах, что указывает на её пригодность в качестве точной «ручки» для идентификации виновных клеток.
Программирование клеток с помощью сенсора РНК
Затем исследователи использовали недавно разработанную технологию под названием CellREADR, которая действует как внутренний молекулярный сенсор. Они сконструировали короткие РНК-последовательности, способные комплементарно связываться с РНК SPRR1A внутри клетки. Когда сенсор обнаруживает SPRR1A, он запускает производство присоединённого «эффекторного» белка, например флуоресцентной метки или рецептора, делающего клетку чувствительной к препарату. У мышей вирусы использовали для доставки этих конструкций сенсор–эффектор в клетки лёгкого. Только клетки, активно продуцирующие SPRR1A, включали флуоресцентный сигнал, что позволило команде отслеживать и выделять переходные клетки непосредственно из фибротических лёгких. Сиквенирование одиночных клеток показало, что помеченные клетки в точности соответствовали известной транскрипционной подписи переходных клеток, подтвердив, что РНК-сенсор точно нацелен на нужную популяцию.
Выведение вредоносных промежуточных клеток
Далее эффектор заменили с безвредного флуоресцентного белка на рецептор дифтерийного токсина, чтобы SPRR1A-положительные клетки можно было селективно уничтожить введением дифтерийного токсина. Подбирая время лечения так, чтобы оно совпадало с пиковым числом переходных клеток после химического повреждения лёгкого, авторы смогли удалить примерно треть этой популяции. Такое целенаправленное истощение привело к заметно меньшему рубцеванию лёгких: уменьшилось накопление коллагена, снизились уровни фибротических белков и восстановилась более нормальная структура альвеол. Детальные анализы показали, что большинство SPRR1A-положительных клеток несут признаки стрессового, сходного со старением состояния, с небольшой подгруппой, обладающей высокой пролиферативной способностью, что указывает на то, что эти промежуточные клетки и не в состоянии должным образом восстановить ткань, и одновременно способствуют поддержанию фибротического процесса.
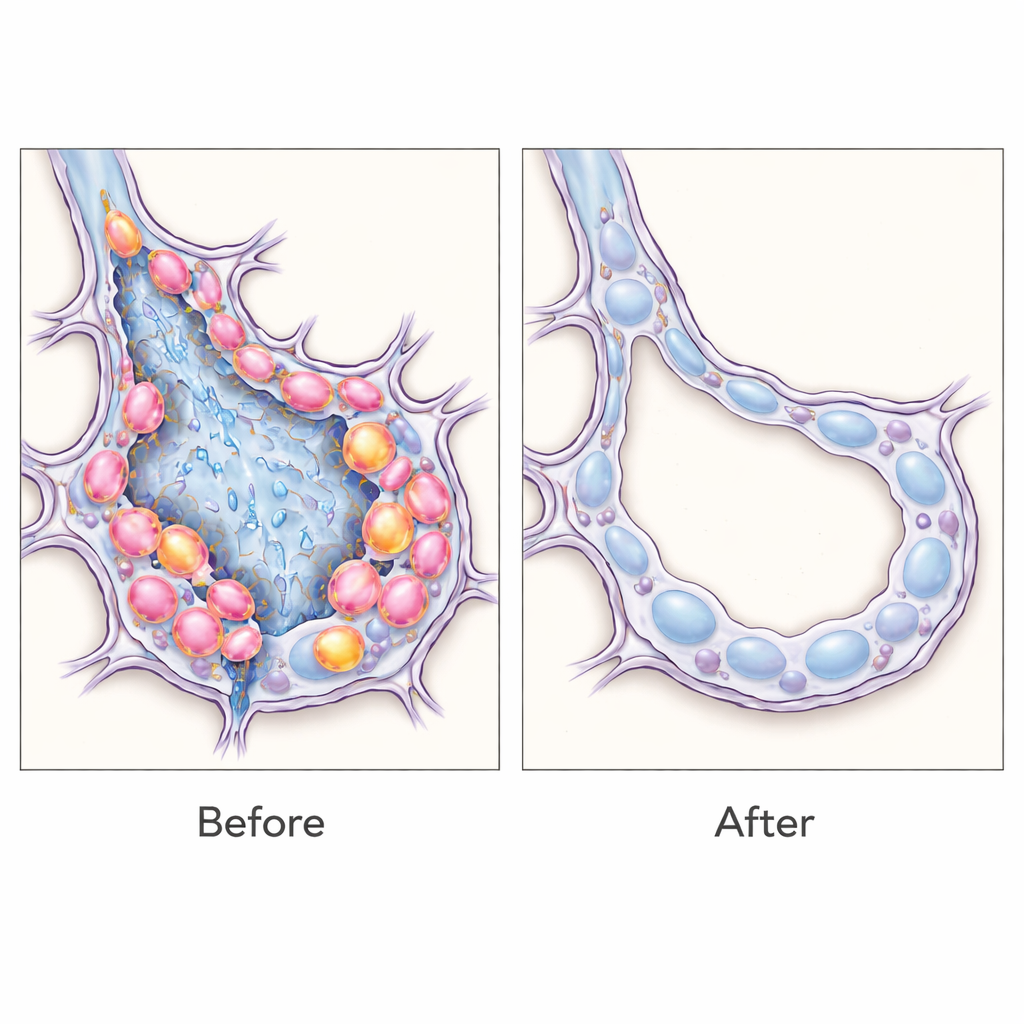
Что это значит для будущих лечений
Эти результаты свидетельствуют о том, что переходные эпителиальные клетки — не просто маркеры, а активные драйверы лёгочного фиброза, и что их селективное удаление может сдвинуть равновесие в сторону более здоровой архитектуры лёгкого у мышей. В более широком смысле работа демонстрирует гибкую стратегию: «считывая» клеточно-специфичные РНК-подписи, исследователи могут помечать, изучать и даже устранять узко определённые популяции клеток в живой ткани без необходимости каждый раз создавать специальные линии животных. Хотя ещё многое предстоит сделать, прежде чем такие инструменты распознавания РНК можно будет безопасно адаптировать для людей, этот подход открывает путь к прецизионным терапиям, нацеленным на те самые типы клеток, которые срывают заживление при хроническом рубцевании лёгких и, возможно, при других фиброзных заболеваниях.
Цитирование: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Ключевые слова: легочный фиброз, альвеолярные эпителиальные клетки, сиквенирование одноядерной РНК (single-cell RNA sequencing), технология распознавания РНК, клеточное старение