Clear Sky Science · ru
Атлас одноядерной ткани центральной миндалины выявляет динамику хроматина и транскрипции генов при алкогольном расстройстве
Почему это исследование важно для повседневной жизни
Алкогольное расстройство (АР) затрагивает миллионы людей и их семьи, но мы по‑прежнему удивительно мало знаем о том, что длительное интенсивное потребление алкоголя делает с человеческим мозгом на уровне отдельных клеток. В этом исследовании внимание сосредоточено на одной небольшой, но ключевой области — центральной миндалине, узле, который участвует в формировании страха, стресса и мотивации — чтобы показать, как алкоголь перестраивает клетки мозга и их генетические регуляторные системы. Сочетая передовые методы «одноядерного» секвенирования с генетическими исследованиями риска зависимости, авторы начинают объяснять, почему некоторые люди более уязвимы к АР и как алкоголь оставляет длительные молекулярные рубцы в мозге.
Внимательный взгляд на крошечный мозговой узел
Центральная миндалина — ключевая структура выходных путей сети эмоций и стресса в мозге и тесно связана с уменьшением тревоги, жаждой и компульсивным употреблением алкоголя. В этой работе исследователи проанализировали около 175 000 отдельных ядер клеток, извлечённых посмертно из центральной миндалины у 50 человек — 22 с историей алкогольного расстройства и 28 без АР. Используя технологию, которая одновременно считывает активность генов (РНК) и доступность хроматина (насколько «открыта» или «закрыта» ДНК) в одной и той же клетке, они создали подробный атлас всех основных типов клеток этой области мозга, включая несколько типов нейронов и поддерживающие клетки, такие как астроциты и микроглия. Они обнаружили, что тормозные (ингибирующие) нейроны — которые ослабляют или формируют активность мозга — особенно многочисленны в центральной миндалине и выглядят особенно затронутыми у людей с АР. 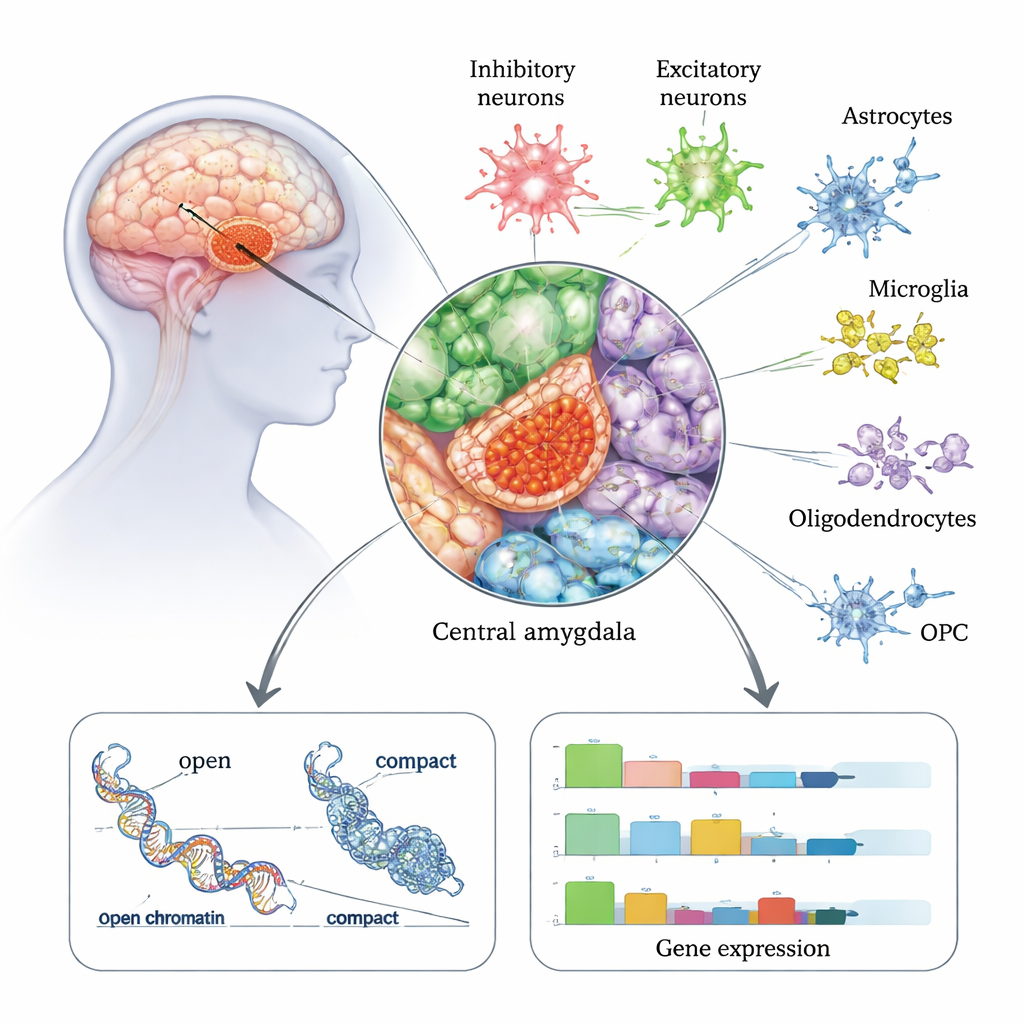
Какие клетки и гены изменяются при алкогольном расстройстве?
Команда систематически сравнила активность генов у людей с АР и без него, по каждому типу клеток. Они обнаружили более 1800 генов, активность которых была изменена в определённых популяциях клеток; самые большие сдвиги происходили в тормозных нейронах, затем — в возбуждающих нейронах и астроцитах. Один подтип ингибирующих нейронов, маркированный пептидом проэнкефалином (PENK), показал особенно сильные изменения. Многие затронутые гены участвуют в коммуникации между клетками мозга, особенно в балансе между возбуждающим сигналом глутаматом и тормозным сигналом ГАМК. Например, ген GABRA2, участвующий в построении одного из основных типов ГАМК‑рецепторов, был повышен в определённых ингибирующих нейронах, тогда как GRM8, глутаматный рецептор, и NCAM1, молекула клеточной адгезии, важная для синапсов, изменялись в противоположных направлениях в разных подтипах нейронов. Эти паттерны указывают на то, что тонкая настройка возбуждения и торможения в центральной миндалине нарушена при АР.
Переключатели контроля мозга: хроматин и регуляторные элементы
Гены не действуют в одиночку; ими управляют участки ДНК, которые функционируют как переключатели и регуляторы яркости. Изучая хроматин — способ упаковки ДНК — исследователи выявили более полумиллиона кандидатных регуляторных элементов и связали их с ближайшими генами в клеточно‑специфичном контексте. Почти половина этих элементов была уникальна для одного типа клеток, что подчеркивает степень специализации различных клеток мозга. Многие регуляторные элементы, изменившиеся при АР, были связаны с генами, вовлечёнными в обработку кальция и сигнализацию через глутамат, такими как CALN1 — ген, связывающий кальций и активно экспрессирующийся в нейронах. В ингибирующих нейронах CALN1 показывал как повышенную экспрессию, так и плотные кластеры регуляторных петель, что подразумевает, что воздействие алкоголя перестраивает локальную архитектуру ДНК, контролирующую этот ген. 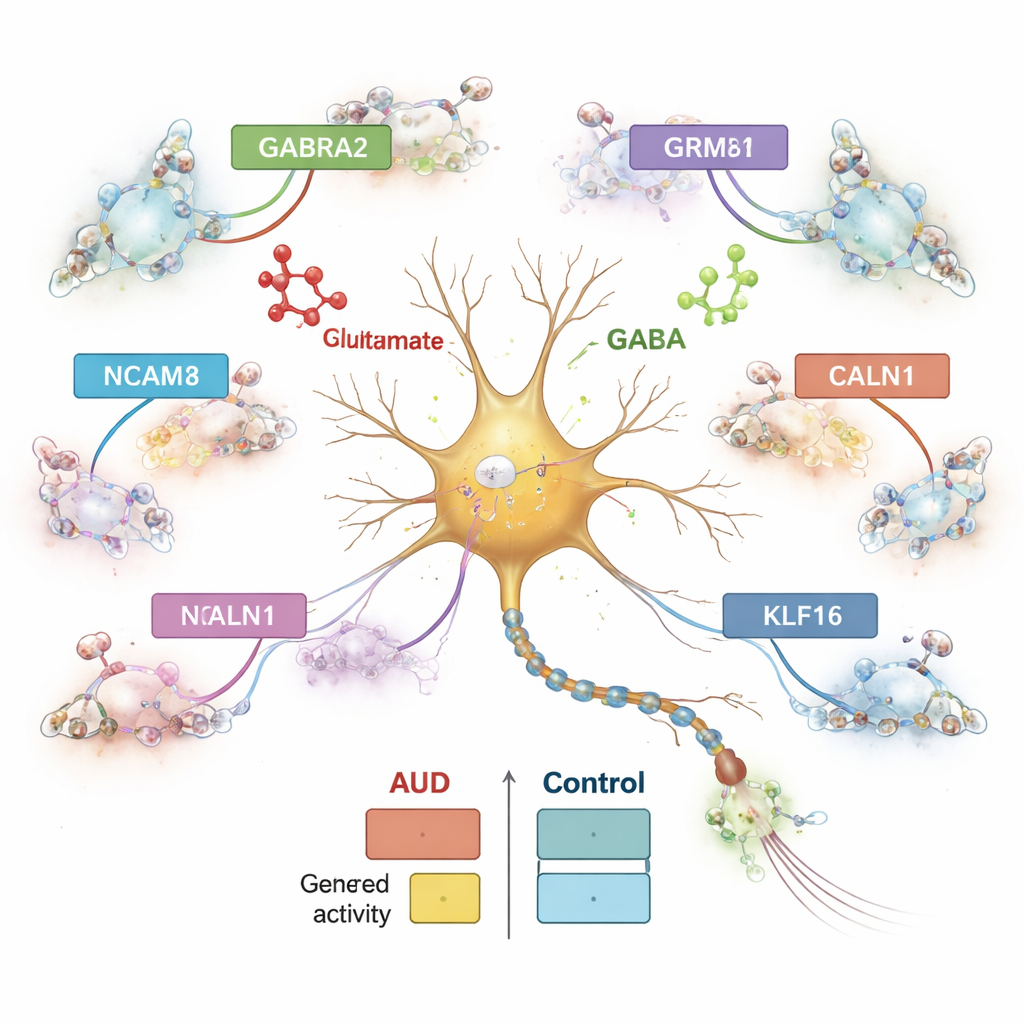
От генов риска к реальным изменениям в мозге
Генетические исследования выявили множество вариантов ДНК, повышающих риск развития проблем с алкоголем, но где именно и как они действуют в мозге оставалось неясно. Наложив свои одноядерные карты на крупные исследования геном‑ассоциированных связей с проблемным употреблением алкоголя, авторы обнаружили, что гены риска непропорционально активны и дисрегулированы в нейронах центральной миндалины, особенно в ингибирующих нейронах. Они выделили более 200 вероятно каузальных вариантов риска, располагавшихся внутри регуляторных элементов, открытых в определённых типах клеток. Некоторые из них находились в или рядом с генами, уже связанными с зависимостью, такими как CACNA1C и DRD2, которые участвуют в контроле возбудимости нейронов и дофаминовой сигнализации. Другие, включая SEMA6D и NF1, выявились как новые кандидаты. Команда также выделила семейство факторов транскрипции Kruppel‑подобных факторов (в частности KLF16), которые, по‑видимому, координируют широкие изменения в генах, связанных с кальцием и глутаматом, и подтвердили части этой регуляторной сети в мышиной модели острого воздействия алкоголя.
Что это значит для понимания и лечения АР
Проще говоря, это исследование показывает, что алкогольное расстройство — это не расплывчатая проблема всего мозга, а высокоорганизованное нарушение, сосредоточенное в отдельных типах клеток и молекулярных путях внутри критического эмоционального узла. Ингибирующие нейроны центральной миндалины, вместе с астроцитами и другими поддерживающими клетками, демонстрируют скоординированные изменения в активности генов и в ДНК‑переключателях, контролирующих эти гены — особенно в системах, управляющих глутаматом, ГАМК и кальцием. Сопоставляя эти клеточные изменения с генетическими вариантами риска, работа предлагает дорожную карту, связывающую унаследованную уязвимость с конкретными молекулярными событиями в мозге. Со временем такие клеточно‑специфичные карты могут помочь разработать более точные методы лечения, восстанавливающие баланс возбуждения и торможения, а не действующие по всему мозгу в целом.
Цитирование: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Ключевые слова: алкогольное расстройство, центральная миндалина, одноядерная геномика, тормозные нейроны, регуляция генов