Clear Sky Science · ru
От образования комплекса TDP-43/RNA до связанной с болезнью агрегации TDP-43: структурный и клеточный подход
Почему этот белок мозга важен
Нейродегенеративные заболевания, такие как боковой амиотрофический склероз (БАС) и фронтотемпоральная деменция, часто сопровождаются скоплениями неправильно свернутых белков внутри нервных клеток. Одним из наиболее частых виновников является белок TDP-43, который в норме участвует в обработке РНК — рабочего копия наших генов. В этом исследовании поставлен ключевой вопрос: что делает TDP-43 в здоровых клетках и что идёт не так, превращая полезного помощника РНК в токсично агрегирующий белок?
Как TDP-43 работает в здоровых нервных клетках
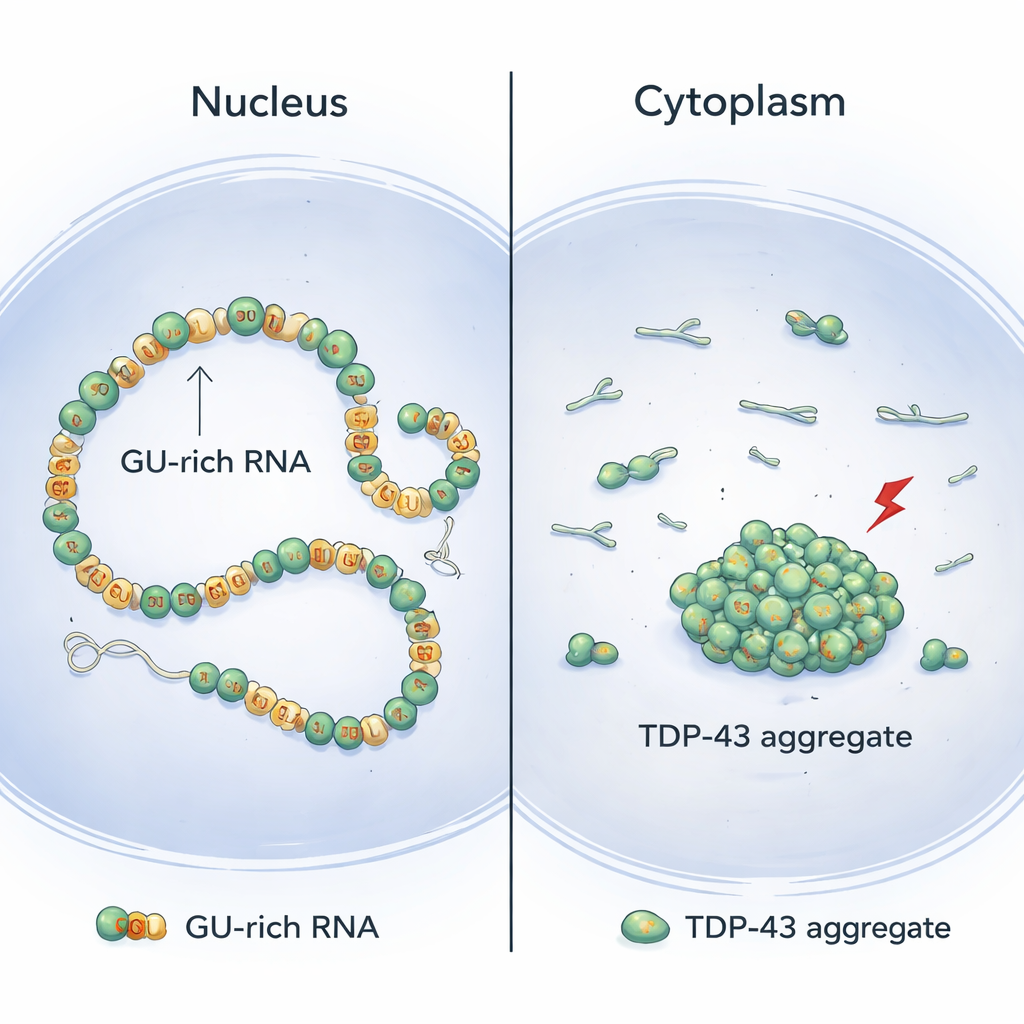
Обычно TDP-43 находится в ядре клетки, где он связывается с длинными участками РНК, богатыми повторами «GU». Авторы, сочетая методы структурной биологии и клеточные эксперименты, показывают, что молекулы TDP-43 выстраиваются кооперативно вдоль этих GU-богатых регионов, образуя гладкие непрерывные цепочки на РНК. При такой организации передний участок белка — N-концевой домен — остаётся физически разнесённым между соседними молекулами. В результате эти N-концевые фрагменты остаются доступными, чтобы тянуться через расстояние и связывать удалённые GU-богатые участки той же молекулы РНК, аккуратно замыкая и уплотняя длинные интроны (некодирующие участки внутри генов) без образования слипшихся агрегатов.
Встроенная внутренняя конкуренция в белке
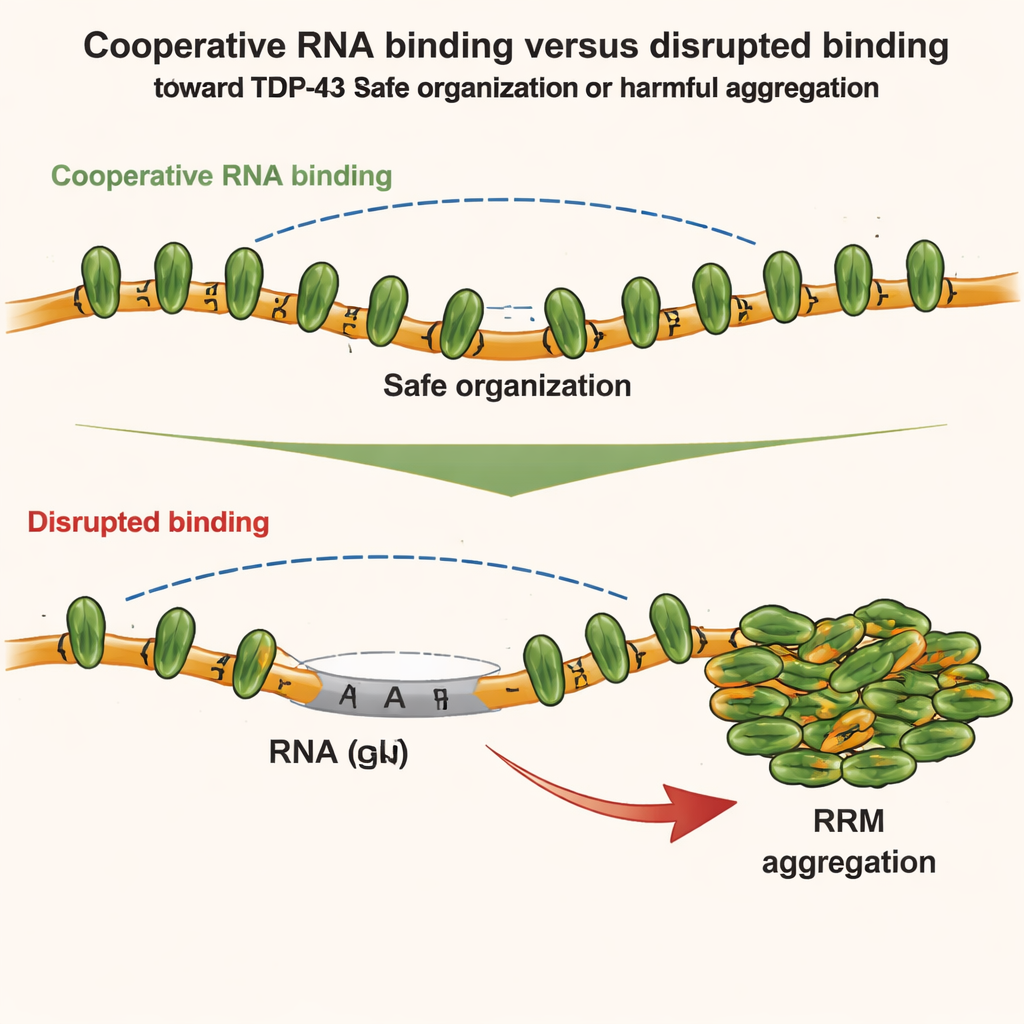
Далее команда изучала, как разные участки TDP-43 конкурируют или сотрудничают между собой. Они сосредоточились на двух регионах: N-концевом домене, который способен сцепляться с другими N-концевыми доменами, и центральных модулях связывания РНК, отвечающих за кооперативное присоединение к GU-богатой РНК. С помощью чувствительных методов, таких как ЯМР-спектроскопия, калориметрия и рассеяние малых углов рентгеновских лучей, исследователи обнаружили, что при кооперативном связывании с РНК геометрия цепочки фактически ослабляет прямые контакты N-концевых доменов соседних молекул. Иными словами, сильное кооперативное связывание с РНК сдерживает локальные N-концевые взаимодействия. Но если эта кооперативность нарушается — например, вставкой участков, не содержащих GU, в РНК или мутациями в TDP-43 — N-концевые участки соседних белков сближаются и могут сцепляться друг с другом.
От полезного уплотнения к вредной слипчивости
Эти структурные наблюдения проверяли в живых клетках. Авторы использовали инженерные клеточные системы, чтобы отслеживать, как разные мутанты TDP-43 смешиваются или разделяются внутри искусственных РНК-богатых компартментов. Они обнаружили, что как кооперативное связывание с РНК, так и N-концевые взаимодействия способствуют организации TDP-43 в высшие структуры, но по-разному. Кооперативное связывание выстраивает белки вдоль GU-богатой РНК, тогда как N-концевые контакты связывают удалённые кластеры вместе. Однако при лёгком окислительном стрессе картина меняется. Химический стрессор (арсенит) вызывает специфические химические модификации — ацетилирование — в центральных мотивах связывания РНК, делая их склонными к сцеплению. Если кооперативное связывание с РНК сохраняется, TDP-43 остаётся в основном растворимым. Если кооперативность ослаблена, N-концевые связи между близко расположенными молекулами TDP-43 выступают как каркас, который сближает ацетилированные ядра, способствуя необратимой агрегации.
Почему TDP-43 сильнее слипается в цитоплазме
Предложенная модель помогает объяснить, почему агрегаты TDP-43 часто обнаруживают в цитоплазме больных нейронов, а не в ядре. В ядре длинные интроны с множеством повторов GU широко распространены, что способствует непрерывному кооперативному связыванию, снижающему риск локальных N-концевых контактов и позволяющему безопасному дальнодействующему замыканию. В цитоплазме, напротив, зрелые РНК содержат гораздо меньше GU-богатых участков. Это делает связывание TDP-43 более пятнистым и менее кооперативным, увеличивая вероятность того, что соседние N-концевые домены вступят во взаимодействие и подготовят почву для агрегации при наступлении стресс-индуцированных химических изменений. В поддержку этой идеи искусственное добавление дополнительных GU-богатых интронов в ядро снижало агрегацию TDP-43 при стрессе.
Что это значит для будущих терапий
Проще говоря, исследование рисует TDP-43 как белок, балансирующий между полезной организацией РНК и вредной слипчивостью, при этом кооперативное связывание с GU-богатой РНК выступает в роли предохранительного механизма. Когда эта страховка даёт сбой — из-за изменённых последовательностей РНК, мутаций белка или клеточного стресса — те же домены, которые обычно уплотняют длинные сегменты РНК, могут вместо этого привести к образованию токсичных агрегатов. Для неспециалистов ключевой вывод в том, что поддержание правильных взаимодействий между TDP-43 и РНК может быть многообещающей стратегией для предотвращения или замедления слипчивости белка, наблюдаемой при БАС и родственных мозговых заболеваниях.
Цитирование: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Ключевые слова: Агрегация TDP-43, Белки, связывающие РНК, БАС (ALS), взаимодействия белок–РНК, нейродегенерация