Clear Sky Science · ru
Атомарно точная модификация лигандов золотых наночастиц посредством межфазного массопереноса
Почему крошечные частицы золота важны для медицины
Медицинская визуализация всё чаще опирается на наночастицы — крошечные частицы, размеры которых в тысячи раз меньше человеческого волоса — чтобы подсвечивать органы и опухоли в глубине тела. В этом исследовании показано, как учёные теперь могут тонко настраивать внешнее покрытие ультрамикроскопичных золотых частиц практически атом за атомом, чтобы один и тот же светящийся сердечник можно было направлять в разные органы, в частности смещая накопление из печени и селезёнки в почки. Такой контроль может помочь проектировать более безопасные контрастные агенты и носители лекарств, которые попадают именно туда, куда нужно врачам, и покидают организм более чисто.
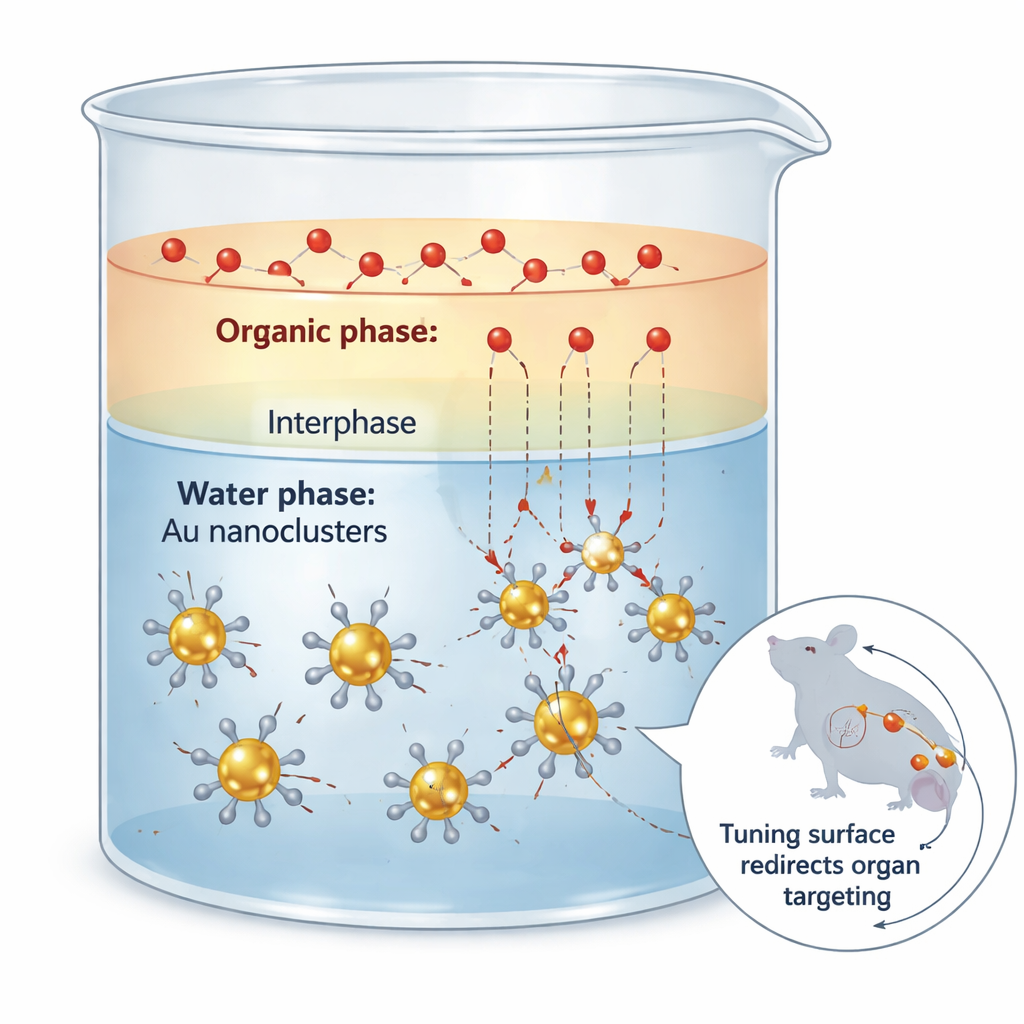
Проблема «одевания» крошечных золотых кластеров
Золотые нанокластеры — это ультрамикроскопичные частицы золота, которые ведут себя скорее как большие молекулы, чем как металлические зерна. Они могут испускать свет в окне ближнего инфракрасного II, который глубоко проникает в ткани и обеспечивает чёткие изображения с низким фоновым сигналом. Однако почти всё в поведении этих кластеров в организме — куда они попадают, как долго циркулируют и как выводятся — зависит не от самого золота, а от органических лигандов, или «оболочки», прикреплённых к их поверхности. Традиционные способы изменения этой оболочки часто похожи на грубую операцию: реакция идёт слишком быстро, покрытие получается неравномерным, а сердечник золота может частично разъедаться, что разрушает структуру и оптические свойства.
Замедляя движение между двумя жидкостями
Исследователи решили эту проблему, воспользовавшись простой физической идеей: сопротивлением массопереносу на границе между двумя несмешивающимися жидкостями. Они поместили золотые кластеры в воду, а поступающие серосодержащие лиганды — в органический растворитель, например этилацетат. В тонкой области, где две жидкости частично смешиваются, лиганды медленно диффундируют к кластерам и обмениваются с исходной оболочкой. Тщательные кинетические измерения показали, что нежелательное «этчингование» золотого сердечника чрезвычайно чувствительно к концентрации лиганда, тогда как желаемый обмен гораздо менее зависим. Используя двухфазную систему для поддержания низкого, но постоянно пополняемого уровня свободных лигандов, команда подавила этчинг примерно в шестьдесят раз, сохранив при этом большую часть полезной скорости обмена.
Создание точного молекулярного набора инструментов
С помощью этого межфазного метода авторы смогли заменить поверхностные лиганды на модельном золотом кластере Au25 в строго контролируемых условиях. Они начали с кластеров, защищённых отрицательно заряженным сульфокислотным лигандом, и заменяли его на ряд новых тиольных лигандов, несущих карбоксильные кислоты, амины, гидроксильные группы, нитрогруппы и гидрофобные ароматические кольца. Масс-спектрометрия показала чистые, чётко определённые смеси, такие как кластеры Au25 с определённым числом каждого типа лиганда, а не широкие, неаккуратные распределения. Метод также работал для других размеров кластеров и семейств лигандов, что указывает на его общую применимость при создании надёжных, специально разработанных золотых нанокластеров для различных задач.
Направляя наночастицы от печени к почкам
Самая впечатляющая проверка точности пришлась на in vivo эксперименты с визуализацией у мышей. Постепенно вводя положительно заряженный лиганд p-аминотиофенол в изначально отрицательно заряженную оболочку, команда создала серию кластеров, общий поверхностный заряд которых смещался от сильно отрицательного к почти цвиттерионному (сбалансированные положительные и отрицательные группы). Во всех вариантах свечения в лабораторных условиях были сопоставимы, но их биораспределение у мышей сильно различалось. Чисто отрицательные кластеры в основном накапливались в печени и селезёнке. По мере добавления положительных лигандов сигнал в этих органах уменьшался, а в почках и мочевом пузыре — увеличивался, что указывает на усиленное почечное выведение. При использовании нейтрального гидроксильного лиганда вместо амина такого смещения не наблюдалось, подчёркивая особую роль положительных зарядов в перенаправлении частиц.
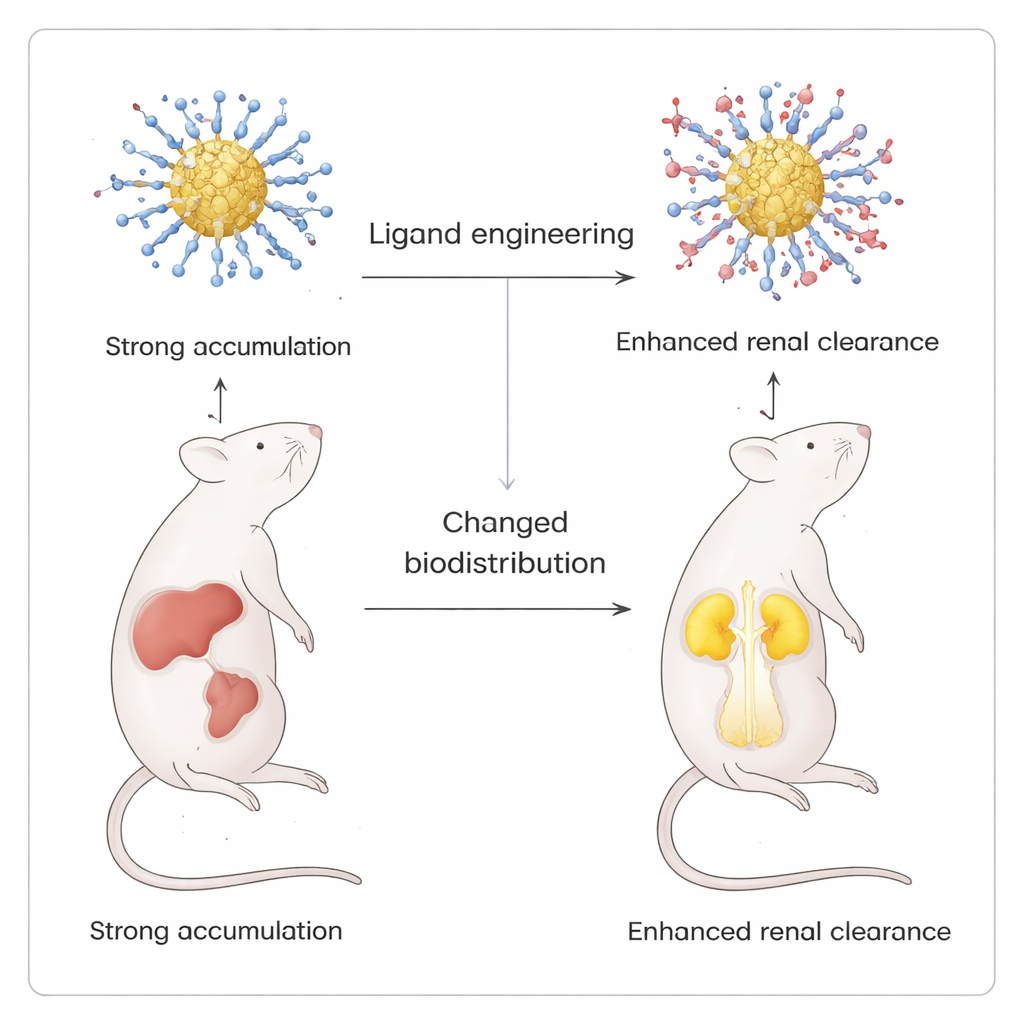
Что это значит для будущих лекарств
Для неспециалистов главное следствие в том, что учёные нашли способ «одевать» светящиеся золотые нанокластеры в молекулярные покрытия, которые можно настраивать почти по одной молекуле за раз, не повреждая при этом саму частицу. Используя мягкую двухжидкостную систему, они контролируют и химию, и конечную судьбу этих частиц в организме. Такой уровень контроля позволяет проектировать контрастные агенты и потенциальные носители лекарств, которые подсвечивают конкретные органы, а затем выводятся через почки, не задерживаясь в печени и селезёнке, что открывает путь к более безопасной и предсказуемой наномедицине.
Цитирование: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Ключевые слова: золотые нанокластеры, модификация лигандов, биоизображение, наномедицина, биораспределение