Clear Sky Science · ru
Интраназальный немодифицированный LcrV усиливает легочный иммунитет, первично вызванный родительскими OMV Yersinia, против пневмонической чумы у мышей
Двухэтапная защита против известного убийцы
Чума звучит как болезнь из средневековой истории, но её легочная форма — пневмоническая чума — всё ещё может быстро убивать и передаваться по воздуху. Антибиотики помогают, однако устойчивые к лекарствам штаммы и угроза преднамеренного использования поддерживают чуму в списках современных угроз. В этом исследовании на мышах рассматривается новая двухэтапная стратегия вакцинации, цель которой — не только вызвать антитела в крови, но и натренировать долгоживущих иммунных «стражей», которые обитают прямо в лёгких и готовы остановить смертельную инфекцию на раннем этапе.
Почему важна защита, ориентированная на лёгкие
Существует две основные формы чумы: бубонная, которая обычно начинается с увеличения лимфатических узлов после укуса блохи, и пневмоническая, которая поражает лёгкие и может быть почти на 100% фатальной, если лечение задерживается даже на сутки. Существующие экспериментальные вакцины в разумной степени защищают от бубонной формы, но с лёгочной формой справляются хуже. Одна из причин — большинство уколов вводят в мышцу и они главным образом тренируют иммунитет в крови, а не на увлажнённых поверхностях дыхательных путей, где начинается пневмоническая чума. Чтобы по‑настоящему защитить лёгкие, учёные всё чаще считают, что вакцины должны засевать «резидентные» иммунные клетки, которые долгосрочно располагаются в ткани лёгких.
Создание более безопасной первичной вакцины
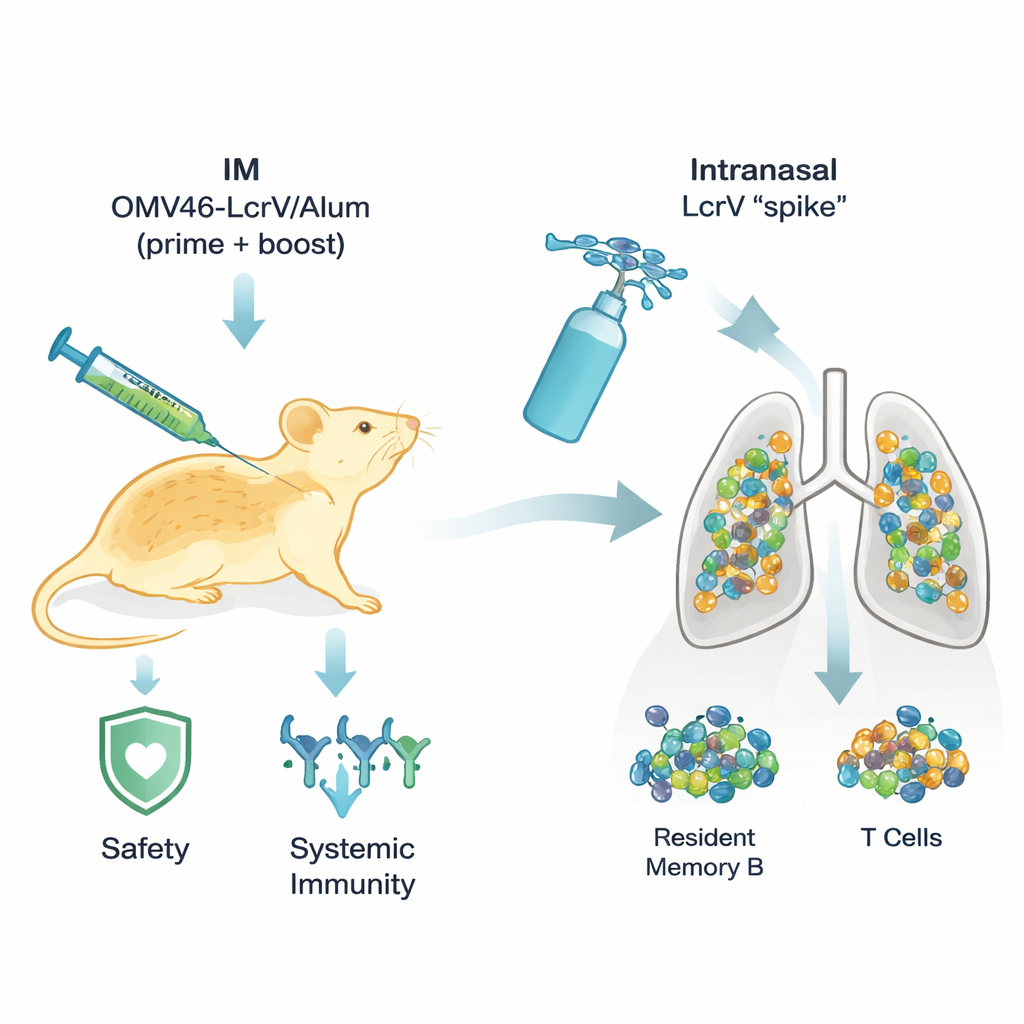
Команда ранее создала перспективную вакцину против чумы на основе внеклеточных мембранных везикул (OMV) от родственника Yersinia, украшенных ключевым белком чумы LcrV. Инъекция OMV46‑LcrV надёжно защищала лёгкие мышей, но вызывала некоторые кратковременные реакции. Чтобы смягчить эти побочные эффекты, исследователи адсорбировали OMV на солях алюминия («алюм»), давно используемом компоненте вакцин, который обычно делает вакцины безопаснее и способствует формированию антител. У мышей эта версия, связанная с алюмом (OMV46‑LcrV/Alum), уже не вызывала потери веса или тревожных сигналов воспаления в крови, но при этом по‑прежнему защищала большинство животных от очень высоких доз чумы. Однако защита немного снизилась при самых больших дозах инфекции, что указывает на то, что безопасность была улучшена ценой небольшой потери эффективности.
Добавление назального «спайка» для усиления защиты лёгких
Чтобы восстановить и даже усилить защиту без введения агрессивных веществ в лёгкие, исследователи заимствовали концепцию, сначала опробованную для COVID‑19: «prime and spike» (прайм и спайк). Мышей сначала праймили и бустировали более безопасными внутримышечными инъекциями OMV46‑LcrV/Alum, а позже им давали небольшую дозу очищенного белка LcrV распылённого в нос, без дополнительного адъюванта. Этот интраназальный «спайк» не нарушал массу тела, показатели крови или структуру лёгких. Тем не менее он полностью изменил иммунитет в дыхательных путях. После назального бустера в жидкости, промывающей лёгкие, обнаруживалось значительно больше специфических к LcrV антител, включая IgA — форму, особенно пригодную для покрытия и защиты слизистых поверхностей. Лёгкие также наполнились резидентными B‑клетками памяти (которые могут быстро превратиться в фабрики по выделению антител), резидентными Т‑клетками памяти и специализированными макрофагами, патрулирующими воздушные пространства. Эти клетки вырабатывали смесь полезных сигнальных белков — таких как интерферон‑γ, IL‑17A и IL‑4 — которые совместно способствовали очищению от бактерий и сбалансированному воспалительному ответу.
Проверка защиты в жестких условиях
Эти иммунные изменения трансформировались в впечатляющую реальную защиту. Мыши, получившие только инъекции OMV с алюмом, выдерживали многие чумные инфекции, но часть из них погибала при самых больших бактериальных нагрузках. Мыши, которые кроме того получили интраназальный LcrV‑спайк, выживали даже при самых экстремальных лёгочных инфекциях, включая штаммы, лишённые основного компонента капсулы, и пожилых животных с перегрузкой железом — состоянием, которое обычно усугубляет инфекции Yersinia. У этих «прайм‑спайк» мышей бактерии практически полностью отсутствовали в лёгких, печени и селезёнке в течение нескольких дней. Когда учёные нейтрализовали ключевые T‑клеточные сигнальные молекулы или блокировали выход лимфоцитов из лимфатических узлов в ткани, защита резко снижалась, что демонстрирует, что резидентные лёгочные клетки, индуцированные схемой, имеют решающее значение. Пересадка этих резидентных B‑ и T‑клеток другим мышам напрямую улучшала их выживаемость, подчёркивая, что именно сами клетки, а не только циркулирующие антитела, обеспечивают дополнительный щит.
Долговременная память лёгких и перспективы
Команда также проверила, сможет ли назальный бустер, введённый спустя многие месяцы после инъекций, вновь пробудить лёгочный иммунитет. Когда интраназальную дозу LcrV отложили примерно на шесть месяцев, она вновь резко усилила антитела и резидентные клетки памяти в лёгких и восстановила полную защиту от тяжёлой пневмонической чумы, тогда как животные, получившие только внутримышечные уколы, были частично незащищены. Это указывает на то, что люди, ранее вакцинированные схожей инъекцией, теоретически могли бы получить простой назальный «топ‑ап» во время вспышки, чтобы быстро обновить защиту лёгких. Хотя эти эксперименты выполнены только на мышах и для клинических испытаний на людях потребуется больше моделей животных, работа указывает на стратегии вакцинации, комбинирующие практичность стандартных инъекций с мощной локальной защитой мукозного иммунитета.
Что это значит для людей
Для неспециалиста главный вывод в том, что то, куда направляет вакцину ваш иммунитет, может быть столь же важно, как и сколько его создаётся. Сначала тренируя иммунную систему безопасной инъекцией, а затем доставляя ключевой белок чумы непосредственно в нос, этот двухэтапный подход учит сами лёгкие запоминать и отражать бактерии чумы. Если похожие стратегии сработают у людей, они могли бы предложить быстрый, долгосрочный способ защиты от пневмонической чумы — и вдохновить новые вакцины, которые лучше защищают наши дыхательные пути от ряда опасных респираторных возбудителей.
Цитирование: Majumder, S., Das, S., Saqib, M. et al. Intranasal unadjuvanted LcrV boosts parental Yersinia OMV primed lung immunity against pneumonic plague in mice. Nat Commun 17, 1624 (2026). https://doi.org/10.1038/s41467-026-68334-2
Ключевые слова: пневмоническая чума, мукозная вакцина, интраназальный бустер, легочный иммунитет, Yersinia pestis