Clear Sky Science · ru
Комьютерное проектирование универсальных циклопрогеназ со стереодивергентной селективностью
Почему крошечные трёхчленные кольца важны для лекарств
Циклопропаны — трёхчленные углеродные кольца — это маленькие, напряжённые строительные блоки, которые могут радикально изменить поведение лекарства в организме. Точная трёхмерная конфигурация атомов (стереохимия) может определить, станет ли молекула полезным препаратом или же неактивным или даже вредным похожим соединением. В этой статье описана вычислительная стратегия проектирования ферментов, которые надёжно синтезируют все четыре возможные трёхмерные формы этих колец из одних и тех же исходных веществ, что открывает путь к более быстрому и чистому исследованию кандидатов в лекарства.
От одного рецепта — к четырём разным результатам
Когда простой двойной атомарный связь (олефин) реагирует с донора карбена, например диазосоединением, результатом может быть циклопропановое кольцо. Но это кольцо может принимать четыре различных стереоизомера, имея те же атомы, но расположенные по‑разному в пространстве. Химикам нужен доступ ко всем этим формам, поскольку они могут по‑разному взаимодействовать с биологическими мишенями и влиять на ключевые свойства лекарств — всасывание, метаболизм и безопасность. Традиционные низкомолекулярные катализаторы иногда обеспечивают такой контроль, но добиться того же с ферментами — природными катализаторами — было сложно, особенно при стремлении одновременно к высокой селективности и широкой терпимости к различным субстратам.
Проектирование ферментов на экране компьютера
Авторы разработали механистически обоснованный многостадийный вычислительный рабочий процесс для решения этой задачи. Сначала они использовали квантово‑химические расчёты для моделирования мимолётных переходных состояний — высокоэнергетических структур вдоль реакционного пути — для образования каждого из четырёх стереоизомеров циклопропана. Эти модели затем поместили в активные центры разных гемсодержащих белков, а программное обеспечение Rosetta для проектирования белков использовали для оценки того, насколько каждый белок стабилизирует или дестабилизирует соответствующее переходное состояние. Существенно, в оценке дизайна учитывались мутации, которые одновременно благоприятствовали желаемому переходному состоянию (позитивный дизайн) и неблагоприятствовали конкурентным вариантам (негативный дизайн), фактически «обучая» фермент предпочитать один 3D‑продукт другим.
Создание полного набора ферментов
С помощью этого подхода команда создала семейство «универсальных» циклопрогеназ. Начиная с миоглобина, они переработали его активный центр, чтобы получить варианты, продуцирующие транc-(1R,2R) циклопропан с очень высокой селективностью и хорошей активностью для более чем 20 разных олефинов, включая требовательные неактивированные и электронно‑бедные субстраты. Ранее созданный вариант миоглобина уже обеспечивал комплементарный транc-(1S,2S) продукт. Чтобы получить два цис‑продукта, авторы обратились к другим гемовым белкам. Они переработали бактериальную P450cam, получив варианты, селективно дающие цис-(1S,2R) продукт, и переориентировали человеческий индоламин‑2,3‑диоксигеназу‑1 (IDO1) — ранее не применявшуюся в карбеновой химии — чтобы она отдавала предпочтение цис-(1R,2S) продукту. В сумме эти четыре биокатализатора могут дать каждый стереоизомер одного и того же набора циклопропанов, часто с контролем до 99% как диастереомеров, так и энантиомеров.
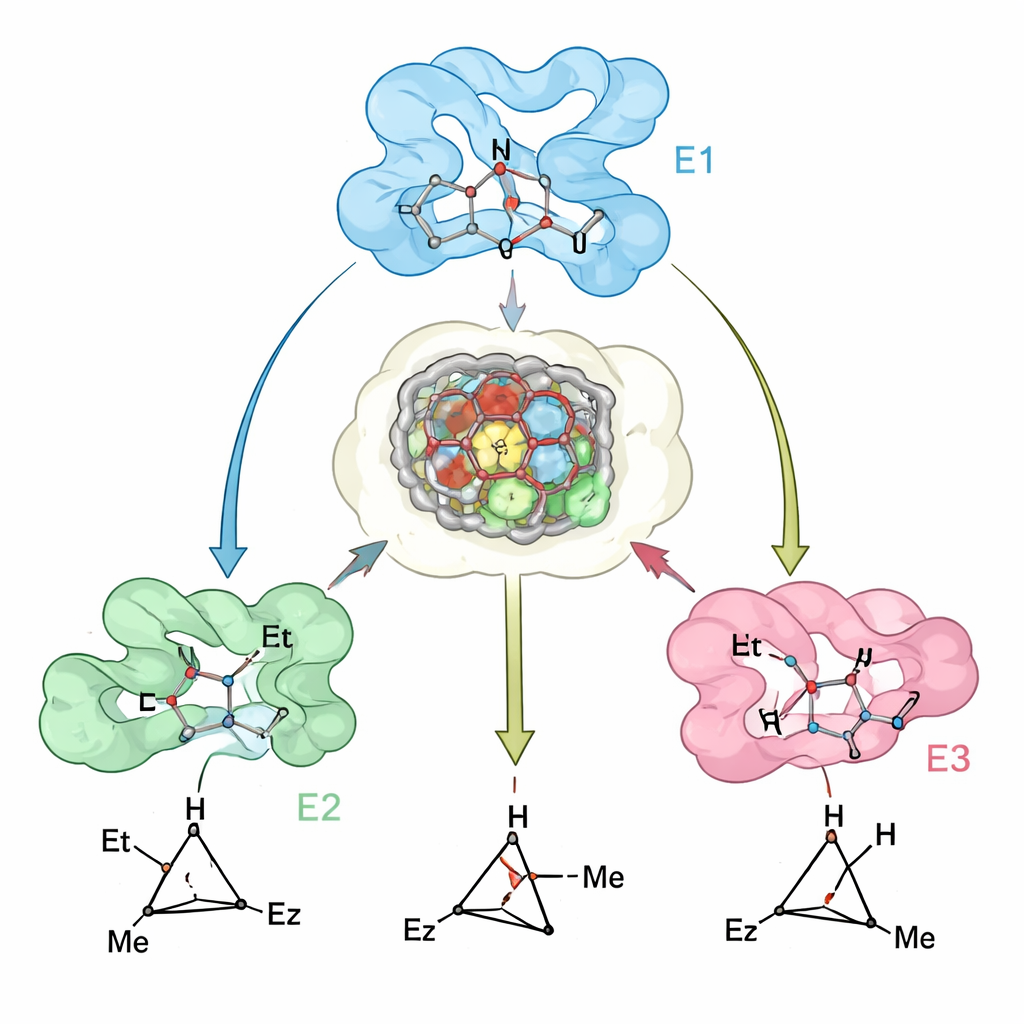
Как совпадает проект и реальность
Чтобы проверить, насколько их вычислительные модели отражают реальные ферменты, исследователи решили кристаллические структуры ключевого варианта миоглобина и сравнили их с предсказанными моделями. Согласование оказалось близким, а экспериментальные данные выявили тонкую, но важную особенность: активный центр белка предорганизован таким образом, чтобы принять предпочитаемое переходное состояние, в то время как небольшие сдвиги в соседних петлях и спиралях делают связывание «неправильного» переходного состояния энергетически невыгодным. В тех случаях, где предсказания были менее точны — например для некоторых громоздких субстратов — расхождения связывали с перемещениями остова, которые не были полностью учтены в моделировании, указывая на очевидные направления для улучшения будущих методов дизайна.
Что это значит для будущих лекарств и катализаторов
Комбинируя физически обоснованное моделирование переходных состояний с продуманным редизайном белков, эта работа демонстрирует, что стереохимические исходы ферментативных реакций можно запрограммировать заранее, а не открывать лишь методом проб и ошибок эволюции. Полученный набор циклопрогеназ даёт химикам практичный способ синтезировать полные наборы стереоизомеров циклопропанов из широкого круга исходных олефинов, существенно упрощая исследования «структура–активность» в открытии лекарств и синтезе природных продуктов. Ту же стратегию можно адаптировать к другим типам ферментов и классам реакций, ускоряя создание биокатализаторов, обеспечивающих точный 3D‑контроль над сложными молекулами.
Цитирование: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Ключевые слова: биокатализ, циклопротанирование, проектирование ферментов, стереохимия, гемовые белки