Clear Sky Science · ru
Глицерол-3-фосфат-ацилтрансфераза усиливает токсичность, вызванную α‑синуклеином, увеличивая перекисное окисление липидов
Почему жиры в мозге важны при болезни Паркинсона
Болезнь Паркинсона обычно описывают как проблему с белком под названием альфа‑синуклеин, который слипается и повреждает нервные клетки, контролирующие движение. Это исследование показывает, что мозговые липиды — особенно то, как они синтезируются и повреждаются — играют удивительно важную роль в том, насколько токсичен альфа‑синуклеин. Выявив фермент синтеза липидов, который усугубляет повреждение нейронов, работа указывает на новый, лекарственно пригодный путь, который может дополнять существующие усилия по борьбе с корневыми причинами болезни Паркинсона.
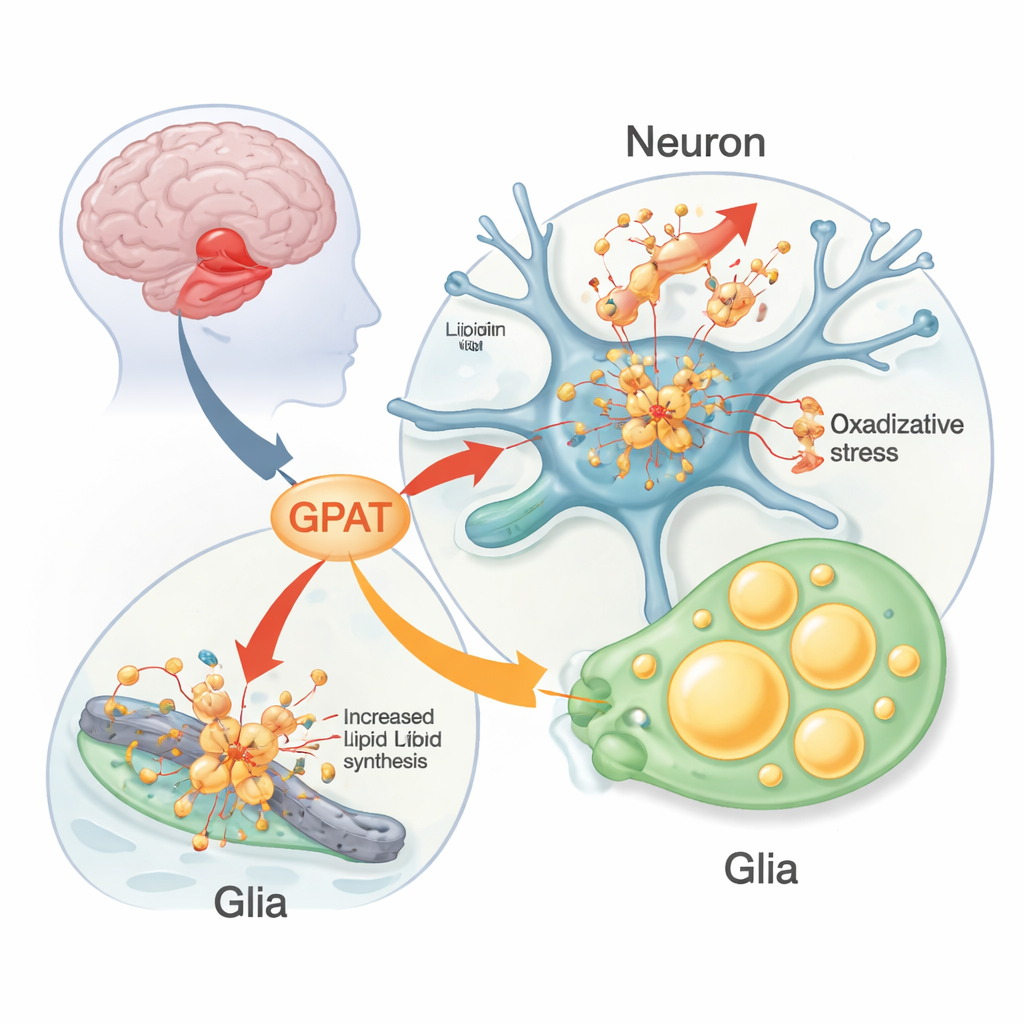
Белок, который ведёт себя неправильно при болезни Паркинсона
У людей с болезнью Паркинсона постепенно гибнут допаминэргические нейроны в глубокой области мозга, координирующей движение. Внутри этих умирающих клеток учёные часто обнаруживают плотные отложения, называемые тельцами Леви, насыщенные белком альфа‑синуклеином. В редких семьях мутации или дополнительные копии гена альфа‑синуклеина прямо вызывают Паркинсон, но распространённые генетические варианты этого гена лишь умеренно повышают риск. Это указывает на то, что другие гены и пути модифицируют вредоносность альфа‑синуклеина. Растущее число данных связывает липиды — жиры и подобные им молекулы, которые формируют клеточные мембраны и запасы энергии — с кластеризацией альфа‑синуклеина и гибелью нейронов.
Поиск мощного липидного фермента на моделях плодовой мухи
Исследователи использовали плодовых мух, генетически модифицированных для экспрессии человеческого альфа‑синуклеина в нервной системе, как живую испытательную модель. Такие мухи развивают симптомы, похожие на Паркинсон: потерю допаминэргических нейронов, трудности при забегании по стенке и нарушение суточных ритмов активности. Команда систематически модифицировала версии у мух генов риска Паркинсона человека, чтобы посмотреть, какие из них меняют влияние альфа‑синуклеина. Выделился один ген: mino, кодирующий митохондриальную форму фермента глицерол‑3‑фосфат‑ацилтрансферазы (GPAT). GPAT стоит на входе в путь синтеза фосфолипидов и триглицеридов — липидов, формирующих мембраны и жировые капли. Снижение активности mino в нейронах позволило мухам с альфа‑синуклеином сохранить больше допаминовых нейронов и дольше лучше двигаться; усиление выражения mino давало противоположный, вредный эффект.
Повреждённые липиды, стресс митохондрий и жировые капли в глии
Углублённый анализ показал, что GPAT влиял на накопление окислительных повреждений в липидах мозга. У мух с альфа‑синуклеином, содержащихся при повышенной температуре (что усугубляет проявления болезни), перекисное окисление липидов — химическое «ржавление» жиров — повышалось в мембранах мозга. Снижение активности mino уменьшало это повреждение, а его сверхэкспрессия увеличивала; без альфа‑синуклеина изменение mino почти не влияло на ситуацию. Маркёры клеточной гибели в зрительной области мозга повторяли этот паттерн. Команда также наблюдала заметное накопление липидных капель — крошечных сфер хранения жира — не в самих нейронах, а в соседних глиальных клетках. Эти капли увеличивались с возрастом у мух с альфа‑синуклеином и изменялись под влиянием ферментов, строящих или расщепляющих триглицериды, подчёркивая активное метаболическое сотрудничество между нейронами и глией при стрессе.
Метаболическая перенастройка и агрегация альфа‑синуклеина
Измерения метаболитов в мозге мух показали, что экспрессия альфа‑синуклеина связана с «узким местом» в цикле производства энергии клетки: цитрат и изоцитрат, два промежуточных продукта трикарбонового (TCA) цикла, значительно накапливались, тогда как последующие шаги смещались менее выраженно. Уровни лактата также росли, что согласуется с усиленной гликолизой. Одновременно детальный липидный профиль выявил изменения в соотношении фосфолипидов мембран и в составе их жирных кислот, сдвигаясь в сторону видов более подверженных окислительному повреждению. Когда команда снижала активность нескольких ферментов GPAT — митохондриального mino и родственных ферментов на эндоплазматическом ретикулуме — альфа‑синуклеин по‑прежнему накапливался, но его склонность образовывать высшие олигомеры (многобелковые комплексы) уменьшалась, а митохондрии демонстрировали меньше признаков реактивного оксидативного стресса и «старения».
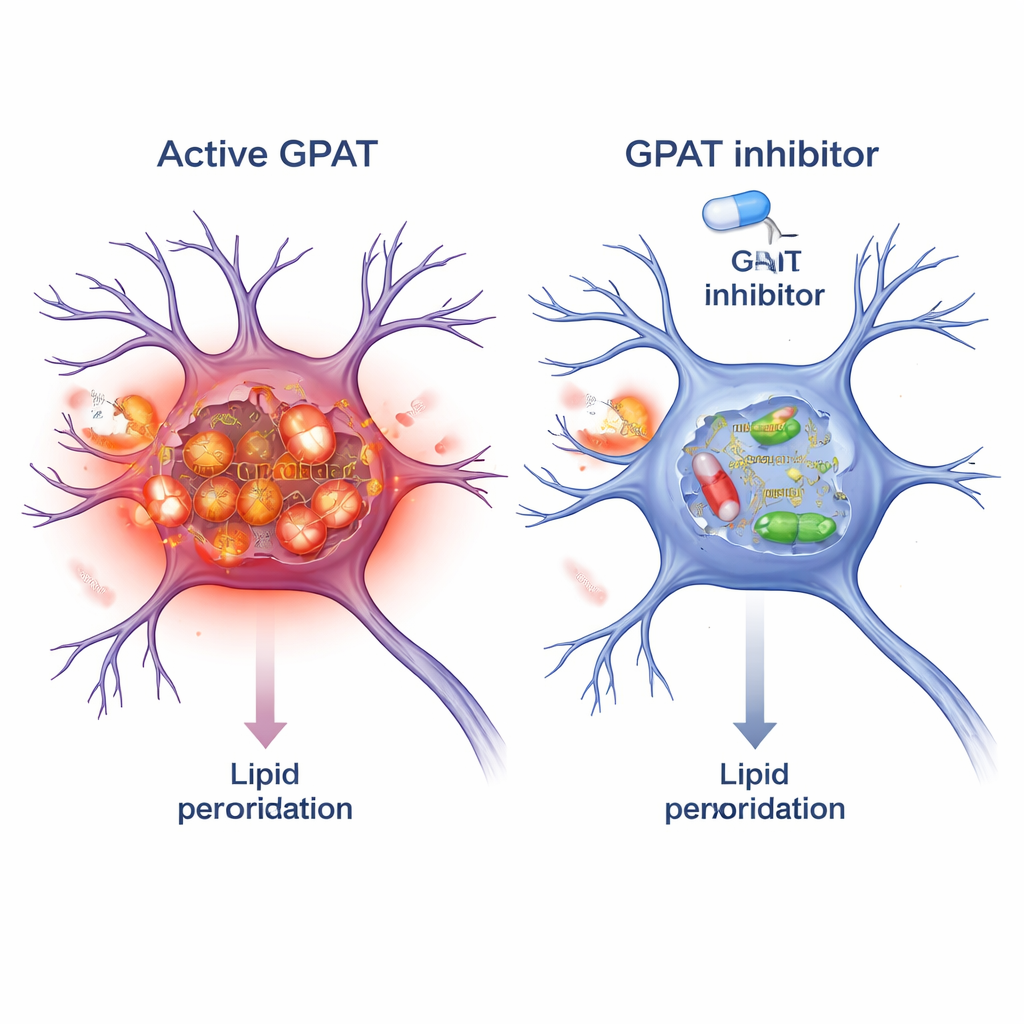
Блокирование GPAT как защитная стратегия
Поскольку GPAT — фермент, его можно нацелить малыми молекулами. Исследователи испытали FSG67, известный ингибитор GPAT, первоначально разработанный для лечения ожирения и диабета. У мух с альфа‑синуклеином добавление FSG67 в пищу воспроизводило преимущества генетического снижения активности GPAT: улучшалась подвижность, лучше сохранялись допаминовые нейроны, уменьшалось количество вредных олигомеров альфа‑синуклеина и снижался митохондриальный окислительный стресс. Чтобы проверить применимость концепции к млекопитающим, они обработали культуру нейронов мышиного мозга предформированными фибриллами альфа‑синуклеина, которые инициируют образование токсичных агрегатов. Одновременная обработка FSG67 снизила накопление фосфорилированного альфа‑синуклеина и уменьшила несколько независимых маркёров перекисного окисления липидов в этих нейронах.
Что это означает для людей с болезнью Паркинсона
Проще говоря, эта работа показывает, что то, как мозг обращается с липидами, может усилить или ослабить токсичность альфа‑синуклеина. При высокой активности GPAT встраиваются в мембраны и запасные капли более уязвимые липиды, которые легче окисляются; такая среда повреждённых жиров, по‑видимому, способствует образованию вредных форм альфа‑синуклеина и нагружает митохондрии — энергетические станции клетки. Снижение активности GPAT — генетически или с помощью препарата — смещает баланс в сторону меньшего «ржавления» липидов, меньшего числа токсичных белковых комплексов и более здоровых нейронов. Хотя эти выводы пока предварительны и получены на мухах и культивируемых нейронах мыши, они выделяют метаболизм липидов, и GPAT в частности, как перспективную новую точку приложения для терапии болезни Паркинсона, дополняющую стратегии, направленные непосредственно на альфа‑синуклеин.
Цитирование: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Ключевые слова: Болезнь Паркинсона, альфа‑синуклеин, перекисное окисление липидов, ингибитор GPAT, нейродегенерация