Clear Sky Science · ru
Структура комплекса SHOC2–KRAS–PP1C раскрывает изоформо-специфические детерминанты RAS и даёт представление о нацеливании сборки комплекса ингибиторами RAS
Как клетки решают, когда расти
Клетки опираются на внутреннюю сеть сигналов, чтобы решать, когда расти, делиться или оставаться в спокойном состоянии. В центре этой системы находятся белки RAS — крошечные молекулярные переключатели, которые часто выходят из строя при раке. В этом исследовании подробно рассматривается, как определённая группа белков — SHOC2, RAS и PP1C — объединяются, чтобы переключить ключевой сигнал роста, и как современные противораковые препараты можно настроить, чтобы эффективнее блокировать этот процесс и мешать опухолям обходить лечение.
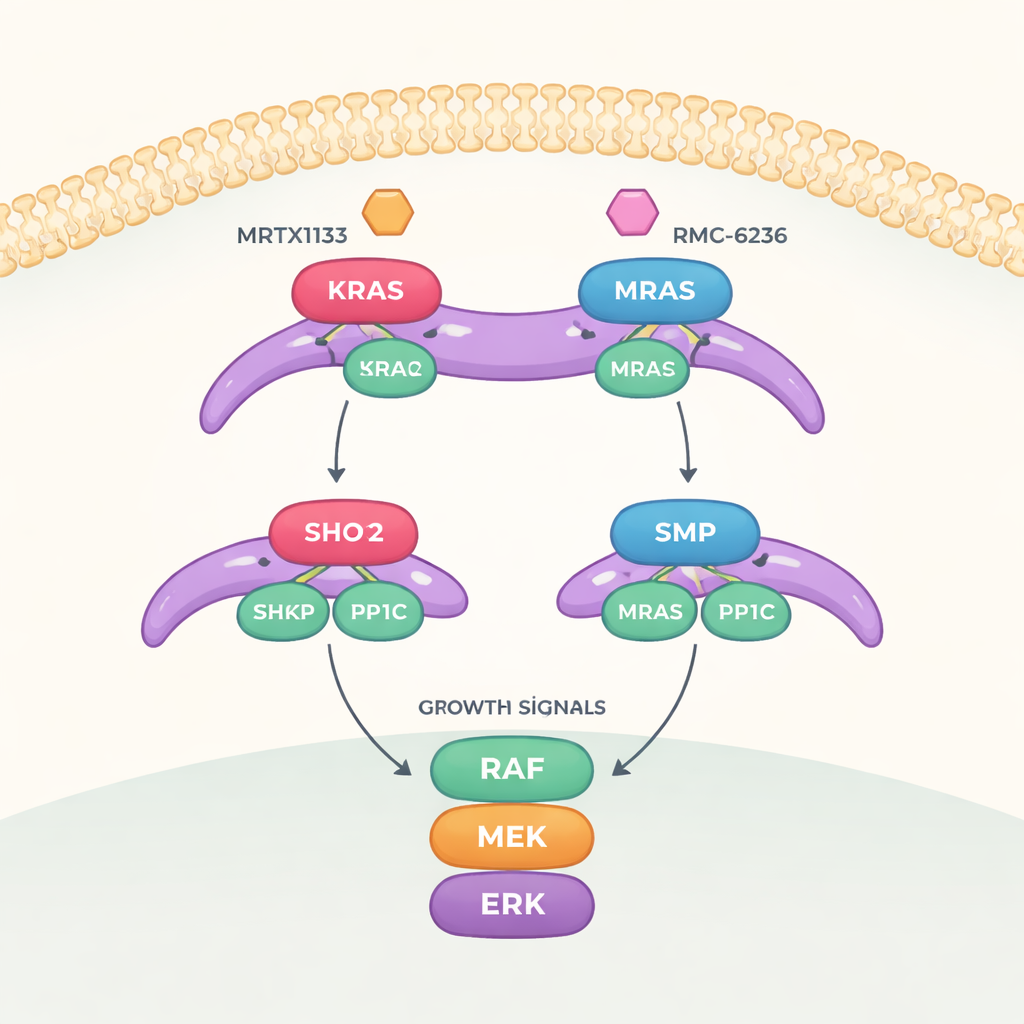
Переключатель роста из трёх критических частей
Работа сосредоточена на сигнальном пути, называемом MAPK, который передаёт сигналы о росте от поверхности клетки к ядру. Чтобы этот путь полностью активировался, белок RAF должен быть переключён из «выключенного» состояния в «включенное». Этот переключатель контролируется трёхкомпонентным комплексом, состоящим из SHOC2 (каркаса, удерживающего компоненты вместе), PP1C (фермента, снимающего фосфатную метку) и активного белка RAS. При сборке этот трио удаляет определённую фосфатную метку с RAF, позволяя ему активировать каскад роста далее по цепочке.
Почему партнёр с более низким сродством всё ещё важен при раке
Существует несколько типов белков RAS. MRAS образует очень прочный комплекс с SHOC2 и PP1C, тогда как более известные онкогенные формы KRAS, HRAS и NRAS формируют менее стабильные варианты того же комплекса. Удивительно, но раковые клетки, управляемые мутантными KRAS, HRAS или NRAS, оказываются сильно зависимыми от SHOC2, несмотря на то, что их комплексы менее устойчивы. Большие генетические скрининговые наборы данных показывают, что многие опухоли с определёнными мутациями RAS — особенно в ключевых положениях, таких как Q61 и G13 — крайне чувствительны к утрате SHOC2, то есть сборка этого комплекса критична для их выживания.
Раскрытие формы комплекса с KRAS
До сих пор учёные видели детальную структуру только прочного комплекса на базе MRAS. Менее стабильная версия с KRAS распадалась слишком легко, чтобы её можно было зафиксировать. В этом исследовании авторы использовали связанные с болезнью мутации, которые слегка укрепляют контакты между компонентами, чтобы стабилизировать комплекс SHOC2–KRAS–PP1C достаточно долго для визуализации методом криоэлектронной микроскопии. Они обнаружили, что общая архитектура близка к комплексу с MRAS, но KRAS лишён нескольких мелких структурных элементов, которыми MRAS пользуется для более прочного захвата SHOC2 и PP1C. В результате комплекс с KRAS имеет меньшую контактную поверхность и образует меньше связей, что объясняет его изначально меньшую устойчивость, хотя он остаётся важным в опухолях с гиперактивным KRAS.
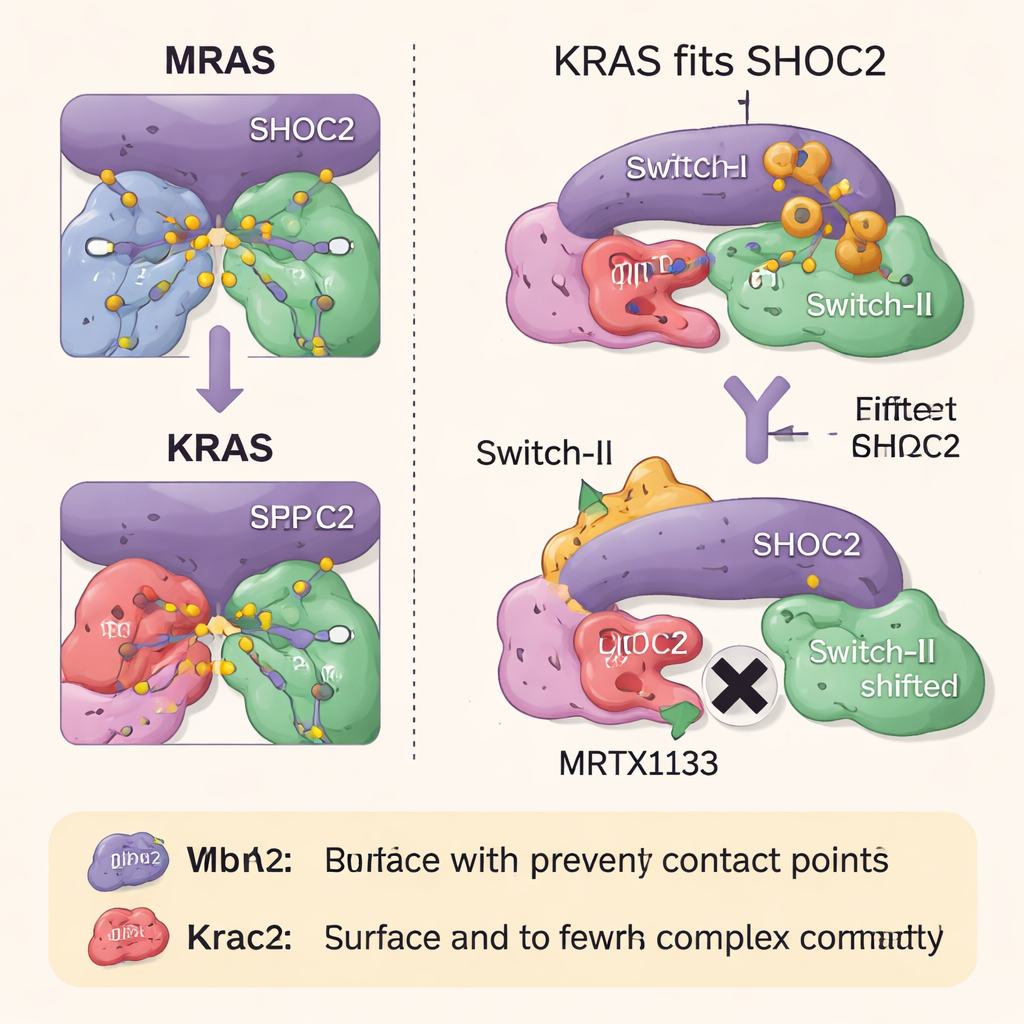
Как препараты против RAS блокируют сборку комплекса
Далее команда изучила, как два класса препаратов, нацеленных на RAS, влияют на этот трёхкомпонентный комплекс. MRTX1133, разработанный для связывания с карманом рядом с гибкой областью KRAS, известной как Switch-II, фиксирует эту область в конформации, которая конфликтует с поверхностью SHOC2. Это сильно препятствует образованию новых комплексов SHOC2–KRAS–PP1C, хотя менее эффективно разрушает уже существующие. Второй препарат, RMC-6236, действует совместно с вспомогательным белком (циклофилин A) и также блокирует те же поверхности KRAS, необходимые для связывания с SHOC2. Ни один из этих препаратов, однако, естественно не связывается с MRAS, поэтому высокосродный комплекс с MRAS остаётся нетронутым и может способствовать повторной активации пути роста, когда KRAS ингибирован.
Крайняя цель — двойное нацеливание, чтобы предотвратить сопротивление
Чтобы проверить возможность двойного нацеливания, исследователи сконструировали версию MRAS, у которой карман Switch-II был изменён так, что MRTX1133 теперь мог связываться. Этот мутант по-прежнему формировал прочный комплекс с SHOC2 и PP1C, но препарат теперь блокировал его сборку и снижал способность активировать RAF в пробирочных тестах. Вкупе с данными о соединениях, связывающихся с SHOC2, эти результаты показывают, что реалистично разработать лекарства, которые одновременно выключают как комплексы на базе KRAS, так и комплексы на базе MRAS. Для неспециалиста главный вывод таков: раковые клетки используют несколько тесно родственных переключателей, чтобы поддерживать поток сигналов роста, особенно когда один переключатель заблокирован лекарством. Понимая точные формы и контакты внутри этих белковых сборок, исследователи теперь могут планировать терапии, которые одновременно атакуют оба резервных пути, затрудняя адаптацию и возникновение сопротивления у RAS-опосредованных опухолей.
Цитирование: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Ключевые слова: Сигнализация RAS, Ингибиторы KRAS, Путь MAPK, Белковые комплексы, Устойчивость к лекарствам