Clear Sky Science · ru
Обратимое липид‑опосредованное pH‑управление каналами коннексин‑46/50 при помощи крио‑ЭМ
Почему микроканалы клеток важны для здоровья и болезни
Каждую секунду наши клетки обмениваются электрическими сигналами и малыми молекулами через микроскопические туннели, называемые щелевыми контактами. Эти каналы помогают сердцу биться согласованно, мозгу удалять токсичные продукты обмена и сохранять прозрачность хрусталика глаза. Когда внутренность клеток становится более кислой, как это случается при инсульте, инфаркте или при развитии катаракты, многие такие каналы закрываются — но то, как они чувствуют и реагируют на кислотность, долго оставалось загадкой. В этой работе использована крио‑электронная микроскопия с высоким разрешением, чтобы почти атом за атомом показать, как специфические каналы в хрусталике закрываются в ответ на кислотность и как этот процесс полностью обратим.
Клеточные туннели, которые синхронизируют ткани
Щелевые контакты состоят из белков, называемых коннексинами, которые собираются в кольцеобразные каналы, пересекающие мембраны двух соседних клеток. В работе изучается пара близкородственных коннексинов — коннексин‑46 и коннексин‑50 — образующих каналы в хрусталике глаза. Эти каналы позволяют ионам и мелким молекулам напрямую течь между клетками, способствуя поддержанию прозрачности хрусталика и общего здоровья ткани. Однако при стрессовых состояниях те же каналы могут стать путями для вредных сигналов. Чтобы защитить ткани, щелевые контакты закрываются, когда внутренняя среда клетки становится более кислой. Понимание тонкомасштабного механизма этого «pH‑управления» важно для выяснения того, как ткани переживают стресс и почему некоторые мутации приводят к таким заболеваниям, как катаракта.
Наблюдая движение каналов с помощью крио‑ЭМ
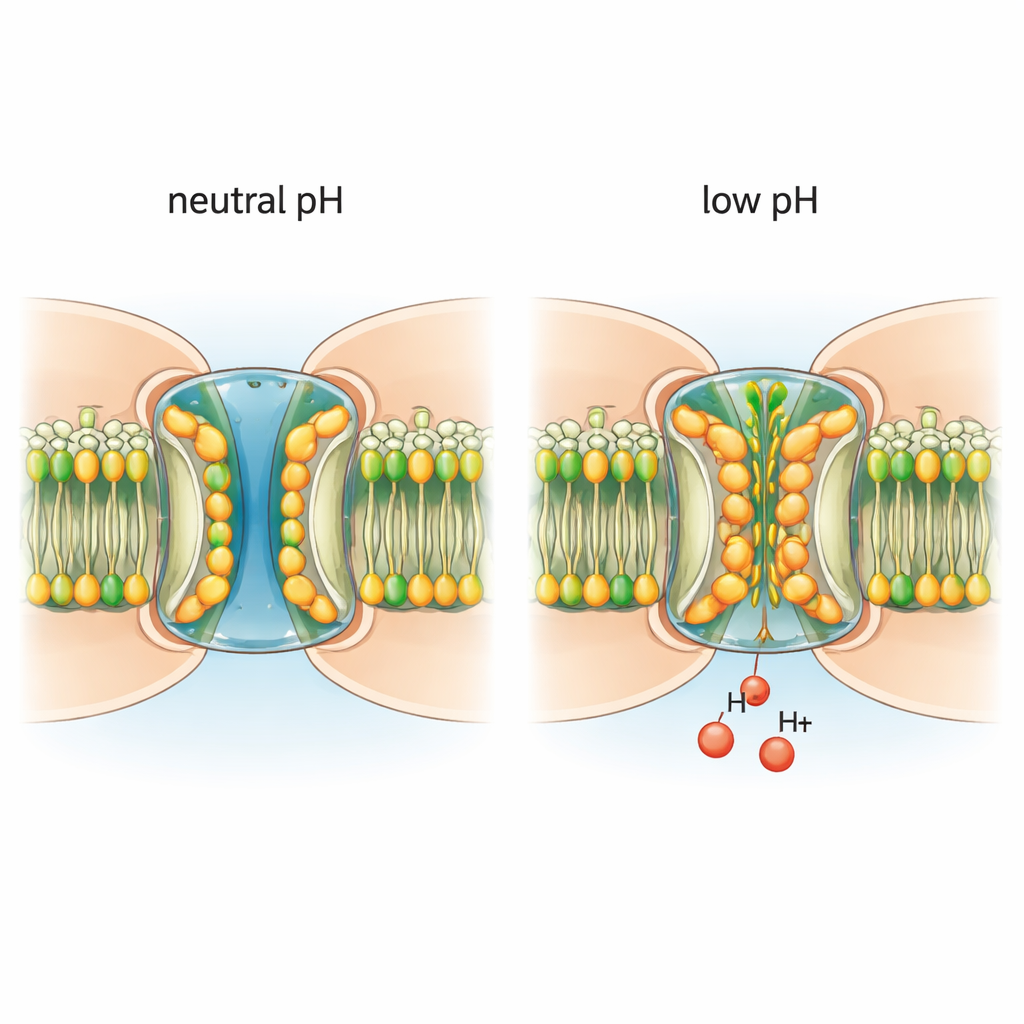
Исследователи очистили нативные каналы коннексин‑46/50 из старых овечьих хрусталиков и встроили их в модельную мембрану. С помощью крио‑электронной микроскопии они получили изображения каналов с почти атомным разрешением в нейтральных условиях, которые способствуют открытому состоянию, и в слабо кислой среде, которая вызывает закрывание. При нейтральном pH каналы в основном принимают устойчивое открытое состояние: центральный туннель достаточно широк для ионов и мелких молекул, а гибкий сегмент — N‑концевой домен — выстилает вход в пору. В этих условиях пора чистая: никаких посторонних молекул, блокирующих проход, и окружающие мембранные липиды остаются организованными в регулярные слои.
Кислота втягивает липиды в пору
Когда среду сделали слабо кислотной, архитектура канала изменилась поразительным образом. Липидные молекулы из окружающей мембраны втянулись в пору, просачиваясь между N‑концевыми сегментами и под ними. Эти вторгшиеся липиды образуют двухслойную гидрофобную «прокладку», которая подталкивает N‑концевые домены внутрь, сужая канал и способствуя блокировке прохода. Дополнительные липиды вжавались между соседними субъединицами белка на их интерфейсах, по-видимому служа путями входа из мембраны в пору. Важно, что при помещении каналов в детергентную среду, лишённую полноценной липидной мембраны, низкий pH больше не индуцировал этих структурных изменений. Это демонстрирует, что настоящие липиды — не просто наблюдатели: они являются необходимыми партнёрами в процессе pH‑управления.
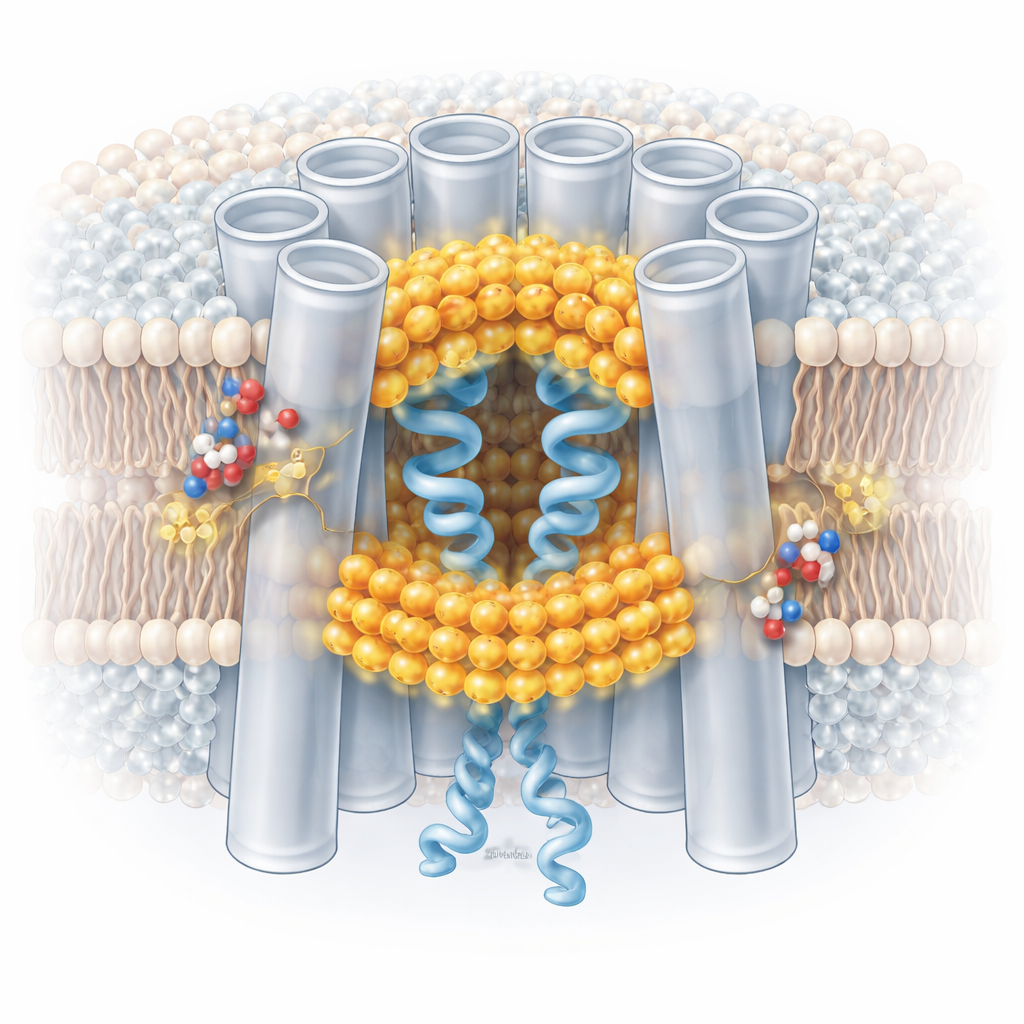
Обратный и точно настроенный предохранительный механизм
Отслеживая миллионы отдельных частиц каналов, авторы выяснили, что низкий pH не просто переводит каналы из полностью открытого в полностью закрытое состояние. Вместо этого он смещает популяцию в сторону смеси состояний: некоторые субъединицы внутри канала демонстрируют липид‑стабилизированные закрытые конформации, в то время как другие остаются более открытыми. Поведение закрывания в основном некоперативно — каждый строительный блок канала может реагировать в значительной степени независимо. Кислая среда способствует этим закрытым конформациям, но при восстановлении нейтрального pH липиды в порах возвращаются в мембрану, и каналы снова переходят в открытое состояние. Сохранённые аминокислоты, называемые гистидинами, которые приобретают положительный заряд при низком pH, по‑видимому, помогают привлекать и стабилизировать интерфейсные липиды, инициирующие этот процесс, что дает правдоподобный молекулярный pH‑сенсор.
Последствия для катаракты и защиты тканей
Эти результаты поддерживают модель, в которой липиды действуют как подвижные заглушки, обратимо контролирующие поток через щелевые контакты в ответ на кислотность. В хрусталике глаза такой механизм может помогать изолировать повреждённые клетки и препятствовать распространению токсичных сигналов, но хроническое или нарушенное управление закрыванием также может способствовать возрастному образованию катаракты. Поскольку подобные липидные вторжения наблюдались в родственных семейств каналов, работа указывает на более общий принцип: при стрессе сами клеточные мембраны могут предоставлять динамичные компоненты, помогающие выключать или включать жизненно важные каналы, что открывает новые идеи для лекарств, стабилизирующих либо открытое, либо закрытое состояние при заболеваниях.
Цитирование: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Ключевые слова: щелевые контакты, коннексин 46/50, pH‑управление, катаракта, крио‑ЭМ