Clear Sky Science · ru
Интегрированный мультиомный атлас раскрывает иерархию пространственно-временных регуляторных сетей гаструляции мыши
Как эмбрион формирует план тела
Каждое млекопитающее, включая человека, начинается как крошечный шар клеток, который должен быстро организоваться в сложный организм с головой, хвостом, спиной, животом и внутренними органами. Эта драматическая перестройка происходит в короткий период, называемый гаструляцией. В обзорной статье создана детальная многослойная карта этого процесса в эмбрионах мыши, показывающая, как гены, ДНК-переключатели и химические сигналы действуют вместе в пространстве и времени, направляя клетки к их будущим судьбам.
Наблюдая, как тысячи клеток делают выбор
Чтобы проследить гаструляцию в действии, исследователи проанализировали более 35 000 отдельных клеток из эмбрионов мыши на пяти близко расположенных стадиях — от ранней до поздней гаструляции. Для каждой клетки они измеряли не только то, какие гены включены, но и какие участки ДНК открыты и доступны, что указывает на их способность выступать регуляторными элементами. На основе этих данных они выделили 31 отдельный тип клеток и проследили, как ранние гибкие клетки постепенно расходятся по ветвям, образуя три основных зародышевых листка — эктодерму, мезодерму и эндодерму — которые в конечном счете формируют все ткани и органы. Они также разработали новый вычислительный метод BioCRE для более точного связывания генов с управляющими ими ДНК-элементами, что показало: многие важные переключатели находятся далеко от генов, которыми они управляют.
Построение 3D молекулярного атласа в реальном эмбриональном пространстве
Большинство одно-клеточных методов теряют исходное положение каждой клетки в эмбрионе, однако местоположение критично для понимания шаблонов развития. Команда обошла это, сопоставив свои одно-клеточные данные с существующей трехмерной картой активности генов в эмбрионах мыши. Результатом стал ST-MAGIC — «цифровой эмбрион», в котором каждая мелкая точка аннотирована вероятными типами клеток, экспрессируемыми ими генами и доступностью окружающей ДНК. Этот атлас показывает, например, как различные подтипы мезодермы — будущие сердце, мышцы и поддерживающие ткани — возникают в разных областях и как широко экспрессируемые гены, такие как Otx2, используют разные регуляторные элементы на внешней (эпибласт) и внутренней (висцеральный эндодерм) поверхностях эмбриона.
Когда разрывается симметрия и левое становится отличным от правого
Одной из поразительных особенностей плана тела является то, что левая и правая стороны не идентичны — вспомните сердце, смещенное немного влево. Авторы использовали свой пространственный атлас, чтобы детально рассмотреть латеральную мезодерму, где впервые появляются различия между левым и правым. Они обнаружили тонкие, но последовательные асимметрии в том, какие типы клеток обогащены по каждой стороне и какие участки ДНК более открыты. На правой стороне были более доступны регионы, связанные с сигнальным путем роста BMP; на левой — регионы, ассоциированные с генами, необходимыми для формирования сегментов и структур сердца. Некоторые из этих ДНК-элементов, включая недавно обнаруженные регуляторы гена Lefty2, становятся доступными до заметных различий в экспрессии генов, что указывает на то, что раннее «праймирование» хроматинового ландшафта готовит каждую сторону эмбриона по-разному интерпретировать сигналы.
Релей факторов направляет среднюю линию тела
Далее исследование сосредоточено на осевом мезенодерме — популяции клеток, которые сформируют нотохорд, стержневую структуру вдоль средней линии, помогающую организовать позвоночник и нервную систему. С помощью объединенных инструментов (ST-MAGIC и расширенной версии ST-MAGIC (+)) авторы проследили, как эти клетки возникают из передней примитивной полоски и расщепляются на две ветви: клетки узла, которые строят ресничную структуру, важную для восприятия лево‑правых сигналов, и передний мезенодерм, вносящий вклад в ткани средней линии. Они раскрыли иерархический релей транскрипционных факторов — белков, управляющих активностью генов. Ранние факторы, такие как EOMES, и промежуточные факторы, включая FOXA2 и LHX1, сначала открывают ключевые участки ДНК и задают чувствительность к главным сигналам, таким как WNT и NODAL. Позже «терминальные» факторы, такие как NOTO, SOX9 и недавно связанный POU6F1, включают специализированные генетические программы, например в отношении ресничек или внеклеточного матрикса.
Сигналы, хроматин и поздние специалисты
Интегрируя публичные наборы данных о том, где эффекторные белки путей WNT и NODAL связываются с ДНК, авторы показали, что чувствительность эмбриона к этим сигналам меняется в пространстве раньше, чем сами источники сигналов перемещаются. В области, приготовленной стать осевым мезенодермом, участки ДНК, восприимчивые к NODAL и WNT, открываются рано, и многие содержат мотивы для FOXA2, Zfp281 и других регуляторов, что указывает на кооперативный контроль. Экспериментальное удаление поздно действующих факторов NOTO и POU6F1 у мышей нарушало экспрессию генов, специфичных для узла и ресничек, и укорачивало реснички узла, при этом основная открытая ДНК‑ландшафт оставался в значительной степени нетронутым. Это указывает на то, что ранние факторы закладывают эпигенетическую основу, тогда как поздние факторы в основном уточняют экспрессию генов без масштабной перестройки хроматина.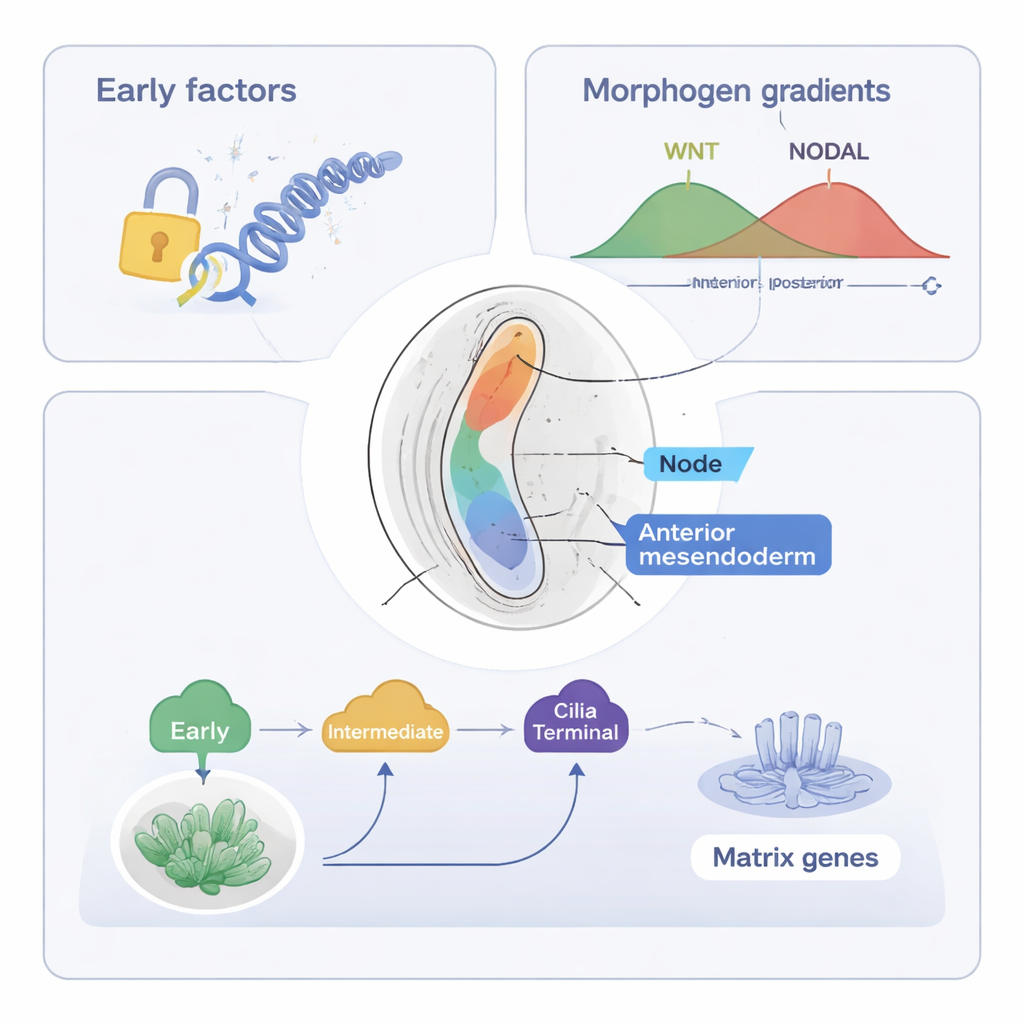
Почему это важно для понимания развития
Для неспециалиста эту работу можно рассматривать как создание высокоразрешающей «электрической схемы» того, как эмбрион прокладывает план тела. Авторы демонстрируют, что решения о судьбе клеток во время гаструляции зависят не только от присутствующих сигналов, но и от того, когда и где открываются ДНК‑переключатели и какие транскрипционные факторы действуют по очереди. Их атласы ST-MAGIC и ST-MAGIC (+) предоставляют ресурс для исследования этих взаимоотношений в пространстве и времени, предлагая основу, которая может быть полезна для изучения врожденных дефектов, моделей эмбрионов на основе стволовых клеток и, в перспективе, аспектов развития человека.
Цитирование: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
Ключевые слова: гаструляция, сети регуляции генов, одно-клеточная мультиомика, паттернизация эмбриона, развитие мыши