Clear Sky Science · ru
Де-ново варианты в гене фактора сплайсинга SF3B1 ассоциируются с нарушениями нейроразвития
Когда один ген нарушает раннюю «черновую» схему мозга
Почему у некоторых детей развиваются трудности в обучении, судороги или проблемы с кормлением, хотя беременность и роды протекали нормально? В этом исследовании изучается один ген, называемый SF3B1, который помогает клеткам обрабатывать генетические сообщения. Авторы показывают, что новые, спонтанные изменения в этом гене могут тонко исказить то, как клетки мозга читают инструкции ДНК, приводя к ранее нераспознанному синдрому нейроразвития.
Главный редактор генетических сообщений
Каждая клетка нашего организма должна преобразовать «сырый» генетический текст в понятные инструкции прежде, чем она сможет синтезировать белки. Этот этап редактирования, известный как РНК-сплайсинг, удаляет некодирующие сегменты и сшивает полезные части. SF3B1 — центральный компонент клеточной «машины сплайсинга». До сих пор изменения в SF3B1 в основном связывали с раком, где опухолевые клетки приобретают мутации в этом гене в течение жизни. Новая работа задаёт другой вопрос: что происходит, когда повреждающее изменение в SF3B1 присутствует с момента зачатия во всех клетках организма?
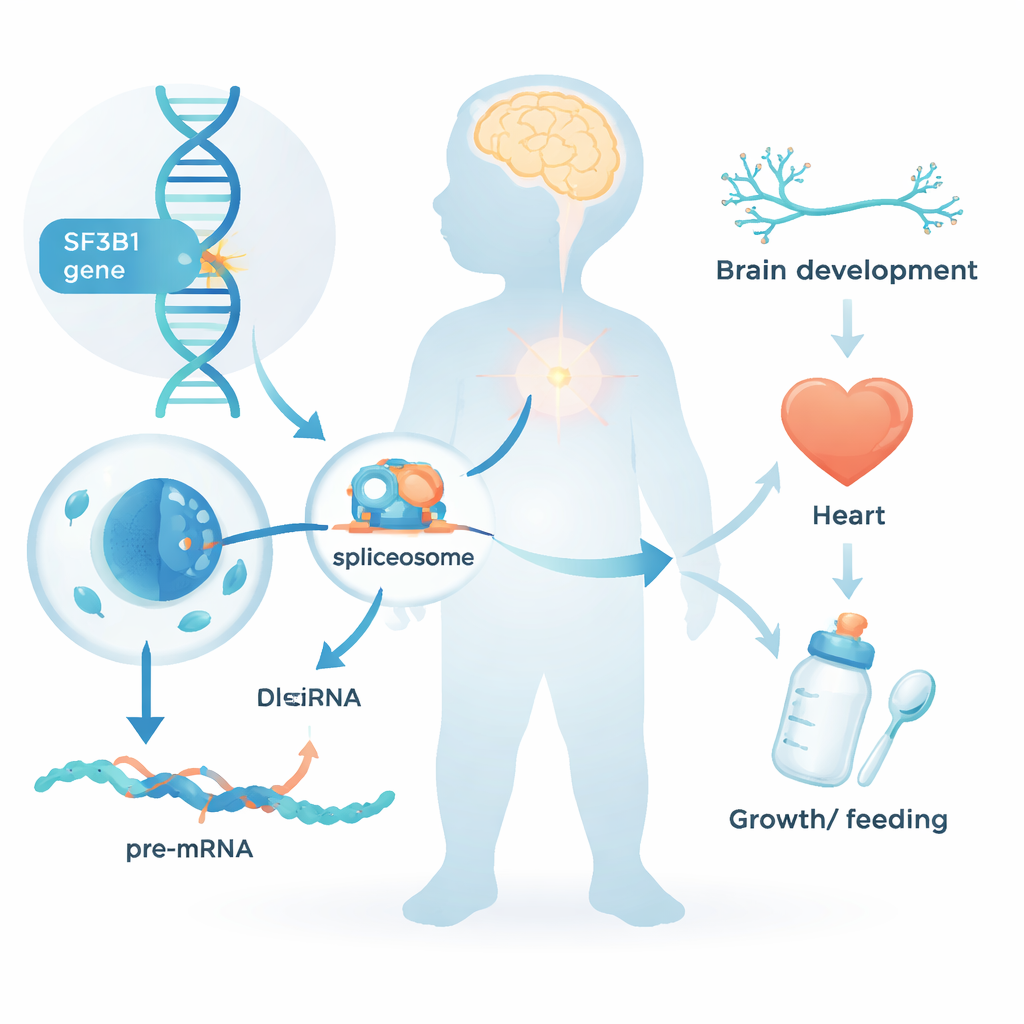
Недавно описанный детский синдром
Исследователи собрали данные о 26 детях и молодых взрослых, у которых выявлены редкие варианты SF3B1, преимущественно появившиеся де-ново — то есть не унаследованные ни от одного из родителей. Почти у всех наблюдались нейроразвитые проблемы: задержки в освоении сидения, ходьбы или речи; умственная отсталость преимущественно лёгкой–умеренной степени; и примерно у половины — судороги. У многих была низкая мышечная тонус и требовалась дополнительная помощь при кормлении, иногда через гастростому. Черты лица были слегка необычными, но не одинаковыми у всех детей; заметно распространённой особенностью была высокая или заячья нёбо. Несколько участников также имели пороки сердца, задержку роста или маленький размер головы, что показывает, что влияние изменений SF3B1 выходит за пределы мозга.
Два класса генетических изменений — две клинические картины
Исследователи выделили два широких типа вариантов SF3B1. В одну группу вошли «утрачивающие функцию» изменения, такие как преждевременные стоп-кодоны, которые, как ожидается, уменьшают количество работающего белка SF3B1. Вторая группа включала миссенс-варианты, при которых в белке изменяется одна аминокислота. Кластеризуя медицинские признаки у детей, команда обнаружила, что у тех, у кого были миссенс-варианты, как правило, наблюдались более тяжёлые и более сложные проблемы, включая более высокий уровень сердечных и желудочно-кишечных аномалий, низкий рост и микроцефалию. Варианты, приводящие к утрате функции, напротив, иногда наследовались от слабо поражённого или даже внешне здорового родителя, что позволяет предположить, что простое уменьшение количества SF3B1 у некоторых людей может сопровождаться относительно мягкими симптомами.
Ошибки тонкой настройки, а не полный сбой
Чтобы понять, как миссенс-варианты действуют внутри клеток, учёные воссоздали их в лабораторных клеточных линиях. Удивительно, но эти модифицированные белки SF3B1 по-прежнему могли выполнять базовую задачу сплайсинга достаточно хорошо, чтобы восстановить клетки, в которых нормальный SF3B1 был заглушен. Это исключает простую модель утраты функции. С помощью глубокого секвенирования РНК команда затем проанализировала весь набор клеточных сообщений. Они обнаружили, что миссенс-варианты тонко смещают сплайсинг сотен генов, особенно меняя выбор сайтов сплайсинга на концах экзонов и вызывая периодическое исключение экзонов. Масштаб нарушения был меньше, чем при классической раковой мутации SF3B1 K700E, но всё же существенным: многие затронутые гены участвуют в развитии мозга, формировании нервных связей и в фундаментальных процессах, таких как обращение с РНК и синтез белка.
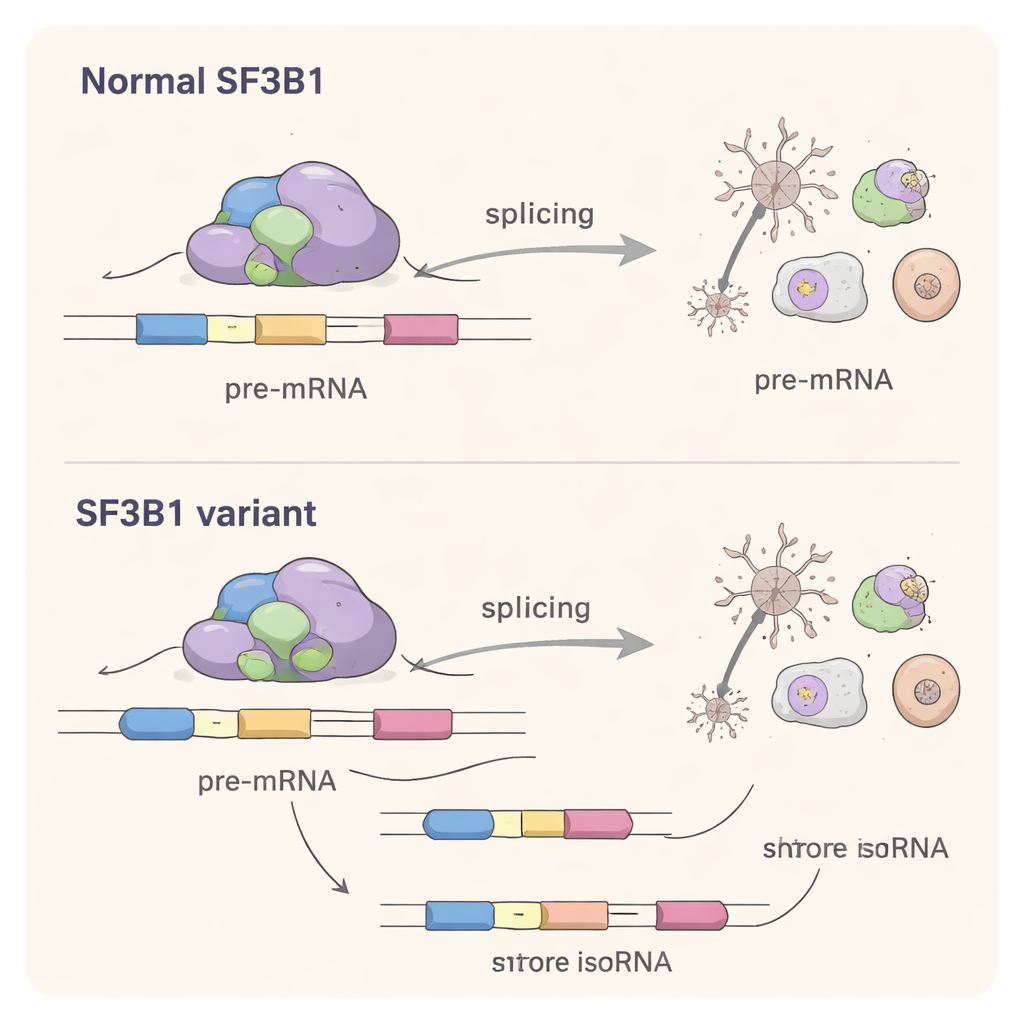
Общий механизм между раком и расстройствами мозга
Хотя большинство вариантов SF3B1, связанных с нейроразвитием, находятся в других позициях, чем хорошо известные раковые мутации, они нарушают тот же ключевой процесс: точное распознавание сайтов сплайсинга в РНК. Исследование показывает, что эти варианты развития имеют собственную «подпись сплайсинга», выбирая альтернативные сайты сплайсинга, которые часто находятся ближе к нормальным, чем те, которые предпочитаются при раке. Это указывает на механизм изменения функции, при котором мутантный белок конкурирует с нормальной копией и сдвигает машину сплайсинга в сторону слегка неверных вариантов во многих генах одновременно.
Что это значит для семей и будущих исследований
Для затронутых семей работа выявляет SF3B1 как новую причину нарушений нейроразвития, которую теперь можно проверить в клиниках генетики, что потенциально положит конец длительным диагностическим поискам. В более широком плане это добавляет SF3B1 в небольшой, но растущий список генов сплайсинга, чьи изменения могут приводить как к раку, так и к детским расстройствам мозга, в зависимости от времени и характера изменения гена. Картирование того, как конкретные варианты SF3B1 перекраивают РНК-сплайсинг, закладывает основу для будущих терапий, направленных на исправление нарушенного сплайсинга специфическими способами.
Цитирование: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Ключевые слова: РНК-сплайсинг, SF3B1, нарушения нейроразвития, де-ново варианты, сплайсосомопатии