Clear Sky Science · ru
Вискозэластичный гидрогель, подготовляющий макрофаги CAR, для лечения легочного фиброза
Превращение «дворников» организма в точные ремонтные бригады
Лёгочный фиброз — разрушительное заболевание лёгких, при котором нормальная эластичная ткань постепенно замещается жёстким рубцом. Людям становится трудно дышать, а существующие препараты в основном лишь замедляют ухудшение. В этом исследовании рассматривается новая идея: превратить собственные уборочные клетки организма, макрофаги, в сконструированных «умных дворников» и усилить их с помощью специально разработанного мягкого геля. В сочетании эти приёмы помогают клеткам обнаруживать виновников образования рубцов и даже ослаблять жёсткую ткань в повреждённых лёгких.
Когда заживление превращается во вред
В здоровых лёгких фибробласты поддерживают тонкую сеть коллагена, которая поддерживает воздушные мешочки. При лёгочном фиброзе эти клетки становятся гиперактивными и откладывают плотные волокна коллагена, которые задыхают воздухоносные пространства. Существующие лекарства могут ослабить эти процессы, но редко их обращают вспять. Авторы сосредоточились на белке на поверхности клеток — белке активации фибробластов (FAP), который при избытке присутствует на гиперактивных фибробластах, но мал в нормальной ткани. Если иммунные клетки можно обучить распознавать FAP, они могли бы выборочно удалять «убегающие» фибробласты, запускающие рубцевание, при этом щадя здоровые соседние клетки.
Перепрограммирование макрофагов для нацеливания на строителей рубцов
Макрофаги — это передвигающиеся иммунные клетки, которые обычно поглощают погибшие клетки, микробы и клеточный мусор. Команда оснастила их химерным антигенным рецептором (CAR), распознающим FAP, создав CAR‑макрофаги (CAR‑M). В лабораторных экспериментах эти CAR‑M эффективно поглощали и уничтожал и фибробласты с высоким содержанием FAP, в то время как в основном игнорировали клетки с пониженным уровнем FAP. Они также интенсивнее расщепляли гели, богатые коллагеном, чем немодифицированные макрофаги, что указывает на двойную выгоду: устранение клеток, создающих рубец, и прямое разрушение матрицы рубцовой ткани. Эти эффекты сохранялись как в стандартных клеточных линиях, так и в первичных макрофагах мышей, которые ближе к реальной тканевой среде. 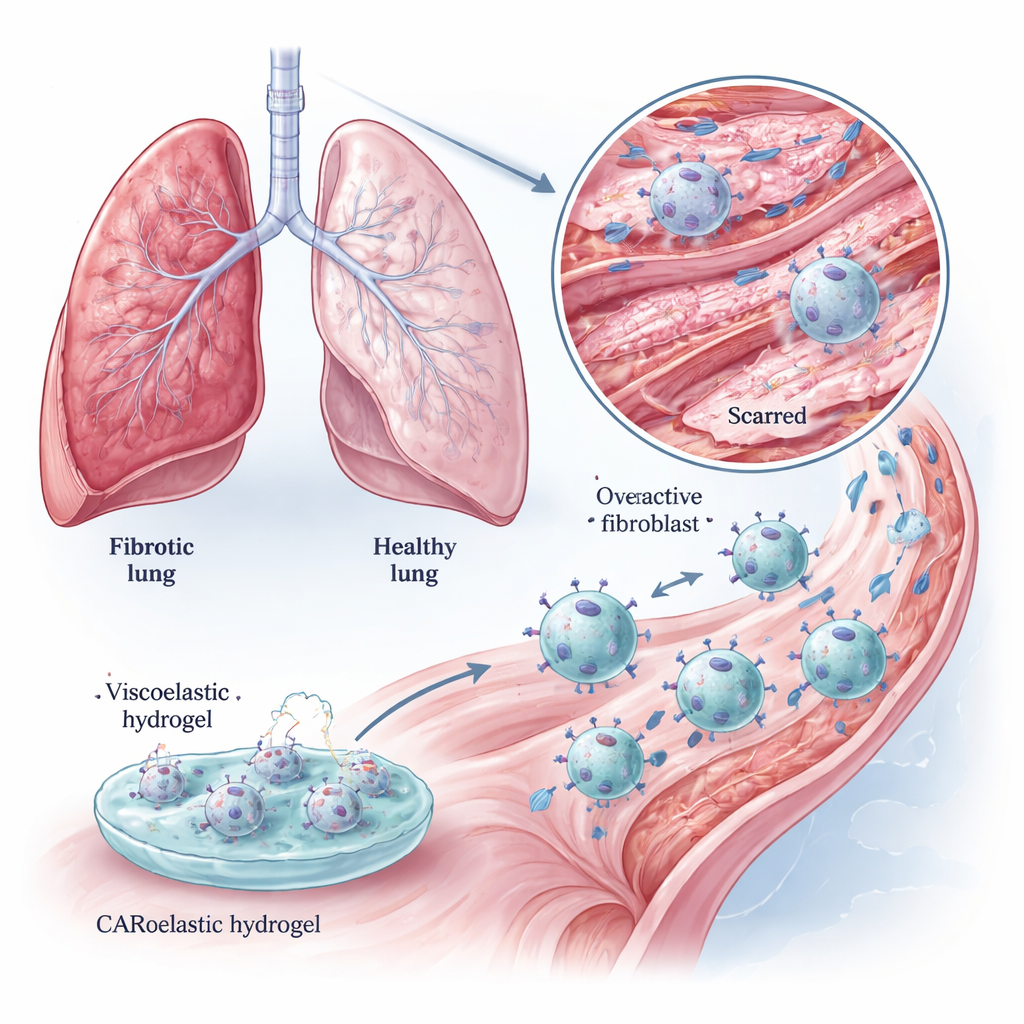
Подготовка иммунных клеток мягким вискозэластичным гелем
Генная инженерия клеток мощна, но сложна. Поэтому исследователи спросили, может ли чисто физический сигнал — мягкий вискозэластичный гидрогель — дополнительно настроить поведение CAR‑M. Они создали желатин‑альгинатный гидрогель, у которого можно тонко регулировать «модуль потерь», показатель того, как он медленно релаксирует под нагрузкой, не меняя при этом общей жёсткости. Когда CAR‑M кратковременно культивировали на гелях с подходящей вискозэластичностью, их способность убивать целевые фибробласты возросла сильнее, чем при обычных химических стимуляторах, и этот эффект сохранялся как минимум два дня. Эти «Gel‑CAR‑M» также включали гены, связанные с иммунной активацией и ремоделированием тканей, и одновременно понижали экспрессию генов, ассоциированных с фиброзом, что намекает на то, что опыт взаимодействия с гелем закрепил у клеток более антирубцовую идентичность.
Как более мягкая поверхность перенастраивает поведение клетки
Чтобы понять, почему гель имеет значение, команда изучила физическое состояние CAR‑рецепторов на поверхности клетки. Флуоресцентный зонд показал, что гидрогелем подготовленные CAR‑M имели более низкое натяжение мембраны — «внешняя кожа» клетки была более расслаблена. В таких условиях молекулы CAR распадались с плотных скоплений на более разобщённые одиночные единицы и пары. Биохимические тесты показали, что эти рассеянные рецепторы предпочитали формы, которые легче запускали внутриклеточную сигнализацию, особенно по путям вроде ERK, контролирующим активацию и способность к уничтожению. Имитирование снижения натяжения с помощью малого молекулы воспроизводило такое же расхождение рецепторов и улучшало уничтожение клеток‑мишеней, что поддерживает идею о том, что механическое расслабление мембраны достаточно, чтобы «предвооружить» клетки до встречи с их целями. 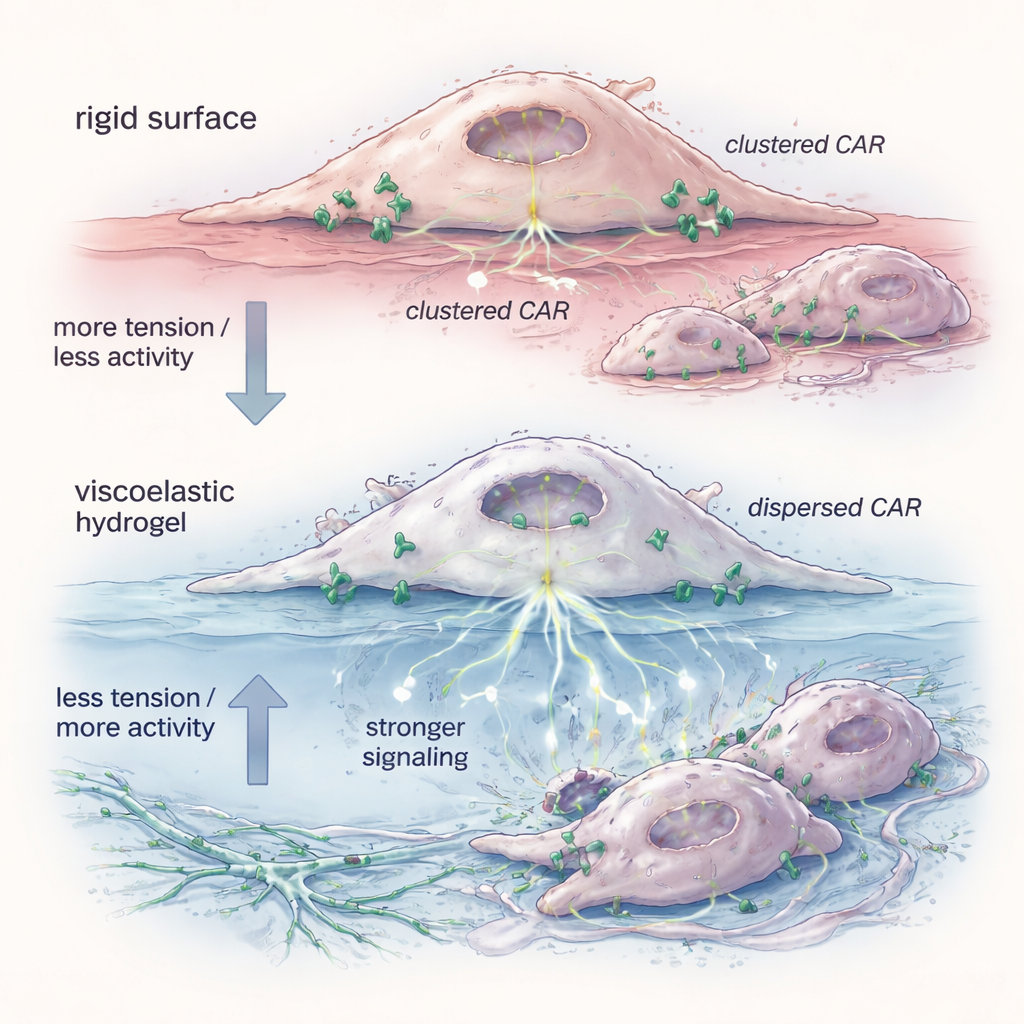
Восстановление рубцовых лёгких у мышей
Кульминационная проверка проводилась на мышиной модели лекарственно‑индуцированного лёгочного фиброза. Животным вводили либо обычные макрофаги, либо стандартные CAR‑M, либо гидрогелем подготовленные Gel‑CAR‑M. Все леченые мыши показали улучшение по сравнению с нелечеными контрольными животными, но Gel‑CAR‑M показали наилучшие результаты: в их лёгких было меньше коллагена, более нормальные воздушные пространства и меньше FAP‑положительных фибробластов. Анализы экспрессии генов в ткани лёгкого показали, что Gel‑CAR‑M эффективнее успокаивали воспалительные сигналы и снижали экспрессию рубцовых генов по сравнению со стандартными CAR‑M. Отслеженные клетки сохранялись в лёгком как минимум неделю, а расширенные проверки безопасности в течение 12 недель не выявили серьёзных повреждений органов, нарушений в крови или признаков аутоиммунитета.
Новое направление для клеточно‑основанных антифиброзных терапий
Для неспециалистов ключевое сообщение таково: сочетание направленной клеточной инженерии и «умных» материалов может превратить клетки врождённого иммунитета в высокоэффективные, но не чрезмерно генетически осложнённые инструменты борьбы с рубцами. Кратковременно поместив сконструированные макрофаги на тщательно настроенный мягкий гель, исследователи механически «предустановили» их поверхностные рецепторы в более отзывчивый режим. У мышей с лёгочным фиброзом это привело к лучшему удалению вредных фибробластов, разрушению лишнего коллагена и частичному восстановлению нормальной структуры лёгких — без очевидных проблем с безопасностью. Хотя до клинических испытаний на людях ещё далеко, эта стратегия указывает на то, что тонкая настройка физической среды терапевтических клеток может однажды сделать лечение фибротических заболеваний лёгких более мощным и более точным.
Цитирование: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Ключевые слова: лёгочный фиброз, терапия макрофагами CAR, вискозэластичный гидрогель, белок активации фибробластов, механобиология клеток