Clear Sky Science · ru
Молекулярная основа ингибирования de novo метилирования ДНК белком TCL1A
Как клетки решают, что запоминать
Каждая клетка вашего организма содержит по сути одинаковую ДНК, но нейроны, кровяные клетки и клетки кожи ведут себя очень по‑разному. Один из способов, которым клетки «запоминают» свою идентичность, — это химические метки на ДНК, процесс, называемый метилированием ДНК. В этом исследовании показано на атомном уровне, как маленький белок TCL1A способен выключать ферменты, наносящие эти метильные метки. Поскольку и метилирование ДНК, и TCL1A связаны с раком и репродуктивными нарушениями, понимание этой молекулярной борьбы за контроль может в будущем вдохновить новые терапевтические подходы.
Машина клетки по маркировке ДНК
Метилирование ДНК работает как штрих карандаша на полях генома, помогая заглушать одни гены и стабилизировать генетический материал в ходе развития клеток. Два фермента, DNMT3A и DNMT3B, — главные «пишущие», которые ставят новые метильные метки во время раннего развития и при специализации стволовых клеток. Если эти ферменты мутируют или их активность нарушается, узор ДНК‑меток может быть исказен и способствовать синдромам развития и кровяным ракам. TCL1A — белок, известный прежде всего своей ролью в раке клеток иммунной системы, где он часто чрезмерно экспрессируется. Ранние работы намекали, что TCL1A может связываться с DNMT3A и DNMT3B и притуплять их активность, но точный механизм этого блокирования оставался неизвестным.
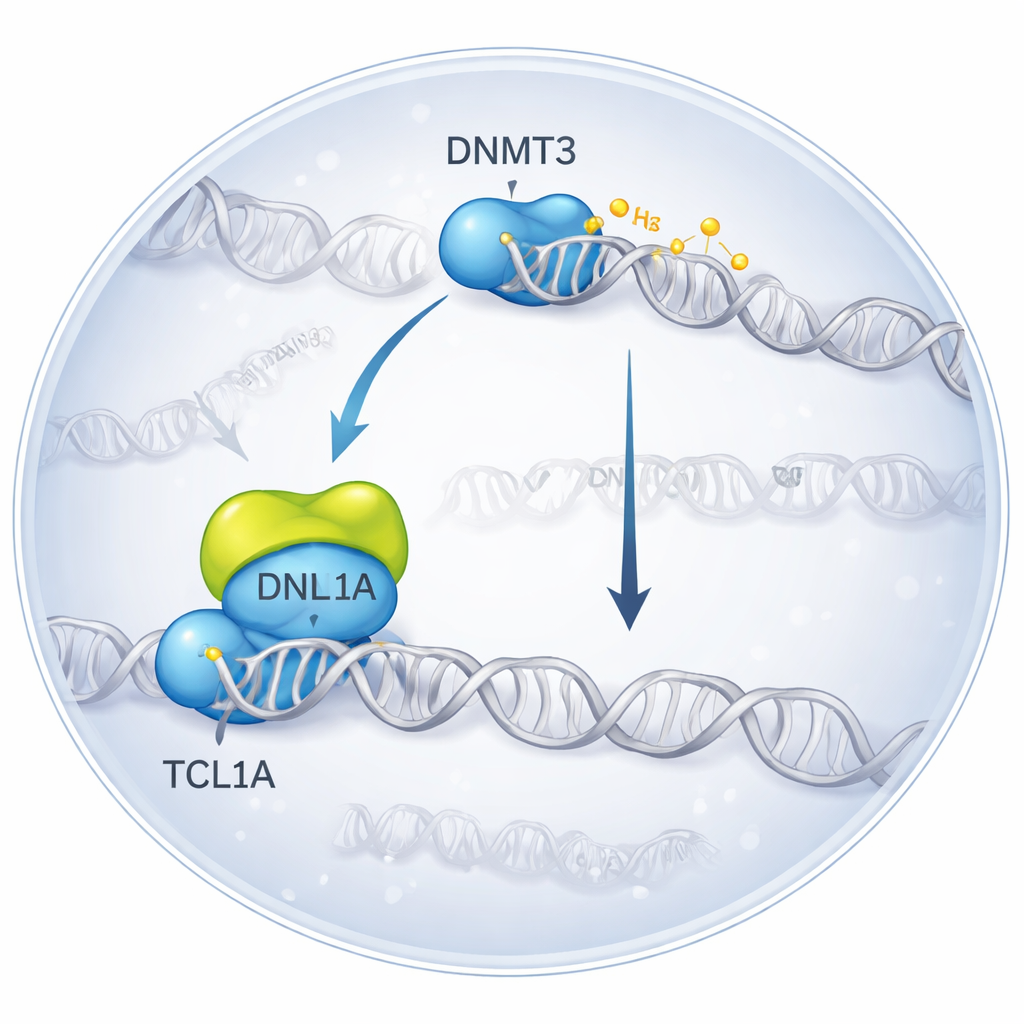
Заморозка молекулярной встречи в 3D
Исследователи использовали крио‑электронную микроскопию, метод, который визуализирует молекулы, быстро замороженные для съемки, чтобы увидеть комплекс, образуемый при связывании DNMT3A с TCL1A. Они обнаружили, что две молекулы DNMT3A образуют пару, и с каждой стороны на каталитическую часть DNMT3A присаживается димер TCL1A — та самая область, которая обычно взаимодействует с вспомогательными белками и ДНК. Поверхность связывания перекрывается с участком, куда обычно присоединяется другой партнер, DNMT3L, усиливающий активность DNMT3A. В биохимических тестах добавление TCL1A резко снижало способность как DNMT3A, так и DNMT3B метилировать ДНК, даже в присутствии DNMT3L, что подтверждает: структурный комплекс соответствует сильно ингибированному состоянию.
Изменение формы, которое заклинивает фермент
Посмотрев внимательнее, команда увидела, что связывание TCL1A не просто перекрывает активный центр как крышка. Вместо этого оно вызывает тонкое, но далеко идущее изменение формы DNMT3A. Две гибкие области фермента, известные как петля распознавания мишени и каталитическая петля, отодвигаются от позиций, которые они занимают при связывании DNMT3A с ДНК. В активной форме эти петли прижимаются к ДНК и образуют карман для маленькой молекулы‑«топлива» SAM, которая передает метильную группу. При присоединении TCL1A каталитическая петля складывается в карман для SAM и блокирует его, а также затрудняет доступ ДНК к ферменту. Измерения связывания подтвердили, что DNMT3A в комплексе с TCL1A уже не в состоянии обнаружимо захватывать ни ДНК, ни SAM.
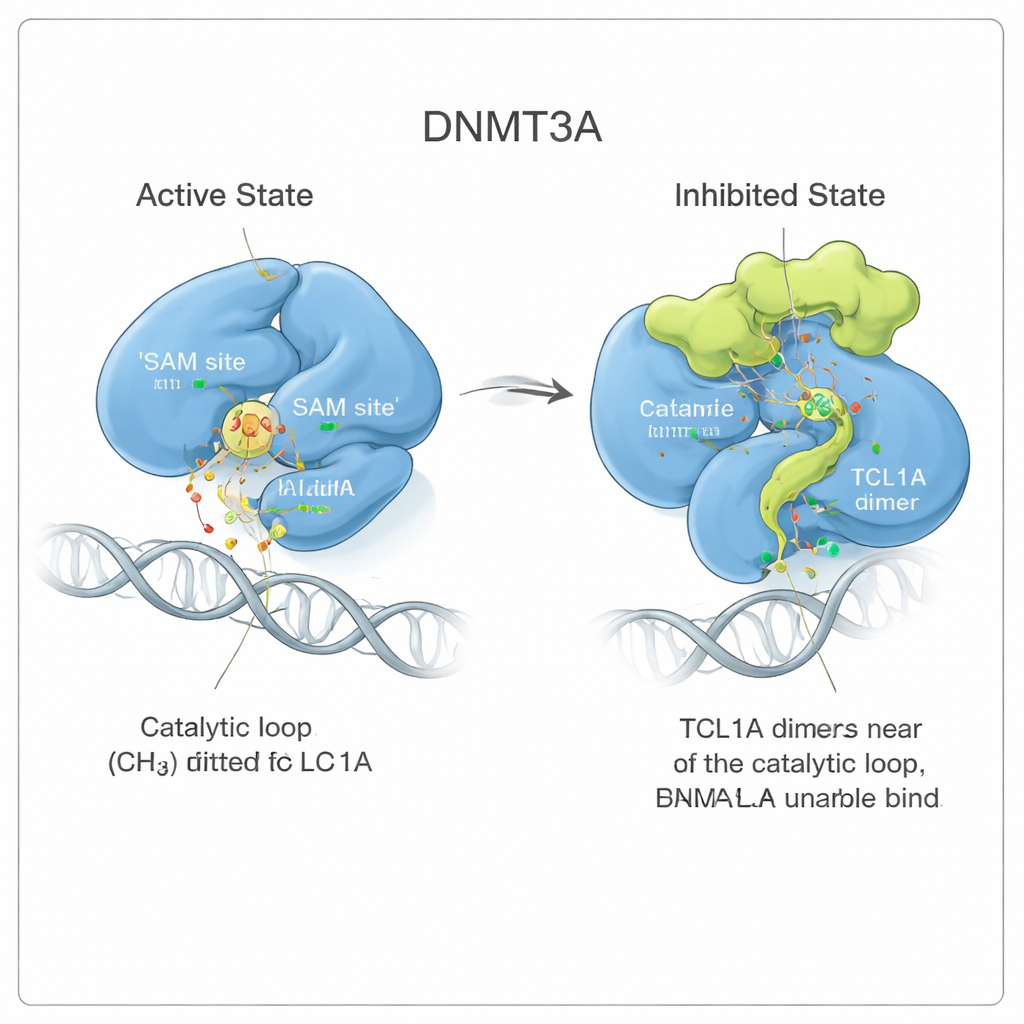
Наблюдение динамической пробки в движении
Чтобы понять, насколько стабильно это ингибированное конформационное состояние, авторы провели длинные молекулярно‑динамические симуляции — по сути физически обоснованные «фильмы» молекул в растворе. Когда DNMT3A был связан со своим активатором DNMT3L, каталитическая петля оставалась плотно в активной позиции. В присутствии TCL1A эта петля становилась гораздо более подвижной, махала и при этом периодически занимала карман для SAM, как водоросль, кружащаяся и всё же закупоривающая сток. Такое постоянное движение уменьшало доступное пространство для SAM более чем в десять раз, что поддерживает модель, в которой TCL1A использует природную гибкость DNMT3A, чтобы навязать динамическую, а не жесткую форму ингибирования.
Последствия для развивающихся клеток и болезней
Далее команда проверила, что означает эта молекулярная блокада для реальных клеток. Они генетически модифицировали мышиные эмбриональные стволовые клетки, чтобы те синтезировали человеческий TCL1A в стадии, когда клетки обычно активируют метилирование ДНК при начале дифференцировки. Геномное картирование метилирования показало, что клетки с переэкспрессией TCL1A не набирали обычный высокий уровень метилирования ДНК, очень напоминая клетки, в которых гены Dnmt3a и Dnmt3b были выключены. Мутантная версия TCL1A, слабо связывающая DNMT3‑ферменты, имела мало эффекта, что подчеркивает: решающим является физическое взаимодействие. Эти данные связывают структурный механизм с широкими эпигенетическими изменениями по всему геному.
Что это значит для здоровья
В совокупности работа показывает, как TCL1A может действовать как мощный тормоз ферментов, устанавливающих новые метки метилирования ДНК. Пришвартовываясь в критическом интерфейсе, TCL1A переставляет гибкие петли в DNMT3A и DNMT3B так, что они уже не могут связывать свою матрицу ДНК или химическое топливо, что приводит к глобальной потере метильных меток в клетках. В нормальном развитии такой точный контроль может помогать регулировать время и место, где добавляется метилирование. Когда TCL1A смещён или чрезмерно экспрессирован, как это бывает при некоторых кровяных раках и редких репродуктивных расстройствах, тот же механизм может нарушить эпигенетическую программу клетки. Понимание этого взаимодействия на атомном уровне открывает путь к разработке молекул, которые имитируют или противодействуют эффектам TCL1A, что теоретически может восстановить здоровые паттерны метилирования ДНК.
Цитирование: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Ключевые слова: метилирование ДНК, DNMT3A, TCL1A, эпигенетика, рак