Clear Sky Science · ru
Снижение RAD23A увеличивает продолжительность жизни и уменьшает патологию в мышиной модели протеинопатии TDP-43
Почему это исследование важно для семей и пациентов
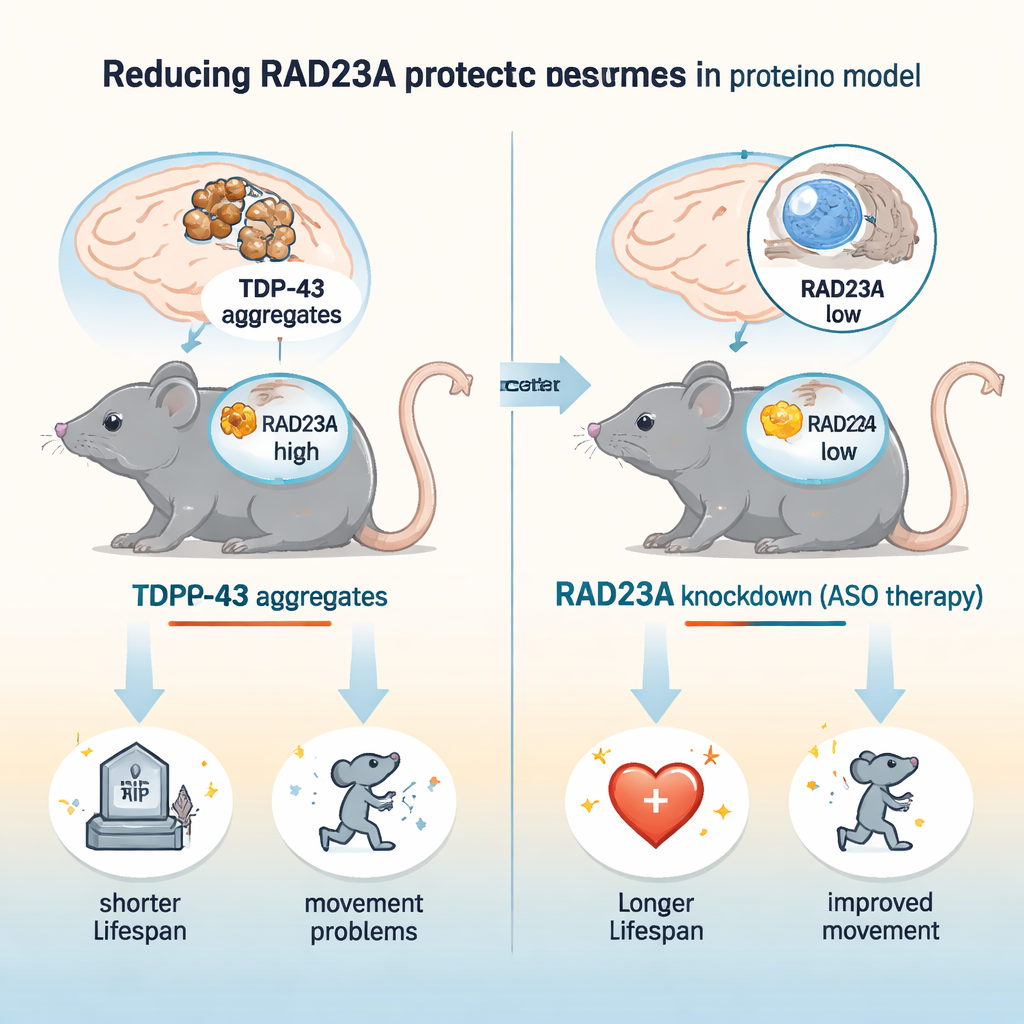
Во многих формах деменции и заболеваний моторных нейронов, включая боковой амиотрофический склероз (БАС) и лобно-височную деменцию (ЛВД), белки в клетках мозга неправильно сворачиваются, слипаются в агрегаты и постепенно отравляют нейроны. Одним из ключевых виновников является белок TDP-43, который в норме участвует в регуляции РНК, но становится токсичным при агрегации. В этом исследовании поставлен обнадеживающий вопрос: можно ли повысить устойчивость клеток мозга, ослабив другой белок — RAD23A, участвующий в обработке повреждённых белков? Авторы показывают на мышах, что снижение RAD23A удлиняет жизнь, улучшает подвижность и уменьшает повреждение мозга в модели болезни, вызванной TDP-43, намекая на новую стратегию лечения.
Транспортный затор белков в больных нейронах
Нейродегенеративные заболевания часто сопровождаются накоплением неправильно свернутых белков, которые система утилизации клетки не успевает удалять. При БАС и ЛВД TDP-43 выходит из ядра, образует липкие скопления и сильно метится убиквитином — сигналом, который обычно направляет белки к протеасоме, главной «шредерной» машине клетки. RAD23A — один из нескольких «перевозчиков», которые могут доставлять убиквитинированные грузы к протеасоме. Тем не менее предшествующие исследования на нематодах и культивируемых нейронах показали парадокс: потеря RAD23-подобных белков может защищать от повреждений, вызванных TDP-43. Это исследование поставило цель выяснить этот парадокс в живом млекопитающем мозге.
Понижение RAD23A в мышиной модели TDP-43
Исследователи использовали хорошо изученную мышиную модель TAR4/4, которая сверхэкспрессирует человеческий TDP-43 в нейронах и развивает нарушения двигательной функции, искривление позвоночника, тремор и раннюю смерть, воспроизводя ключевые черты БАС/ЛВД. Они снижали RAD23A двумя способами: введением новорождённым мышам антисмысловых олигонуклеотидов (ASO), уменьшающих уровень Rad23a-РНК, и скрещиванием с мышами с генетическим нокаутом Rad23a. Одно лечение ASO сократило уровень RAD23A в мозге и спинном мозге примерно на три четверти. У TDP-43-мышей снижение RAD23A увеличило продолжительность жизни примерно на 50% и отложило начало и уменьшило выраженность проблем походки, тремора, искривления позвоночника и сцепления задних лап. Любопытно, что полная генетическая утрата RAD23A не давала дополнительной пользы, что говорит о том, что частичное снижение оптимально, а длительное полное отсутствие может вызывать компенсаторные изменения.
Меньше воспаления, чище обработка белков и более спокойный геном
Микроскопический анализ моторной коры показал, что у TDP-43-мышей гибнут нейроны и активно включаются астроциты и микроглия — вспомогательные и иммунные клетки мозга. Снижение RAD23A сохраняло число нейронов и уменьшало маркеры воспаления и клеточной гибели. Биохимические исследования выявили, что переизбыток TDP-43 затапливает клетки убиквитинированными, детергент-нерастворимыми белками и втягивает субъединицы протеасомы в эти агрегаты, ослабляя способность клетки очищать повреждённые белки. Снижение RAD23A уменьшало общий объём убиквитинированных белков, сохраняло больше протеасом в растворимой, рабочей фракции и частично восстанавливало несколько видов протеасомальной активности. Одновременно снижение RAD23A уменьшало как общий, так и агрегированный TDP-43, включая особенно токсичный фрагмент ~25 килодальтон, и смещало локализацию TDP-43 из цитоплазмы обратно в ядро. Геномный РНК‑секвенс показал, что тысячи изменений экспрессии генов, вызванных TDP-43, частично обращались при снижении RAD23A, особенно гены, вовлечённые в нейрональную функцию, митохондриальное производство энергии и пути удаления агрегатов, такие как аггрефагия.
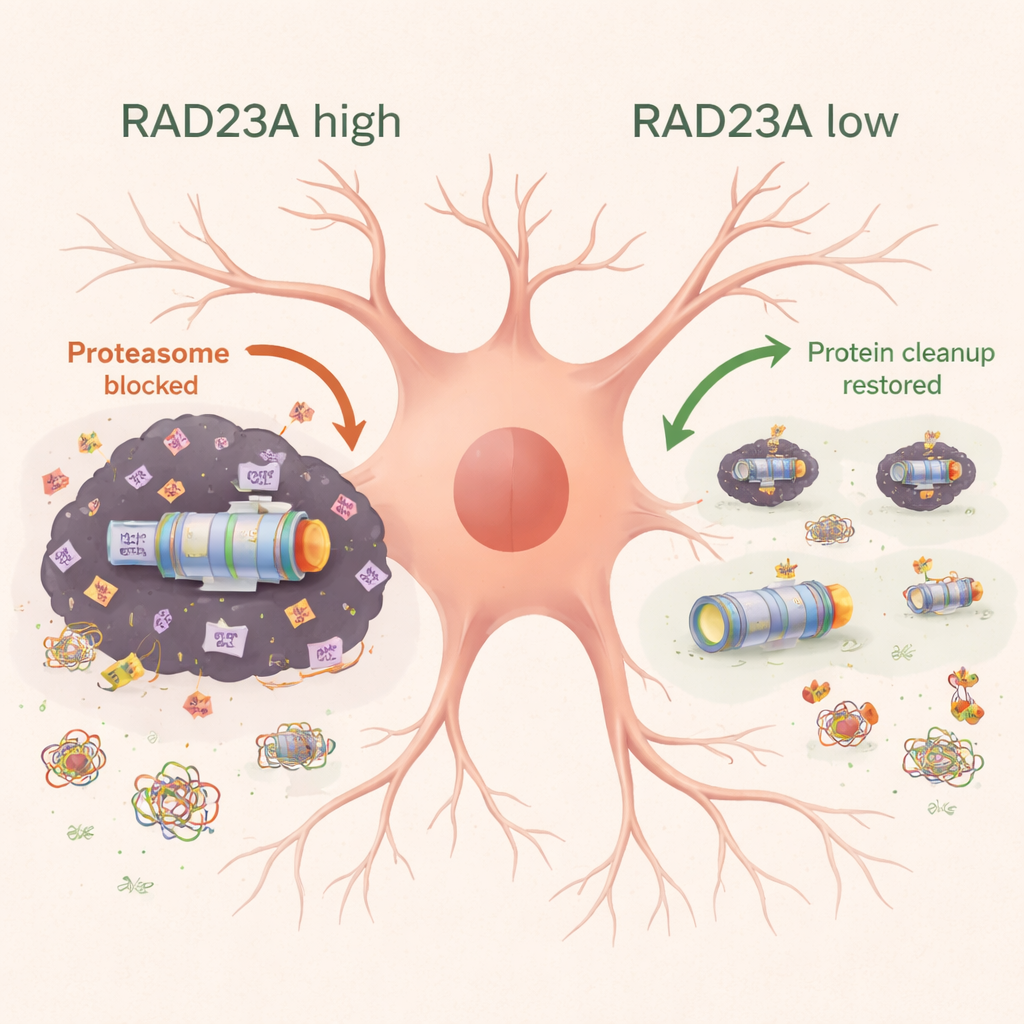
Перестройка «нерастворимого» протеома
Чтобы подробно изучить упрямые агрегаты, нерастворимые обычными детергентами, команда использовала масс-спектрометрию с тяжёлыми изотопами для каталогизации белков, захваченных в нерастворимой фракции коры мыши. Экспрессия человеческого TDP-43 привлекала компоненты протеасомы, цитоскелетные и транспортные белки и другую клеточную аппаратуру. При снижении RAD23A состав этого нерастворимого протеома изменялся: меньше протеасомных и транспортных белков было захвачено в агрегаты, тогда как некоторые рибосомные и стресс-ассоциированные белки увеличивались в составе агрегатов. Важно, что эта перестройка не просто повторяла изменения на уровне РНК, что указывает на то, что RAD23A главным образом влияет на перераспределение существующих белков между растворимым и агрегированным состояниями, а не на то, сколько каждого белка синтезируется.
Что это может значить для будущих терапий
В совокупности результаты рисуют RAD23A как мощный регулятор контроля качества белков в напряжённых нейронах. Частичное снижение RAD23A в модели, вызванной TDP-43, позволило уменьшить токсичные белковые агрегаты, восстановить работу механизма утилизации белков, ослабить вредные изменения экспрессии генов, ограничить воспаление в мозге и продлить жизнь и двигательную функцию. Поскольку аномальное накопление TDP-43 широко распространено как при наследственных, так и при спорадических формах БАС, ЛВД и родственных расстройств, нацеливание на RAD23A при помощи совместимых с человеком антисмысловых препаратов может предложить способ защитить нейроны, не блокируя сам TDP-43, который необходим для нормальной функции. Хотя предстоит ещё много проверок в других моделях и у людей, эта работа выделяет RAD23A как перспективную новую точку воздействия на общий путь нейродегенерации.
Цитирование: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Ключевые слова: TDP-43, БАС, агрегация белков, протеасома, антисмысловая терапия