Clear Sky Science · ru
Нервный центр инженерии органов
Почему подключение органов важно
Ученые приближаются к созданию заместительных органов в лаборатории, чтобы справиться с острой нехваткой донорских сердец, печеней, почек и других органов. Но большинство искусственных органов сосредоточено на кровеносных сосудах и игнорирует ещё один ключевой компонент: нервы. В этом обзорном материале объясняется, почему электрическая проводка организма необходима для роста органов, их повседневной функции и заживления, а также как исследователи учатся встраивать нервные сети в выращиваемые в лаборатории органы.
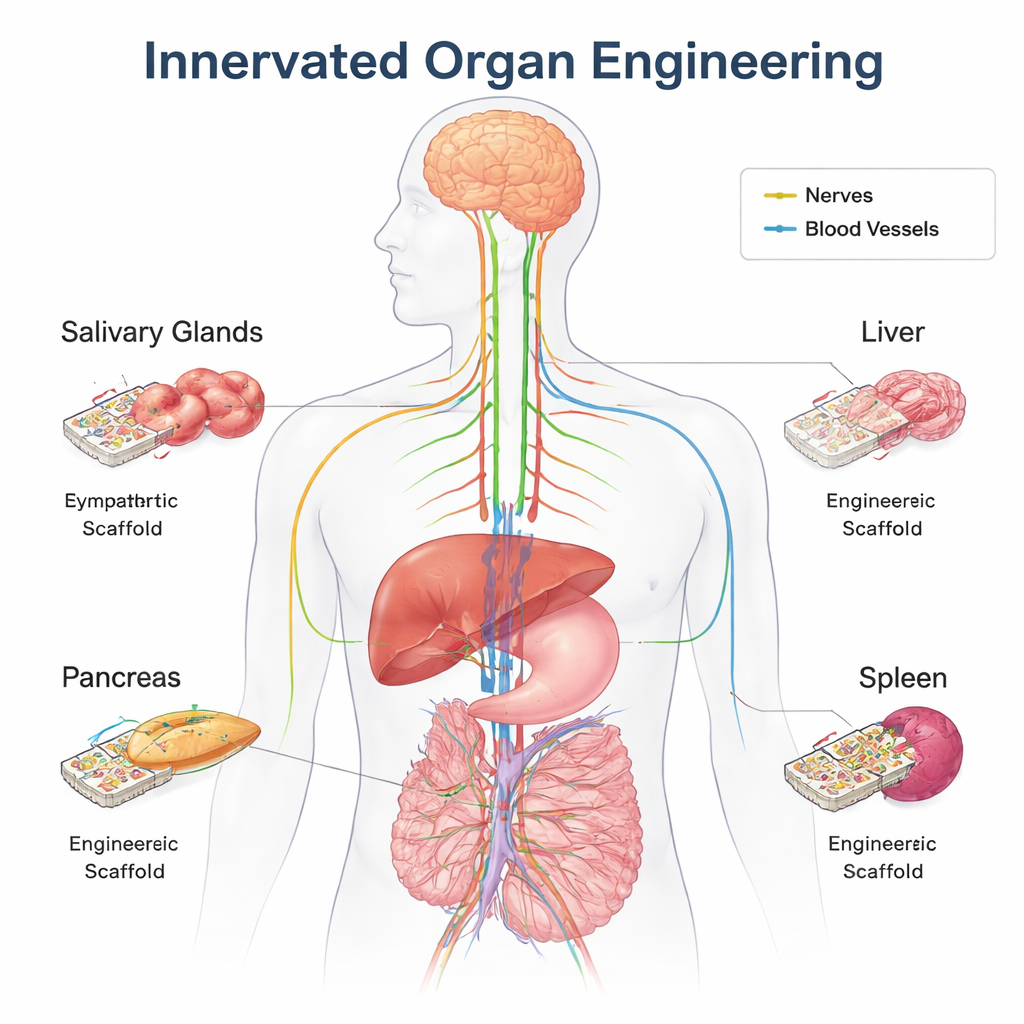
Скрытая сеть управления в теле
Каждый крупный орган пронизан нервными волокнами, которые постоянно общаются с мозгом и спинным мозгом. Через вегетативную нервную систему — ветви «борьбы или бегства» и «отдыха и пищеварения» — эти нервы тихо регулируют уровень сахара в крови, пищеварение, иммунные реакции, кровоток и многое другое. Они делают это, отправляя химические сигналы, такие как ацетилхолин и норэпинефрин, а также ощущая изменения, например растяжение, температуру или уровень питательных веществ. Помимо повседневного контроля, нервы помогают формировать органы до рождения, направляют заживление ран и поддерживают стволовые клетки, восстанавливающие ткани. Во многих местах нервы растут рядом с кровеносными сосудами, используя похожие направляющие сигналы, поэтому «проводка» и «водопровод» развиваются вместе.
Почему пересадки обходятся без нервов — а лабораторные органы нет
Традиционные трансплантаты обычно имплантируют без их исходных нервов. Трансплантированная печень или почка все ещё могут функционировать, потому что они получают гормоны и другие сигналы через кровоток, а со временем в организм реципиента могут врастать новые нервные волокна. У инженерных органов, созданных с нуля, такого «льготного периода» нет. Эти конструкции обычно лишены полного набора зрелых типов клеток и сложного поддерживающего матрикса, присутствующего в естественном органе. Точные нервные связи особенно важны для координации множества специализированных клеток в таких органах, как поджелудочная железа, печень, слюнные железы и селезенка. Авторы утверждают, что при конструировании органов снизу вверх — когда органы собирают из мелких блоков — заранее продуманная иннервация должна рассматриваться как требование дизайна, а не как дополнительная опция.
Как нервы формируют четыре ключевых органа
Обзор подробно рассматривает, как нервы влияют на четыре примера органов. В поджелудочной железе симпатические и парасимпатические волокна помогают формировать архитектуру инсулин-продуцирующих островков в ходе развития и затем тонко регулируют высвобождение инсулина и глюкагона по мере колебаний уровня сахара в крови. В слюнных железах ранняя парасимпатическая стимуляция сохраняет эпителиальные стволовые клетки живыми и направляет ветвление протоков, которые в конечном итоге выделяют слюну; повреждение этих нервов в неподходящее время нарушает нормальное формирование железы. Нервы печени чувствуют уровень соли, воды, сахара и жира в крови и корректируют метаболизм, кровяное давление и регенерацию после повреждений. В селезенке симпатические волокна непосредственно взаимодействуют с иммунными клетками, подавляя или усиливая воспаление и помогая организму реагировать на инфекции и стресс. Во всех этих органах потеря или неправильная проводка нервов связана с диабетом, нарушениями пищеварения, заболеваниями печени и ослабленным иммунитетом.
Создание органов с встроенной проводкой
Чтобы внедрить иннервацию в био-инженерные органы, ученые комбинируют продвинутую 3D-печать, умный дизайн каркасов и нейроны, полученные из стволовых клеток. Экструзионная и светозависимая биопечать позволяют размещать различные типы клеток и материалы в точных узорах, тогда как специализированные гидрогели и полимеры настроены для поддержки длинных ветвящихся нервных волокон. Уже были созданы печатные нейронные сети, нервно-мышечные единицы и миниатюрные ткани, похожие на мозг, демонстрирующие реалистическую электрическую активность. Авторы описывают практические схемы для иннервированных версий поджелудочной железы, слюнной железы, печени и селезенки: выделить или получить ключевые клетки органа, смешать их с вегетативными нейронами (симпатическими и парасимпатическими) в совместимых биочернилах, напечатать их в формах, имитирующих орган, и дозреть в биореакторах, чтобы нервы могли отрасти в ткань до имплантации.
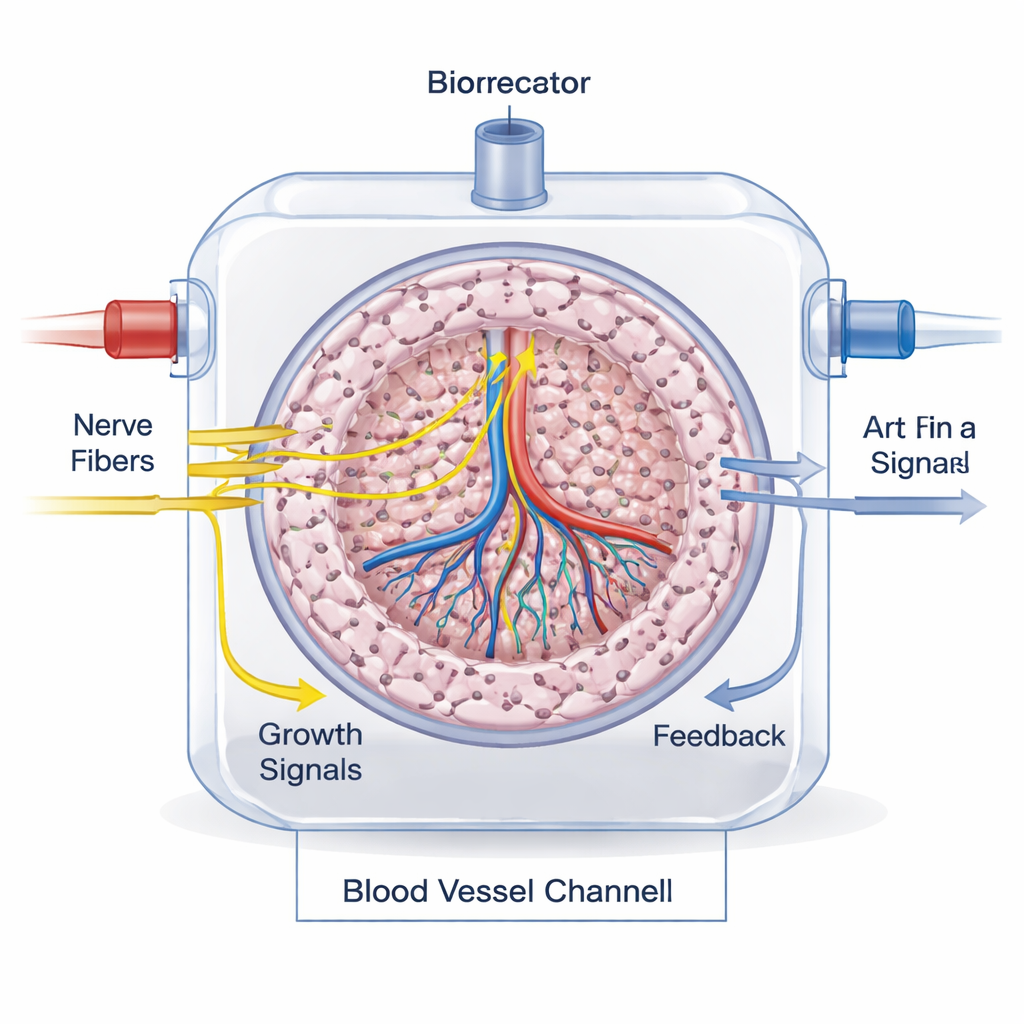
Как проверить, работает ли проводка
Проверка того, что нервы действительно интегрированы и функциональны, — серьёзная задача. В лаборатории исследователи окрашивают ткани на специфические для нервов белки, измеряют нейромедиаторы биохимическими тестами и используют живую визуализацию, чтобы наблюдать рост аксонов и реакцию клеток. Микрофлюидные платформы «орган-на-чипе» помогают моделировать реалистичный кровоток и сигнализацию между нервом и органом. В экспериментах на животных и, в перспективе, у пациентов иннервацию можно отслеживать, сочетая тканевую окраску, трассеры нервов и современные методы визуализации, такие как МРТ, КТ и ПЭТ-сканирование с специализированными радиоактивными соединениями, выделяющими симпатические или парасимпатические волокна.
От идеи к терапии
Статья заключает, что нервы — не лишняя роскошь, а основное требование для по-настоящему функциональных искусственных органов. Чтобы перейти от многообещающих лабораторных демонстраций к реальным терапиям, в будущем нужно улучшить масштабную биопечать сложных нервных сетей, усовершенствовать источники клеток (особенно человеческие стволовые клетки, дающие вегетативные нейроны) и разработать практичные клинические методы визуализации для мониторинга нейронной интеграции после имплантации. Если эти препятствия будут преодолены, органы следующего поколения смогут не только заменить утраченные ткани, но и бесшовно встроиться в собственные управляющие цепи организма, предлагая более надёжные и естественные лечения диабета, печёночной недостаточности, нарушений слюноотделения, иммунных дефицитов и других состояний.
Цитирование: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
Ключевые слова: инженерия органов, иннервация, биофабрикация, 3D-биопечать, вегетативная нервная система