Clear Sky Science · ru
Нанозимы расширяют границы биокатализа
Маленькие помощники, ускоряющие химию
От пивоварения до переваривания ужина наша жизнь зависит от невидимых помощников — катализаторов, которые ускоряют химические реакции. Более века считалось, что биологические катализаторы — это только хрупкие белки, а позднее и каталитическая РНК. В этом обзоре представлены «нанозимы» — крошечные сконструированные частицы, которые ведут себя как ферменты, но построены из прочных материалов, таких как металлы, оксиды и углерод. Они выдерживают жару, холод и агрессивные условия и начинают менять наше представление о химии в живых системах, болезнях, промышленности и даже о происхождении жизни.
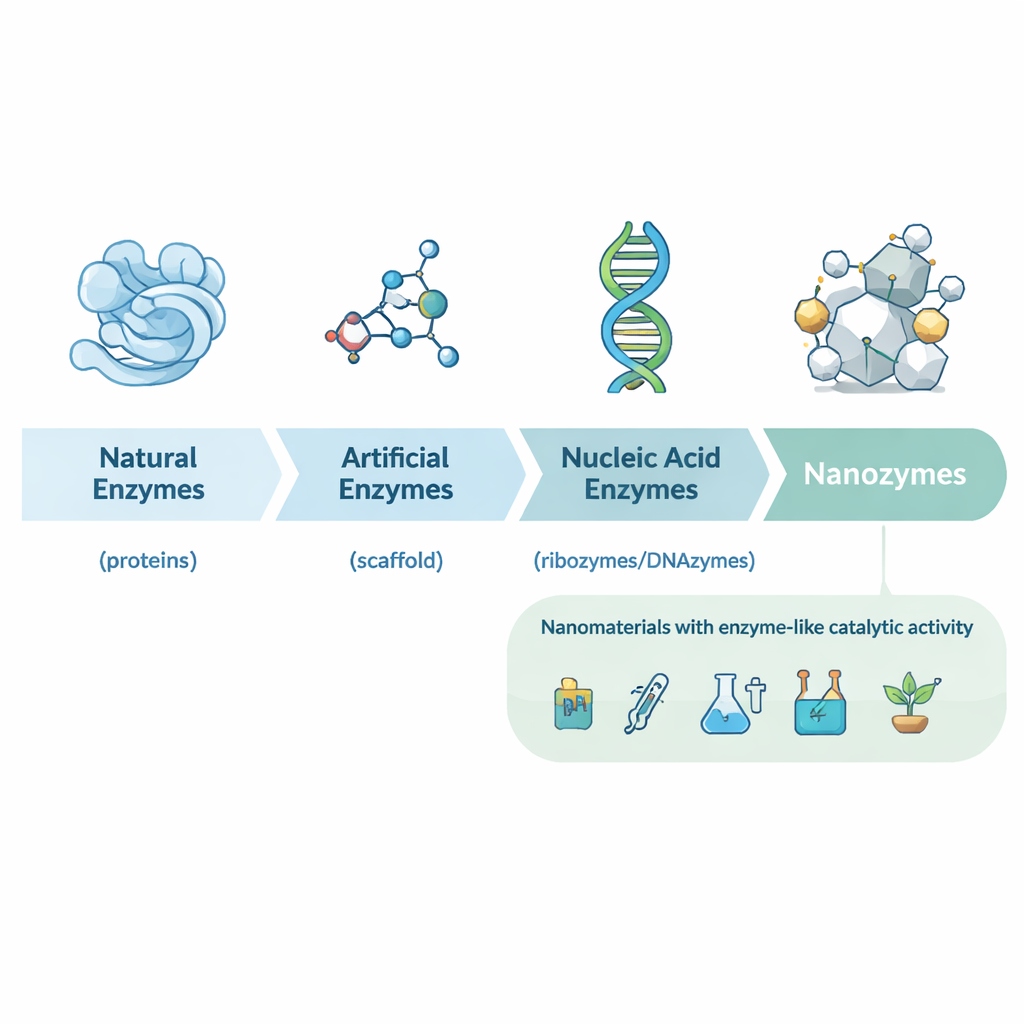
От природных ферментов к дизайнерским нанокатализаторам
Статья сначала прослеживает историю биокатализа: от ранних открытий белковых ферментов в дрожжах и желудочных соках до рибозимов (каталитической РНК) и множества искусственных ферментов, созданных из небольших молекул и антител. Эти традиционные катализаторы мощны, но часто дороги, нестабильны и сложны в массовом производстве. В начале 2000-х исследователи обнаружили, что некоторые наноматериалы — например, наночастицы оксида железа — могут имитировать поведение классических ферментов, таких как пероксидаза хрена. Это привело к понятию нанозимов: частиц нанометрового масштаба, чья собственная структура придаёт им ферментоподобную активность, а не присоединённые белки или малые молекулы.
Чем нанозимы отличаются
В отличие от ферментов, у которых есть единый, точно сформированный активный карман, нанозимы открывают множество активных участков по всей поверхности. Эти участки могут располагаться на краях кристаллов, дефектах или на границах между двумя материалами и в совокупности способны одновременно перерабатывать многие молекулы. Один активный центр нанозима обычно менее эффективен, чем у фермента, но одна наночастица может содержать тысячи таких центров, поэтому её суммарная каталитическая мощность может соперничать или превосходить природные ферменты. Их активность также можно настраивать, меняя размер, форму, химическое легирование и поверхностные покрытия — подобно тому, как регулируют архитектуру и проводку крошечной машины. Поскольку они сделаны из прочных твёрдых материалов, а не из деликатно свёрнутых белков, нанозимы продолжают работать при высоких и низких температурах или при высоком содержании соли, которые быстро выводят из строя большинство ферментов.
Как работают нанозимы и как их измеряют
Авторы показывают, что нанозимы часто подчиняются тем же базовым кинетическим правилам, которые биохимики используют для ферментов, например поведению по Михаэлису—Ментен, когда скорость реакции зависит от того, насколько легко катализатор связывает и превращает субстрат. Но есть важные особенности. Одна частица может содержать несколько типов активных центров, поэтому один нанозим способен выполнять разные реакции или даже противоречивые процессы, например одновременно образовывать и разрушать реактивные формы кислорода. Это может порождать сложные «нетекстовые» кинетические кривые, скрывающие множественные процессы за одним плавным трендом. Обзор объясняет, как исследователи расчленяют такие поведения, оценивают, сколько активных центров реально существует, и сравнивают общую активность различных нанозимов с помощью стандартных единиц, что критически важно для превращения интересного материала в надёжный инструмент.
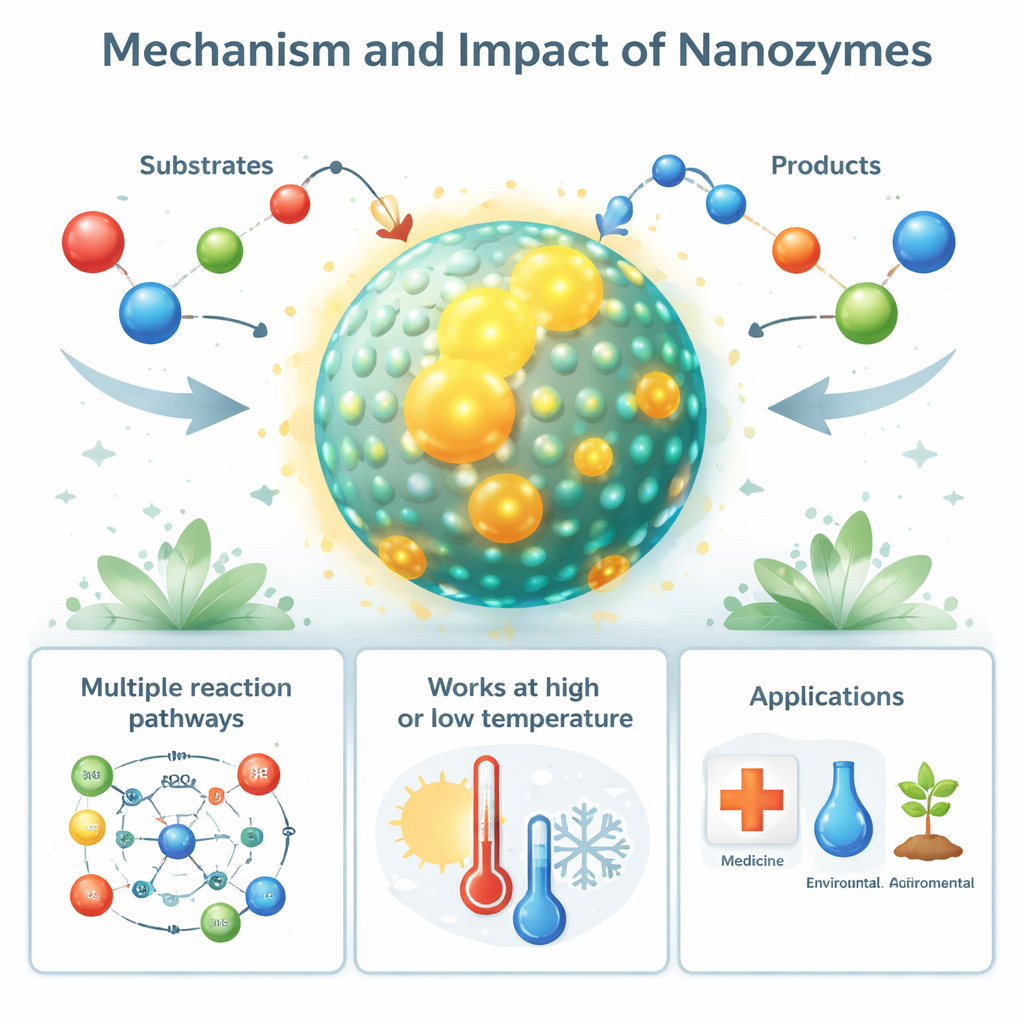
От природных нанозимов к прикладным использованиям
Любопытно, что поведение, напоминающее нанозимы, не ограничивается лабораторией. Определённые биологические наноструктуры, такие как белковые «клетки» с железом (ферритин) и магнитные частицы в бактериях (магнетосомы), действуют как природные нанозимы, которые помогают контролировать вредные реактивные формы кислорода. Даже белковые волокна, связанные с болезнями, например амилоидные отложения при болезни Альцгеймера, могут приобретать пероксидазоподобную активность нанозима, повреждая соседние клетки. В прикладной области синтетические нанозимы используются как более дешёвая, более прочная альтернатива ферментам в диагностических тестах, биосенсорах и промышленных анализах. Их способность либо генерировать, либо удалять реактивные формы кислорода используется для уничтожения опухолевых клеток и бактерий, защиты тканей от окислительного стресса и помощи сельскому хозяйству в противостоянии засухе, засолению и загрязнению.
Проектирование следующего поколения «умных» катализаторов
Смотря вперёд, авторы выделяют ключевые задачи: определить точные атомные структуры, выступающие активными центрами; повысить селективность реакций, чтобы нанозимы действовали только там и тогда, где нужно; и обеспечить безопасность и стабильность в организме. Они указывают на передовую визуализацию, квантово‑уровневые симуляции и машинное обучение как мощные инструменты для прогнозирования и оптимизации работы нанозимов. Поскольку нанозимы могут функционировать в экстремальных условиях, реагировать на свет, тепло, звук или магнитные поля и иногда выполнять несколько реакций последовательно, они могут лечь в основу новых терапий, экологических технологий и промышленных процессов. Обзор приходит к выводу, что нанозимы расширяют само определение биокатализа и даже могут дать подсказки о том, как примитивные катализаторы когда‑то приводили в действие химию ранней жизни.
Цитирование: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Ключевые слова: нанозимы, биокатализ, наночастицы, имитаторы ферментов, реактивные формы кислорода