Clear Sky Science · ru
Нанопоровое детектирование конформаций белков и пептидов для прикроватных приложений
Почему крошечные формы белков могут изменить ваше следующее обследование
По мере старения населения заболевания, такие как болезнь Альцгеймера, Паркинсона, сердечные болезни и рак, становятся более распространёнными. Многие из этих болезней начинаются с того, что жизненно важные белки и небольшие фрагменты белков (пептиды) едва заметно меняют свою форму задолго до появления симптомов. Современные клинические тесты чаще измеряют количество биомаркера, а не то, нормальна ли его форма или искажена. В этой статье рассматривается технология, называемая нанопоровым детектированием, которая электрически «ощупывает» форму и химию отдельных молекул белка, и утверждается, что она может стать основой будущих прикроватных тестов, выполняемых за минуты на небольшом приборе.
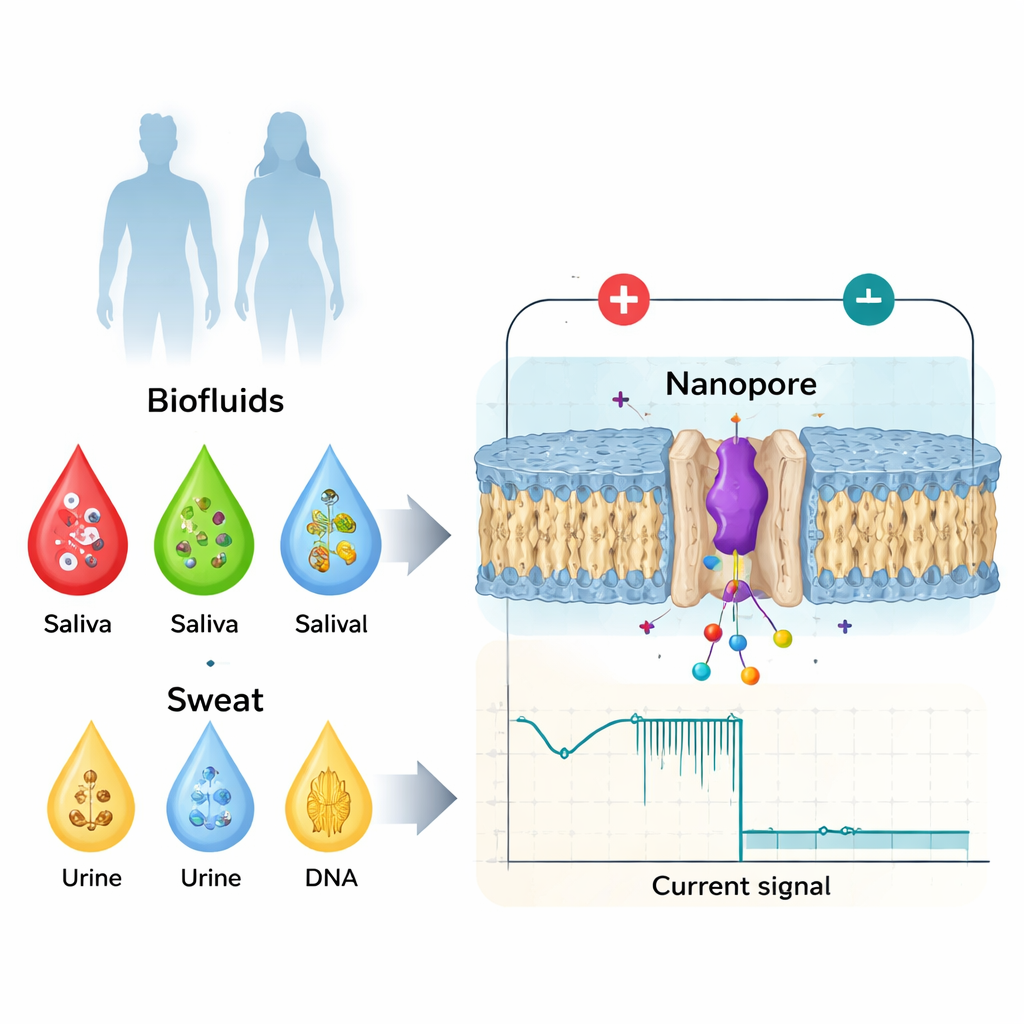
От простых анализов крови к биомаркерам, чувствительным к форме
Врачи уже используют множество биомаркеров, взятых из крови, слюны, мочи или пота — например белки, гормоны или малые молекулы — для отслеживания состояния здоровья и болезней. Традиционно внимание уделялось грубым изменениям: увеличению копий белка, повреждению ДНК или наличию вирусного компонента. Но биология оказывается более тонкой. Один и тот же белок может быть включён или выключен из‑за крошечных изменений структуры, химических меток, добавляемых после синтеза, или зеркальных форм его строительных блоков. Эти мелкие изменения могут менять связываемость белка с партнёрами, его склонность к агрегации или перенос сигналов и связаны с проблемами свертывания крови, нейродегенеративными заболеваниями и раком. Стандартные инструменты госпиталей — масс‑спектрометрия, тесты на основе антител и методы высокоразрешающей визуализации — мощны, но дорогие, медленные, требуют высококвалифицированного персонала и обычно не подходят для быстрого простого использования в прикроватной диагностике.
Чем нанопора отличается
Нанопоровое детектирование переворачивает задачу. Вместо усреднения по триллионам молекул метод исследует их по одной, когда они проходят через крошечное отверстие в мембране, ширина которого составляет всего несколько миллиардных долей метра. Применяется напряжение, чтобы ионы текли через пору и создавали стабильный электрический ток. Когда белок или пептид входит в пору, он частично блокирует этот ток. Глубина провала тока, его продолжительность и тонкие особенности формы зависят от размера молекулы, заряда и конформации (трёхмерной складки). Тщательно проектируя пору — используя либо модифицированные белковые каналы, либо твёрдотельные материалы — исследователи могут удерживать отдельные биомолекулы достаточно долго, чтобы получить насыщенные электрические «отпечатки», позволяющие различать не только разные белки, но и тонкие варианты одного и того же биомаркера.
Чтение болезненно значимых изменений по одной молекуле
Обзор подчёркивает, как нанопоры уже использовались для разрешения медицински важных различий, которые другим методам трудно заметить. Они способны различать пептиды, отличающиеся одной аминокислотой, обнаруживать варианты гемоглобина, связанные с болезнью, прямо в крови, и распознавать короткие пептиды, похожие на гормоны, которые различаются лишь одним строительным блоком или даже зеркальной формой этого блока. Нанопоры также способны фиксировать посттрансляционные модификации — небольшие химические метки, такие как фосфат, сахар или сульфат, — которые регулируют, ведут ли себя белки, вовлечённые в болезнь Альцгеймера, Паркинсона, свертывание крови или рак, нормально или патологически. В некоторых экспериментах внутри поры удерживается отдельный фермент или связывающий белок, и изменения в его электрическом сигнале показывают в реальном времени, как он связывает партнёров или проводит реакции, потенциально выявляя сбои в путях, связанных с заболеванием.
К быстрым прикроватным тестам
Поскольку каждое событие блокировки соответствует одной молекуле, нанопоровые приборы могут быть чрезвычайно чувствительными, обнаруживая всего несколько тысяч копий биомаркера в сложной жидкости. Авторы обсуждают стратегии преодоления ключевых препятствий для клинического использования: увеличение скорости захвата редких молекул, стабилизация мембран или использование гибридных твёрдо‑биологических пор, а также применение машинного обучения для автоматической классификации сложных электрических паттернов в понятные диагностические категории. Они также показывают, как косвенные подходы — например, прикрепление ДНК-меток или связывающих партнёров — могут усиливать слабые сигналы или позволять одновременно измерять несколько биомаркеров, при этом сохраняя большую часть конформационной информации, которая делает нанопоры уникальными.
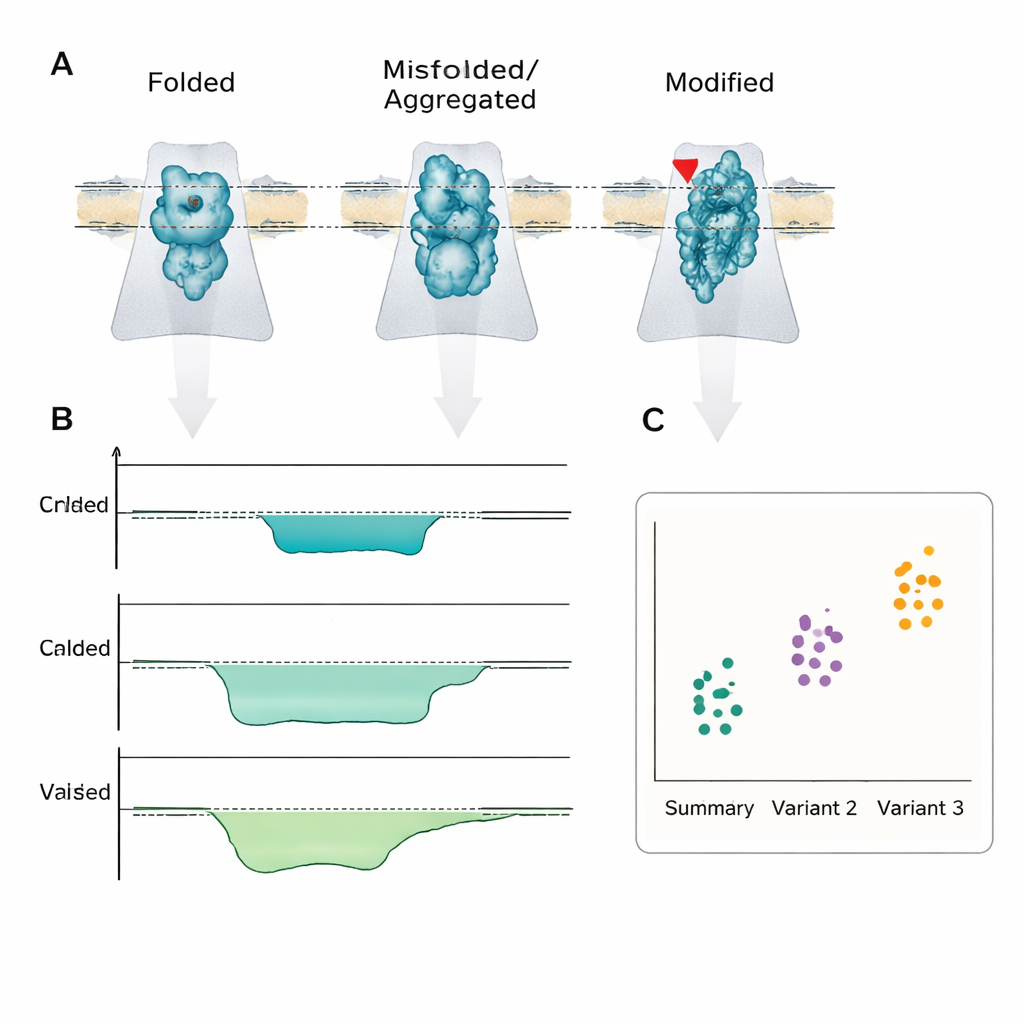
Что это может значить для пациентов
Главная мысль в том, что болезнь часто определяется не столько количеством белка, сколько тем, какая форма или химическая версия присутствует. Нанопоровое детектирование — одна из немногих технологий, способных непосредственно считывать эти различия на уровне одиночных молекул достаточно быстро и просто, чтобы быть интегрированными в портативные устройства. Хотя остаётся множество инженерных и задач по стандартизации, авторы утверждают, что, подобно тому как нанопоровые секвенаторы ДНК вошли в клинику, сенсоры белков и пептидов на основе нанопор в конечном итоге могут обеспечить быстрые прикроватные тесты, которые не только сигнализируют «что‑то не в порядке», но и точно указывают молекулярное неправильное сворачивание или модификацию, лежащую в основе состояния пациента.
Цитирование: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Ключевые слова: нанопоровое детектирование, белковые биомаркеры, диагностика у постели пациента, посттрансляционные модификации, болезни, связанные с конформацией