Clear Sky Science · ru
Освещая влияние N‑концевой ацетилирования: от белка к физиологии
Как крошечные химические метки изменяют поведение белков
Каждая клетка вашего тела заполнена белками, которые должны правильно сворачиваться, попадать в нужное место, собираться в молекулярные машины и удаляться при повреждении. В этом обзорном материале рассматривается тонкое, но чрезвычайно распространённое химическое изменение на одном конце многих белков — так называемая N‑концевая ацетилирование — и показано, как этот небольшой «кеп» контролирует всё: от роста клеток и реакции на стресс до развития сердца и функций мозга.
Белковая «крышечка», о которой большинство из нас не слышало
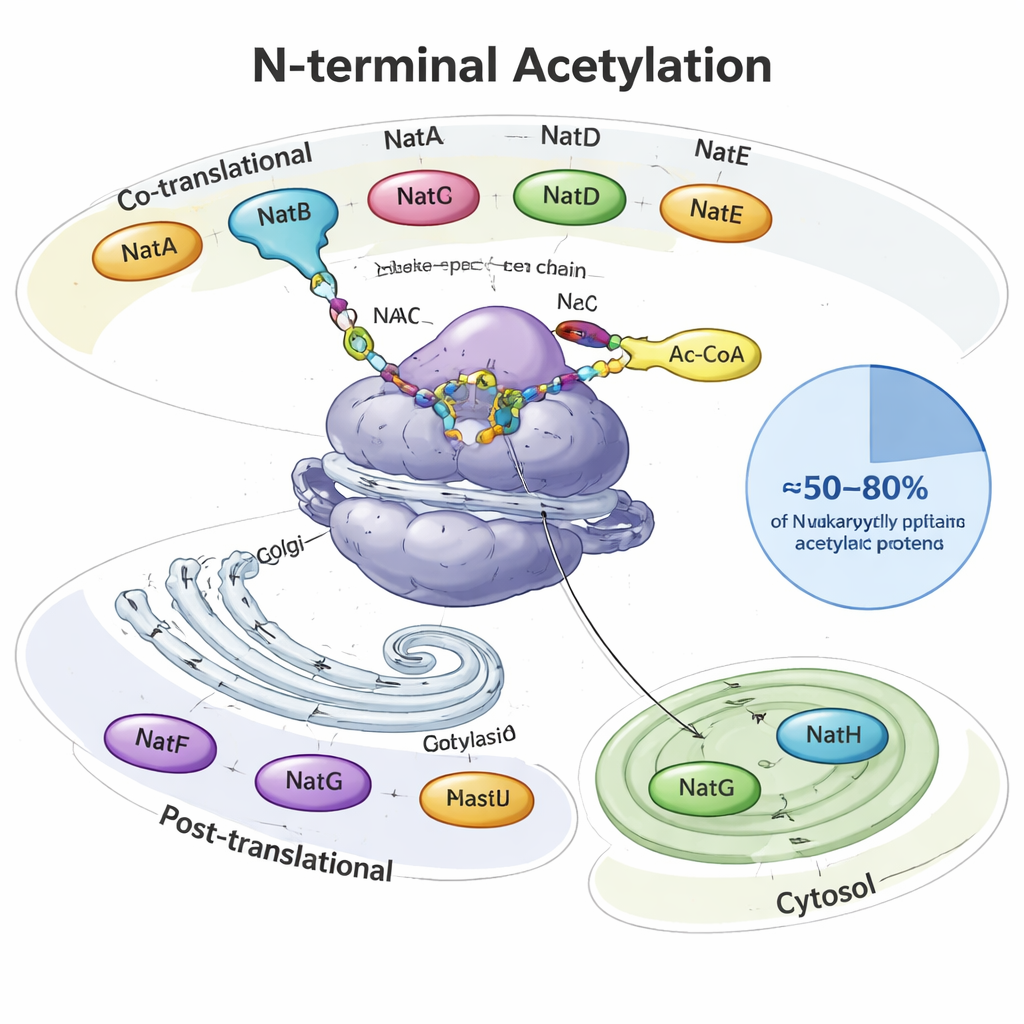
Когда белок синтезируется, он выходит из клеточной белковой фабрики — рибосомы — словно растущая нить. В самом начале — на N‑терминале — многие эукариотические белки получают ацетильную группу, крошечную двухуглеродную «крышечку». Специализированные ферменты, называемые N‑концевыми ацетилтрансферазами (NAT), выполняют эту работу, используя в качестве донора общий метаболический молекула (ацетил‑CoA). У дрожжей, растений и животных существует восемь основных типов NAT (NatA–NatH), которые распределяют работу. Некоторые действуют в то время, когда белок ещё синтезируется, другие работают после синтеза и локализованы в определённых местах, таких как аппарат Гольджи или растительные пластиды. В совокупности они модифицируют примерно от половины до четырёх пятых всех клеточных белков, причём каждый NAT узнаёт предпочтительные стартовые последовательности из двух‑четырёх аминокислот.
Много ферментов, у каждого — своя специализация
NatA, NatB и NatC выполняют основную работу, действуя прямо у рибосомы и покрывая большие участки «N‑концевого ацетилома». Один только NatA может модифицировать около 40% человеческих белков, как правило тех, у которых первый метионин отрезается. NatB и NatC действуют на белки, сохраняющие начальный метионин, но различаются по предпочтениям соседних аминокислот. Другие NAT более избирательны: NatD нацелен лишь на несколько гистонов, упаковывающих ДНК; NatF — на трансмембранные белки в аппарате Гольджи; NatG работает внутри растительных пластид; а NatH (NAA80) завершает особый двухэтапный процесс созревания актина, главного компонента клеточного каркаса. В статье собраны структурные и биохимические данные, показывающие, как вспомогательные субъединицы прикрепляют эти ферменты к рибосомам или мембранам и тонко настраивают, какие белки они модифицируют.
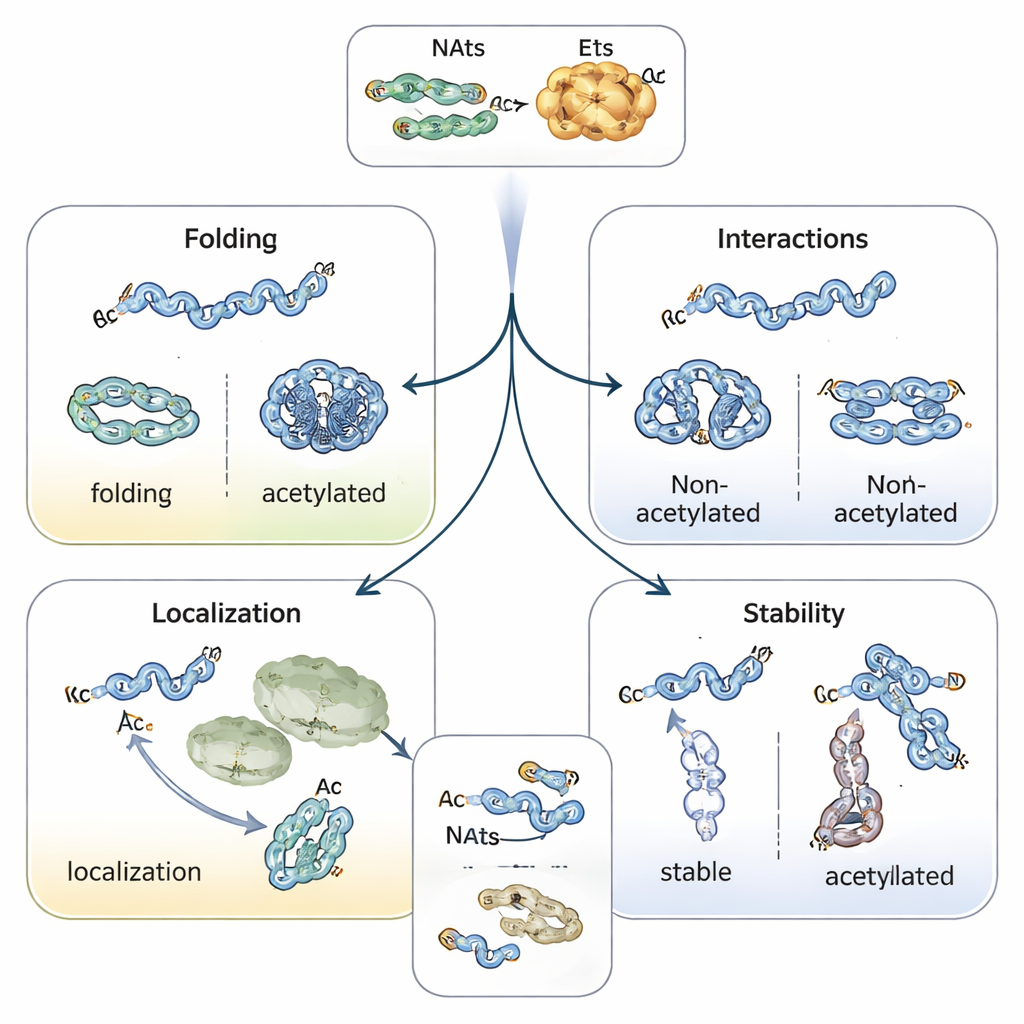
Управление сворачиванием белков, их локализацией и сроком службы
Добавление ацетильной «крышечки» меняет химические свойства начала белка, часто стабилизируя спиральные структуры и влияя на сворачивание. Например, белок альфа‑синуклеин, связанный с болезнью Паркинсона, склонен меньше агрегироваться и принимать более безопасную конформацию при ацетилировании N‑конца. Тропомиозин, партнёр актина, гораздо лучше связывается и регулирует актиновые нити при правильной ацетиляции. У растений и животных N‑концевая ацетилирование может служить своего рода адресной меткой, помогая белкам попадать в хлоропласты, лизосомы или аппарат Гольджи. Возможно наиболее примечательно его участие в определении продолжительности жизни белков: незащищённый N‑конец может расцениваться как «сигнал деградации» ферментами, помечающими белок убиквитином, тогда как ацетилирование может маскировать этот сигнал и стабилизировать белок — или, в некоторых случаях, создавать условную метку, распознаваемую только когда белок неправильно свернут или не в том комплексе.
От физиологии клетки до развития и болезней
Поскольку N‑концевая ацетилирование затрагивает столь многие белки, нарушение работы NAT приводит к широким последствиям для организма в целом. Удаление NatA, NatB или NatC в модельных организмах часто вызывает тяжёлые нарушения развития, изменённую реакцию на стресс или даже летальность, тогда как более специализированные ферменты, такие как NatF и NatH, дают более узкие проблемы — например кальциноз мозга или потерю слуха. У людей наследственные мутации в нескольких генах NAT лежат в основе редких нейроразвитийных синдромов с интеллектуальной недостаточностью, пороками сердца или мышечной слабостью. Та же система часто гиперактивна при раке: повышенные уровни NAT коррелируют с плохим прогнозом и могут способствовать росту опухоли, метастазированию и устойчивости к терапии. Изменения N‑концевого ацетилирования также влияют на белки, склонные к агрегации, такие как альфа‑синуклеин и хантингтин, связывая эту модификацию с механизмами нейродегенеративных заболеваний.
Дальнейшие направления и медицинский потенциал
Авторы делают вывод, что, хотя теперь мы знаем большинство основных ферментов, добавляющих эти N‑концевые «крышечки», мы по‑прежнему понимаем лишь часть конкретных белковых мишеней и правил регуляции. Важная тема — что ацетилирование в начале белка часто защищает его от преждевременной деградации, а также создаёт контекст‑зависимые сигналы для контроля качества. Ключевые открытые вопросы — какие убиквитинлигазы читают какие N‑терминальные паттерны и существует ли фермент, способный снимать эти «крышечки». Поскольку NAT находятся на пересечении стабильности белков, регуляции генов и ответов на клеточный стресс, селективные ингибиторы NAT — и, возможно, будущие инструменты, позволяющие точечно изменять N‑концевую ацетилирование белков, связанных с болезнью — выглядят многообещающе для разработки новых терапий при раке, заболеваниях сердца и нейродегенерации.
Цитирование: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Ключевые слова: модификация белка, N‑концевая ацетилирование, качество белков, нейродегенеративное заболевание, онкология