Clear Sky Science · ru
Метилирование м6A РНК модулирует антивирусный ответ при целиакии
Когда вирус и глютен объединяются
Целиакия часто воспринимается как простая пищевая проблема: съел глютен — и кишечник пострадал. Это исследование показывает более сложную картину, в которой обычный кишечный вирус и крошечная химическая пометка на наших молекулах РНК действуют совместно, подтолкнув иммунную систему к долговременному повреждению. Понимание этого скрытого уровня регуляции может помочь объяснить, почему лишь у некоторых людей развивается целиакия, и указать на новые подходы к лечению, выходящие за рамки безглютеновой диеты. 
Скрытая метка на наших генетических сообщениях
Клетки непрерывно считывают гены и переписывают их в РНК — короткие «послания», которые говорят клетке, какие белки синтезировать. Эти послания не статичны: их можно украшать химическими метками, которые действуют как маркеры, меняя, насколько активно послание читается. Одна из наиболее распространённых меток называется m6A — крошечное изменение в буквах РНК. Известно, что вирусы изменяют эти РНК‑метки в инфицированных клетках, а ранние работы уже связывали m6A с тем, как глютен вызывает воспаление в кишечнике при целиакии. Авторы статьи спросили, может ли вирус‑индуцируемое изменение m6A помочь переключить иммунитет от толерантности к пище на атаку.
Доказательства от пациентов с целиакией
Исследователи сначала изучили кровь и кишечные биоптаты у людей с активной целиакией и у контрольной группы без целиакии. Они обнаружили, что у пациентов с целиакией выше уровни антител к реовирусу — двуцепочечному РНК‑вирусу, инфицирующему кишечник, что указывает на более частое или сильное воздействие. В тканях кишечника у этих пациентов ключевые антивирусные «сигнальные» гены, особенно IRF7, были включены в более высокой степени, наряду с провоспалительными молекулами, такими как STAT1 и привлечающим иммунные клетки CXCL10. В то же время машины, добавляющие и считывающие метки m6A, работали активнее, и общий уровень m6A на РНК был выше. Экспрессия антивирусных генов возрастала и убывала синхронно с генами, связанными с m6A, что наводит на мысль, что одна и та же система контроля может управлять как защитой от вирусов, так и аутоиммунным повреждением.
Как глютен усиливает вирусную тревогу
Чтобы проверить причинно‑следственную связь, команда создала модель, напоминающую целиакию, в культивируемых кишечных клетках. Они имитировали вирусную инфекцию с помощью синтетической двуцепочечной РНК, затем добавляли переваренные фрагменты глютена, подобные тем, что появляются в кишечнике после еды. Подобие вируса само по себе усиливало и IRF3, и IRF7 — два главных переключателя антивирусного ответа. Но при добавлении глютена IRF7 давал заметный дополнительный всплеск, тогда как IRF3 — нет. Исследователи обнаружили, что при таких условиях метки m6A увеличивались в определённом участке РНК IRF7, и что эта РНК физически взаимодействовала с ферментом, «пишущим» m6A (METTL3), и ферментом, «стирающим» её (ALKBH5). Повышение уровня m6A — либо за счёт увеличения METTL3, либо за счёт снижения ALKBH5 — приводило к ещё большему увеличению IRF7, связывая синергию глютена и вируса напрямую с этой модификацией РНК. 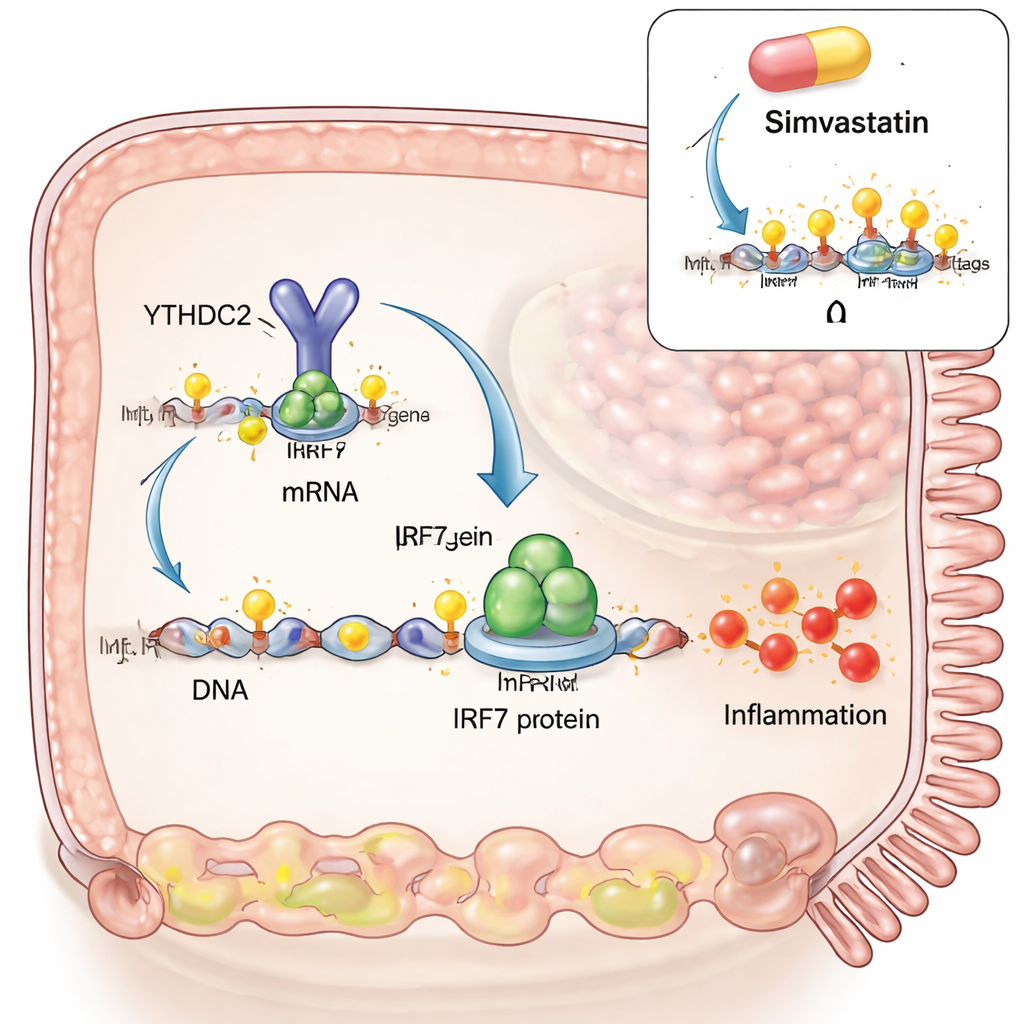
Молекулярный посредник и неожиданный препарат
Далее авторы спросили, как метки m6A на РНК IRF7 фактически меняют поведение клетки. Они создали версию РНК IRF7 с тем же кодом белка, но без сайтов m6A. Такая РНК давала сопоставимое количество транскрипта, но значительно меньше белка IRF7 и не вызывала включения последующих провоспалительных генов, таких как STAT1 и CXCL10. Отсутствующим звеном оказался белок‑ридер YTHDC2, который обычно связывается с m6A в кодирующей области и помогает эффективному трансляционному синтезу белка. Без сайтов m6A YTHDC2 уже не мог сцепиться с РНК IRF7. Блокада «пишущего» фермента METTL3 в клеточной модели снижала уровень белка IRF7 и CXCL10, уменьшая воспалительный ответ. Препарат для снижения холестерина — симвастатин, который недавно показали уменьшающим m6A в других тканях, также снижал m6A на РНК IRF7, уменьшал уровень IRF7 в клетках и ослаблял экспрессию генов, связанных с IRF7, в только что полученных биоптатах кишечника пациентов с целиакией, выращенных экс‑виво. Сравнения крупных профилей экспрессии генов показали, что симвастатин сдвигает ткани целиакийных пациентов в сторону профиля, более похожего на таковой у пациентов на безглютеновой диете.
Что это означает для людей с целиакией
Эта работа рисует картину, в которой кишечный вирус и глютен действуют совместно на тонко настроенном уровне РНК‑регуляции. У восприимчивых людей вирусная инфекция, по‑видимому, усиливает пометку m6A на РНК IRF7 в кишечных клетках. Экспозиция глютена затем дополнительно усиливает этот помеченный сигнал, приводя к увеличению количества белка IRF7, более сильной антивирусной тревоге и повышению уровня провоспалительных молекул, которые способствуют аутоиммунной атаке на слизистую кишечника. Понижая метки m6A — генетически или с помощью препарата вроде симвастатина — можно смягчить эту цепную реакцию, по крайней мере в лабораторных и экс‑виво моделях. Для непрофессиональной аудитории ключевое сообщение таково: целиакия — это не только вопрос того, что вы едите, но и то, как инфекции и тонкие химические метки на РНК формируют решение иммунной системы — терпеть или атаковать. Ориентация на эти РНК‑метки в будущем может дополнить безглютеновую диету и вдохновить новые подходы к лечению более широкого круга аутоиммунных заболеваний.
Цитирование: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Ключевые слова: целиакия, метилирование РНК, антивирусный иммунитет, IRF7, симвастатин