Clear Sky Science · ru
CRISPR-AuNP: физико‑химическая оптимизация платформы на основе золотых наночастиц для экономичного и модульного невирусного редактирования генов в ГСКК
Расширение доступа к редактированию генов для большего числа пациентов
Инструменты редактирования генов, такие как CRISPR, уже изменили жизнь людей с наследственными заболеваниями крови, но эти методы остаются дорогостоящими, технически сложными и в основном ограничены несколькими специализированными центрами. В этой работе описан новый способ доставки CRISPR в кроветворные стволовые клетки с помощью маленьких частиц на основе золота, которые можно собрать на лабораторном столе всего за пару часов. Цель — сделать мощные подходы к редактированию генов проще, дешевле и легче внедряемыми в большем числе мест по всему миру.
Почему важны кроветворные стволовые клетки
Клетки крови-порождающие — стволовые и прогениторные клетки — находятся в костном мозге и постоянно пополняют все типы клеток крови в организме. Если врачи смогут безопасно исправить вызывающие заболевание мутации в этих клетках, одноразовая процедура может обеспечить пожизненное излечение при таких состояниях, как серповидноклеточная анемия и некоторые иммунодефициты. В настоящее время наиболее распространённый способ доставки CRISPR в эти клетки — электропорация, процесс, в котором электрические импульсы создают отверстия в мембране клетки. Хотя метод эффективен, электропорация жестко влияет на клетки, требует дорогого оборудования и специализированных реагентов и плохо масштабируется или переносится в условиях с ограниченными ресурсами. Более безопасные вирусные векторы превосходны для многих генотерапий, но они менее пригодны для доставки CRISPR, потому что длительно экспрессируют инструменты редактирования, что повышает риск побочных, внецелевых изменений.
Создание крошечного золотоносителя для доставки
Исследователи поставили цель улучшить ранее описанную систему золотых наночастиц, которая несла компоненты CRISPR на своей поверхности. В ранних вариантах направляющая РНК, ориентирующая белок-разрезатель CRISPR к мишени, напрямую закреплялась на золотом ядре и затем комбинировалась с белком Cas9. Это работало относительно неплохо для одного типа фермента CRISPR, но плохо показало себя с Cas9, ключевым для многих терапевтических стратегий. Тщательно изучив поведение Cas9 и его направляющей РНК в кислых условиях, применявшихся при сборке частиц, команда обнаружила, что дуплекс направляющей РНК становился нестабильным на золотой поверхности, в результате чего к частице прикреплялось мало или вообще не было активного Cas9. Конфокальная микроскопия также показала, что полимерное покрытие, призванное помочь частицам покинуть внутриклеточные отсеки, отслаивалось до того, как могло выполнить свою функцию.
Пошаговый редизайн платформы
Чтобы преодолеть эти проблемы, учёные перестроили систему с нуля в три этапа. Во‑первых, вместо того чтобы закреплять голую РНК на золоте и затем добавлять белок, они формировали полные рибонуклеопротеиновые комплексы CRISPR (белок плюс направляющая РНК) до контакта с золотой поверхностью. Они подобрали слегка кислые условия, которые позволяли этим комплексам связываться с частицами, при этом сохраняя активность белка-разрезателя. Затем они покрыли загруженные частицы специально разработанными полимерами, которые сочетали положительно заряженные цепи — необходимые для выхода из внутриклеточных компартментов — с гибкими гидрофильными сегментами полиэтиленгликоля, предотвращающими агрегацию. По измерениям размера, поверхностного заряда и содержания белка они показали, что позволяют воспроизводимо загружать десятки комплексов CRISPR на частицу, сохраняя при этом стабильность в растворе.
Преодоление клеточных защит
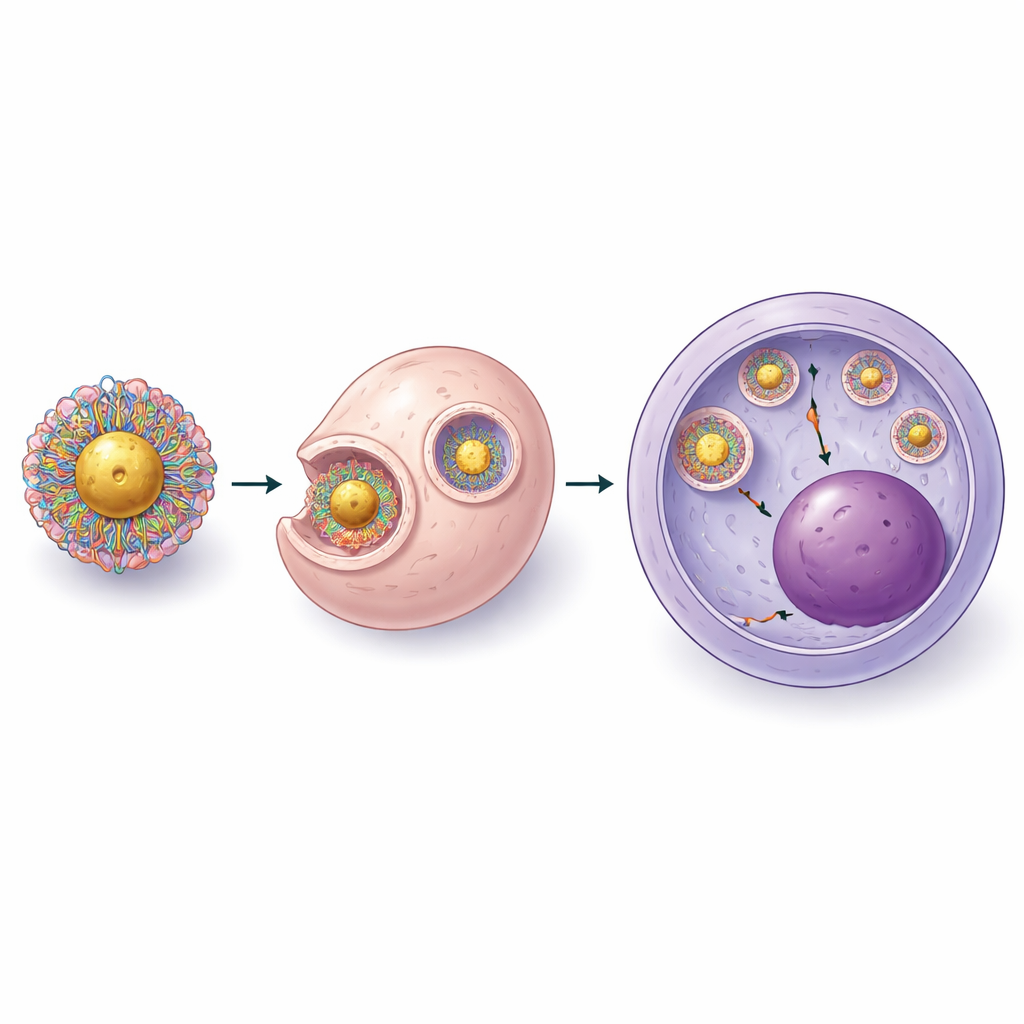
Даже при лучшей загрузке частицы второго поколения по‑прежнему сталкивались с ключевым препятствием: доставить CRISPR из внутриклеточных везикул в ту часть клетки, где находится ДНК. Поэтому команда систематически настраивала химию полимерного слоя и соотношение между положительными группами на полимере и отрицательными группами на комплексе CRISPR. Они обнаружили, что добавление большего количества коротких цепей полиэтиленгликоля и строго контролируемого числа серосодержащих анкеров улучшало как стабильность частиц, так и их способность нарушать мембраны эндосом без вреда для клеток. В финальном, третьем поколении конструкции сначала создавали компактные комплексы CRISPR и полимера, а затем прикрепляли их к концентрированным золотым ядрам. Электронная микроскопия показала тонкую оболочку из CRISPR и полимера вокруг каждой золотой сферы, а визуализация в живых стволовых клетках подтвердила, что груз может выходить в цитоплазму и достигать ядра.
Результаты редактирования с разными инструментами CRISPR
Чтобы оценить эффективность оптимизированных частиц, исследователи нацелились на ген бета‑2‑микроглобулина, который кодирует белок на поверхности почти всех клеток крови и легко измеряется методом проточной цитометрии. Используя платформу третьего поколения на основе золота, они достигли более 10% точных нарушений этого гена в первичных человеческих гемопоэтических стволовых и прогениторных клетках — уровней, считающихся значимыми для многих терапевтических применений — при высоком выживаемости клеток. Хотя эта эффективность ниже, чем у электропорации, золотая система не требовала специализированного оборудования и вызывала минимальный стресс у клеток. Важно, что ту же платформу можно было использовать с разными белками CRISPR, включая Cas9, Cas12a и более новый фермент Cas12a‑M29‑1, при схожих уровнях редактирования и отсутствии обнаруживаемой токсичности, что подчеркивает модульность конструкции.
Что это может означать для будущих терапий
Проще говоря, эта работа показывает, что возможно создать маленький, тщательно сконструированный носитель на основе золота, который доставит инструменты CRISPR в чувствительные кроветворные стволовые клетки без электричества и вирусов, используя доступные материалы стоимостью менее семидесяти долларов на миллион клеток. Хотя для достижения эффективности лучших современных клинических методов, особенно при заболеваниях, требующих очень высокого доли скорректированных клеток, нужны дальнейшие улучшения, эта платформа, собираемая на скамье, снижает практические барьеры для выполнения сложных генетических вмешательств. С продолжением оптимизации и проверок безопасности такие наночастицы могут помочь расширить доступ к преимуществам терапий на основе CRISPR за пределы специализированных центров, делая лечебные методики, потенциально излечивающие, доступнее для пациентов во всём мире.
Цитирование: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Ключевые слова: Редактирование генов CRISPR, золотые наночастицы, гемопоэтические стволовые клетки, невирусная доставка, наномедицина