Clear Sky Science · ru
Переосмысление геномики фасциоскулопулярной дистрофии в эпоху «теломер‑к‑теломере»: подводные камни в скрытом ландшафте повторов D4Z4
Почему эта история о мышечной болезни важна
Фасциоскулопулярная дистрофия (FSHD) — одно из наиболее распространённых наследственных заболеваний с истощением мышц, часто ослабляющее мышцы лица и плеч у в остальном здоровых молодых людей. В течение многих лет учёные обвиняли в этом один фрагмент ДНК возле конца хромосомы 4. Новое исследование показывает, что картина намного сложнее: похожие повторяющиеся последовательности разбросаны по всему геному, и многие обычные лабораторные тесты не в состоянии их различить. Понимание этого скрытого ландшафта важно для точной диагностики, качественных исследований и в итоге для безопасности терапий.
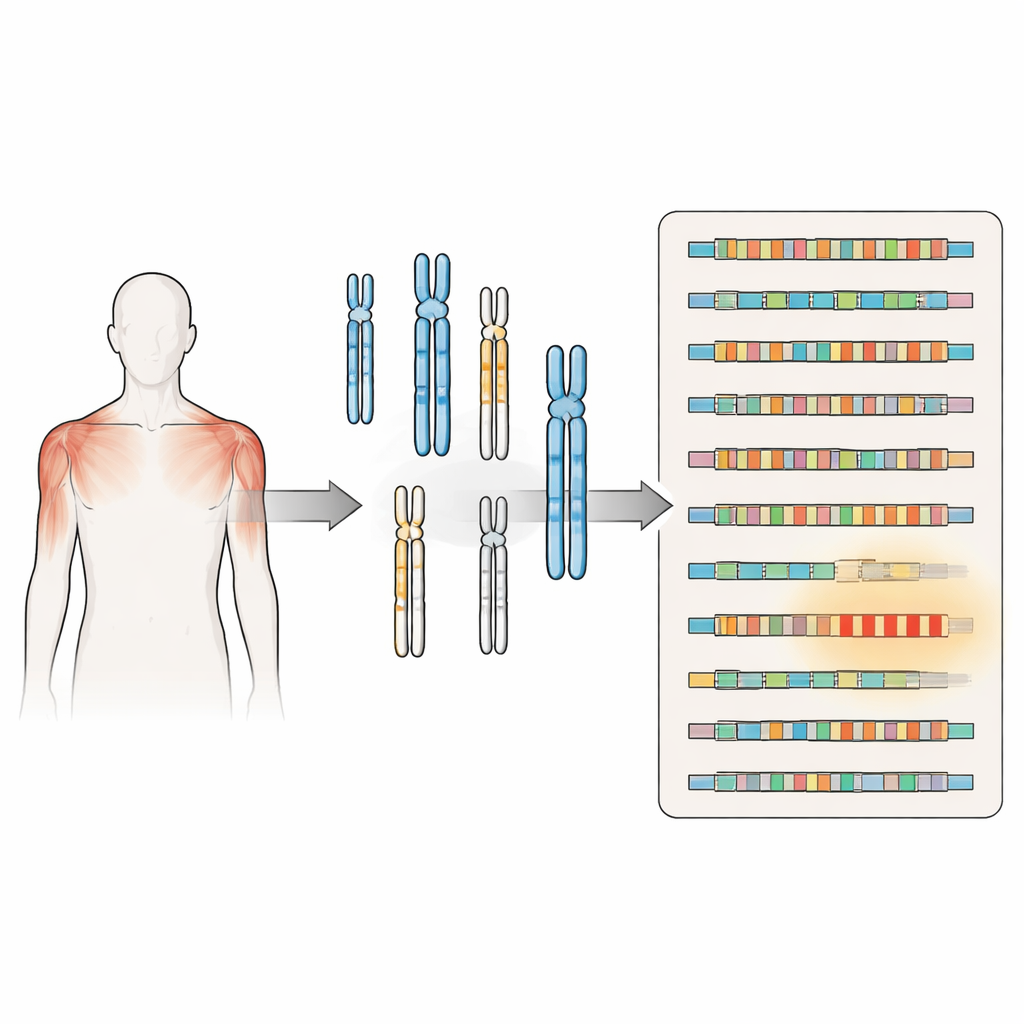
Более пристальный взгляд на запутанное мышечное заболевание
FSHD долгое время связывали с укорочением повторяющейся последовательности ДНК, называемой D4Z4, близ концов хромосомы 4. Когда этот участок повторов сокращается ниже определённого размера и находится на специфическом генетическом фоне, это позволяет синтезироваться белку DUX4, который может повреждать мышечные клетки. Второй вариант болезни возникает, когда мутированы гены, которые обычно удерживают этот регион в плотном, неактивном состоянии, что также приводит к появлению DUX4. Оба пути сходятся в одной проблеме: ген, который в норме должен быть почти выключен в зрелой мышце, становится эпизодически активным и способствует слабости и атрофии мышц.
Скрытые повторы по всему геному
Ранние карты человеческого генома были неполными, особенно в областях, богатых повторяющимися последовательностями у концов хромосом и около центромер. Используя новую сборку человеческого генома «от теломера до теломера», которая заполнила эти пробелы, авторы заново просканировали весь геном, используя последовательность D4Z4 с хромосомы 4 в качестве шаблона. Они обнаружили кластеры и изолированные копии D4Z4‑подобных повторов как минимум на десяти дополнительных хромосомах. Некоторые из этих повторов структурно полные и расположены рядом с элементами, которые могли бы стабилизировать РНК, похожие на DUX4, что подразумевает возможность производства родственных белков или РНК при определённых условиях.
Когда лабораторные тесты видят сразу несколько мест
Исследования FSHD и диагностика часто опираются на тесты, которые амплифицируют определённые фрагменты ДНК или РНК с помощью коротких праймеров — стратегия, известная как ПЦР. Эти праймеры изначально проектировались при предположении, что повторы D4Z4 существуют только на хромосомах 4 и 10. Комбинируя компьютерные прогнозы с экспериментами на клетках, несущих отдельные человеческие хромосомы, авторы показывают, что многие широко используемые наборы праймеров связываются не только с заболевшим участком на хромосоме 4, но и с похожими повторами, разбросанными по всему геному. Праймеры, нацеленные на основной экзон DUX4 или на соседние длинные некодирующие РНК, часто амплифицируют продукты сразу с нескольких хромосом, что делает невозможным определить, откуда именно пришёл тот или иной сигнал.
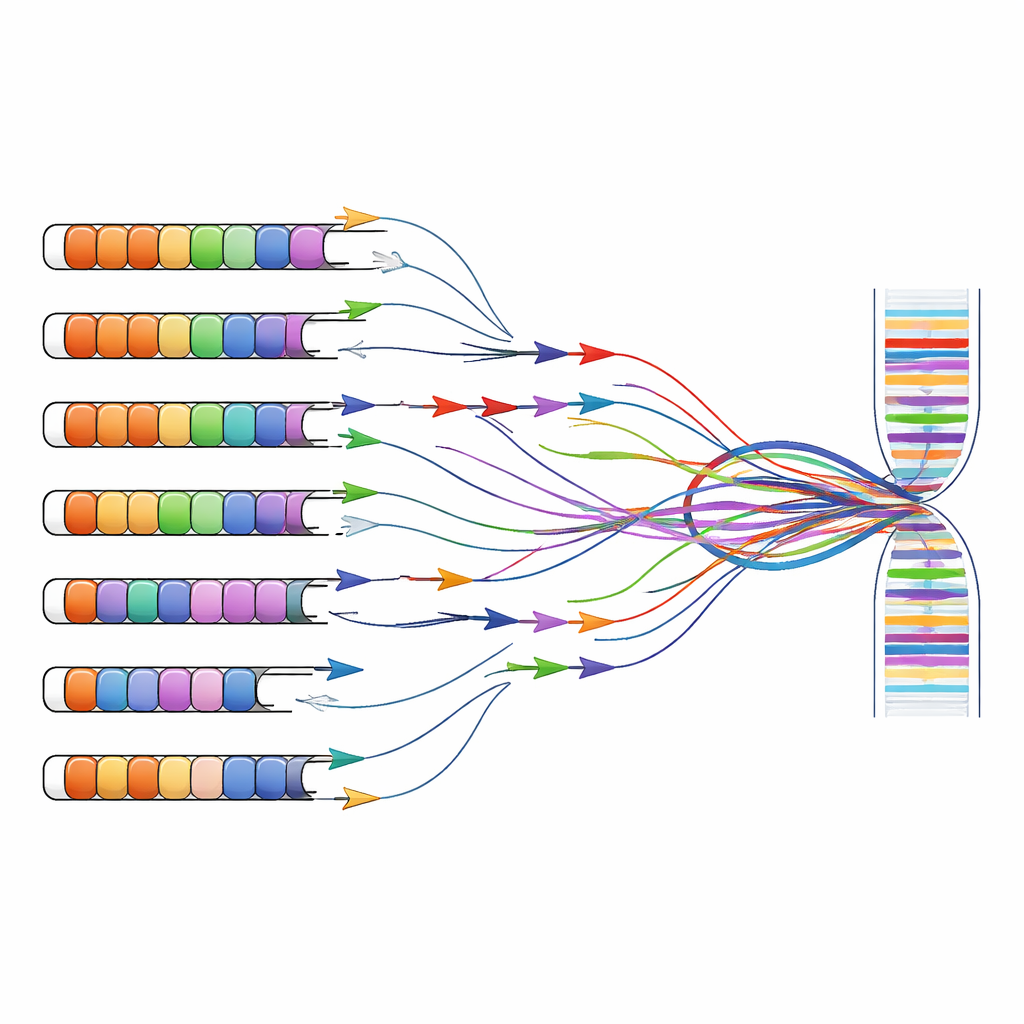
Переосмысление диагностических и исследовательских инструментов
Эта проблема множественных локусов выходит за рамки фундаментальных исследований и касается клиники. Новые тесты, измеряющие метилирование ДНК (химическую отметку, связанную с приглушением генов) или использующие короткие рид‑секвенирования, часто сводят сигналы от многих почти идентичных повторов в единое целое. В результате измерения «метилирования D4Z4» или «транскриптов DUX4» в общедоступных наборах данных могут на самом деле отражать смесь вкладов с хромосомы 4, хромосомы 10 и других участков. Авторы утверждают, что чтобы корректно связывать генетические изменения с симптомами, учёным теперь необходимо применять методы, учитывающие повторы и различающие отдельные локусы — например, длинно-ридное секвенирование, которое может покрыть целые блоки повторов и зафиксировать их профиль метилирования и РНК‑продукты полностью.
Что это значит для пациентов и будущих терапий
Исследование не отменяет центральную роль укороченного региона D4Z4 на хромосоме 4 в FSHD, но показывает, что этот участок находится в густонаселённом «соседстве» похожих последовательностей. Сигналы, которые когда‑то считали доказательством активности именно в локусе болезни, могут частично происходить от его геномных «родственников». Для пациентов это означает, что наиболее надёжные диагностические методы — те, которые физически разрешают, какая именно хромосома и массив повторов вовлечены, а не полагаются исключительно на косвенные показатели. Для исследователей и разработчиков лекарств это подчёркивает необходимость высокоспецифичных конструкций, которые не будут случайно поражать безвредные повторы в других местах генома. В эпоху «теломер‑к‑теломере» понимание и лечение FSHD будут зависеть от обзора всего ландшафта повторов, а не только одного ориентира.
Цитирование: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Ключевые слова: фасциоскулопулярная дистрофия, повторы D4Z4, DUX4, геном от теломера до теломера, генетическая диагностика