Clear Sky Science · ru
Борьба с купроптозом: от перепрограммирования метаболизма к терапевтической эксплуатации в онкологии
Когда полезный металл обращается против рака
Медь известна прежде всего как материал для проводки и сантехники, но она также тихо циркулирует в наших клетках, помогая ферментам вырабатывать энергию и защищать нас от повреждений. В этом обзорном материале рассматривается неожиданный поворот: при определённых условиях избыток меди может заставить раковые клетки вступить в особый вид гибели. Понимание этого процесса — называемого «купроптозом» — может открыть новые пути лечения опухолей, которые ускользают от стандартных терапий.
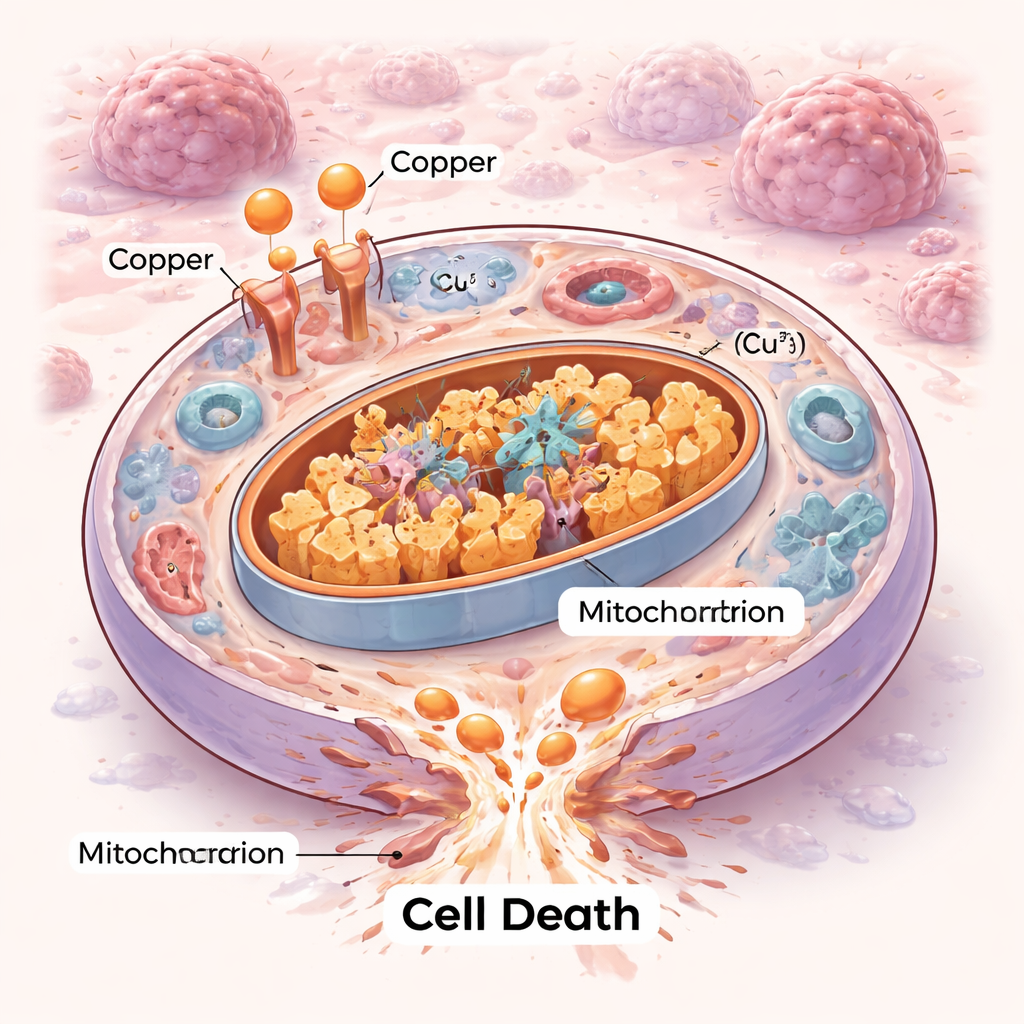
Новый путь клеточной гибели
Клетки умирают не одинаково. На протяжении десятилетий учёные описывали упорядоченные программы самоуничтожения, такие как апоптоз, и более новые формы, например ферроптоз. Купроптоз добавляет новую главу. В этом случае избыток меди заливает энергетические станции клетки — митохондрии — и связывается со специфическими метаболическими ферментами, которые обычно помогают сжигать топливо. Такое связывание приводит к слипанию этих ферментов и дестабилизации малых железосерных компонентов, необходимых митохондриям для работы. В результате возникает своего рода внутренняя пробка и механический сбой, которые клетка не может исправить, что приводит к гибели от протеотоксического стресса, а не по классическим путям «самоубийства».
Как раковые клетки контролируют медь и энергию
Поскольку медь одновременно необходима и потенциально опасна, клетки поддерживают сложную логистическую сеть для её безопасного перемещения. Специальные транспортеры вносят медь в клетку, шапероны сопроводжают её к митохондриям и другим пунктам назначения, а молекулы‑депо, такие как металлотионеины и глутатион, поглощают излишки. Опухоли часто перенастраивают эту систему. Некоторые усиливают импортеры или шапероны, чтобы подпитывать высокий энергетический спрос; другие увеличивают экспортеры или белки‑хранилища, чтобы избежать перегрузки медью. Одновременно многие раки меняют свой метаболизм — переключаясь между сжиганием сахаров у поверхности клетки и глубинным митохондриальным дыханием. В обзоре показано, что купроптоз сильнее всего поражает клетки, которые всё ещё сильно зависят от митохондрий, делая опухоли с таким метаболическим профилем особенно уязвимыми.
Главные переключатели, регулирующие чувствительность к меди
Крупные клеточные «принимающие решения» влияют на вероятность наступления купроптоза. Так, супрессор опухолей p53, как правило, отталкивает клетки от быстрого ферментативного брожения сахаров в пользу более упорядоченного митохондриального использования топлива. Делая это и изменяя обращение с медесвязывающими ферментами, p53 может сделать рак более чувствительным к меди, тогда как мутантные формы p53 часто действуют в обратном направлении. Напротив, фактор гипоксии HIF‑1α, активируемый в плохо оксигенированных участках опухоли, помогает клеткам избежать купроптоза, понижая ключевые митохондриальные ферменты и усиливая медесвязывающие щиты. Другие пути, такие как Wnt/β‑катенин и AKT, способствуют резистентности, стимулируя вывоз меди или химически модифицируя важные белки так, чтобы они менее реагировали на перегрузку медью. В совокупности эти сети работают как термостаты, повышая или понижая чувствительность опухоли к терапии, основанной на меди.
Медь, иммунная система и умная доставка препаратов
Роль меди не ограничивается прямым уничтожением раковых клеток; она также формирует иммунную среду вокруг опухолей. Контролируемый медный стресс может сделать умирающие клетки более «заметными», высвобождая сигналы опасности, которые привлекают и активируют Т‑клетки, дендритные клетки и макрофаги. Медь также может влиять на уровни иммунных чекпойнтов, таких как PD‑L1, которыми опухоли пользуются, чтобы выключать противоопухолевые Т‑клетки, что открывает возможности для сочетания препаратов, нацеленных на медь, с современными иммунотерапиями. Поскольку свободная медь может повредить здоровые ткани, исследователи создают точные инструменты — малые молекулы‑ионофоры, которые направляют медь избирательно в раковые клетки, и наномедицинские платформы, упаковывающие медь или медиактивируемые лекарства внутри таргетированных частиц или гидрогелей. Эти технологии нацелены на увеличение уровня меди до летальных концентраций внутри опухолей при сохранении безопасных уровней в остальном организме.
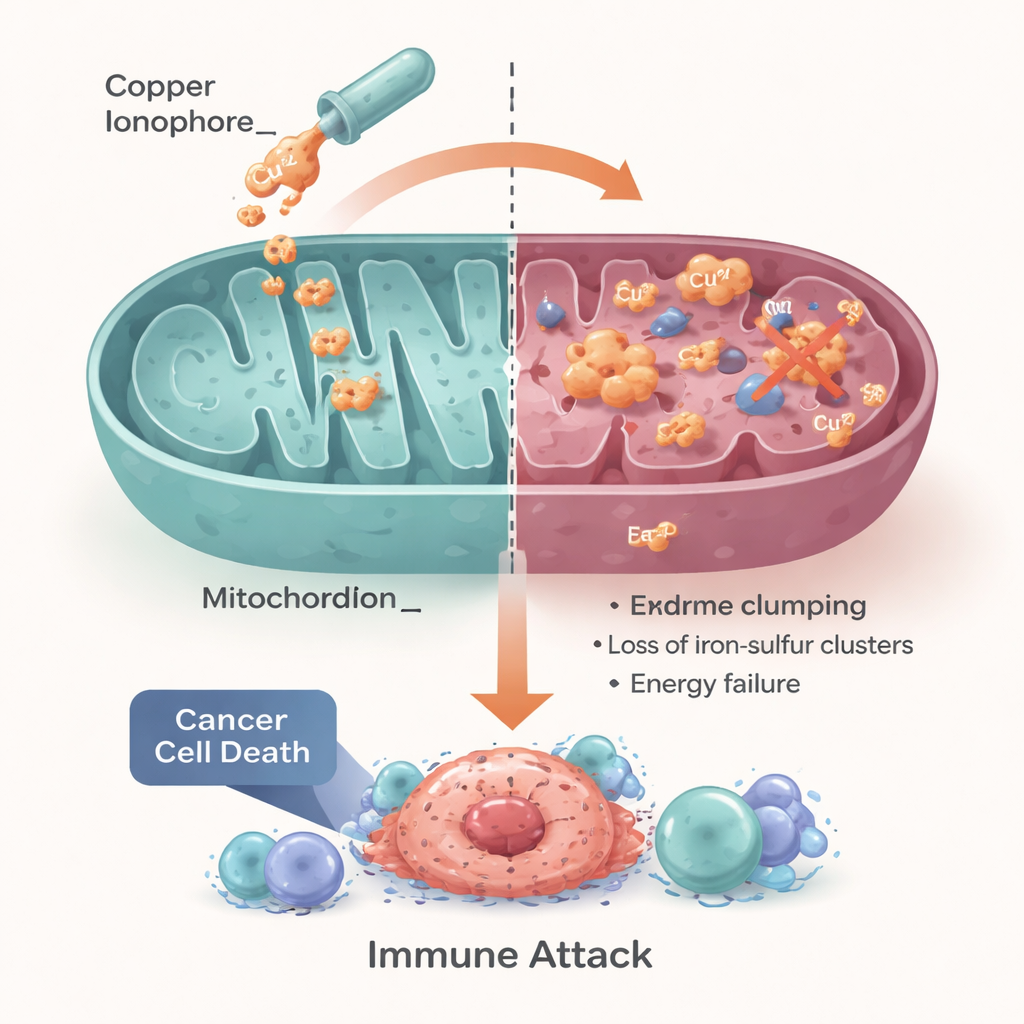
Преобразование клеточной уязвимости в лечение
Авторы заключают, что купроптоз превращает базовую потребность клетки — бережное управление медью и энергией — в потенциальную ахиллесову пяту рака. Опухоли с нарушенным обращением с медью или с чрезмерной зависимостью от митохондриального метаболизма могут быть особенно чувствительны к стратегиям на основе меди, включая перепрофилированные препараты, такие как дисульфирам и элескломол, а также препараты следующего поколения на основе наночастиц. В то же время они подчёркивают, что успех будет зависеть от точного подбора пациентов под конкретный подход, с использованием биомаркеров, которые отражают статус транспортеров меди, митохондриальную активность и иммунный и кислородный статус опухоли. Если эти препятствия удастся преодолеть, использование купроптоза может дать онкологам новый, питаемый металлом рычаг для лечения опухолей, для которых в настоящее время мало эффективных вариантов.
Цитирование: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Ключевые слова: купроптоз, метаболизм меди, терапия рака, метаболизм опухоли, иммунотерапия рака