Clear Sky Science · ru
Транзитная механическая активация канала Piezo1 облегчает экс-виво расширение гемопоэтических стволовых клеток
Производство большего числа жизненно важных кроветворных стволовых клеток
Трансплантации костного мозга могут излечить некоторые онкологические заболевания крови и наследственные нарушения, но врачи часто ограничены тем, насколько мало истинных кроветворных стволовых клеток удаётся получить от донора. В этом исследовании показан неожиданный способ выращивать эти редкие клетки вне организма, мягко «касаясь» их крошечными пластиковыми шариками, которые стимулируют механический датчик на их поверхности. Работа предлагает новый, потенциально более безопасный путь получения достаточного числа стволовых клеток, чтобы больше пациентов могли получить пользу от трансплантации.
Почему так сложно вырастить кроветворные стволовые клетки
Кроветворные стволовые клетки находятся глубоко внутри костей и на протяжении жизни незаметно обеспечивают нас эритроцитами, лейкоцитами и тромбоцитами. Трансплантация этих клеток может восстановить повреждённую систему крови, например при лечении лейкемии, но только если доступно достаточно здоровых стволовых клеток и они сохраняют свою полноценную функцию. Попытки расширить их в культуре часто не дают результата: клетки либо перестают самоподдерживаться, либо утрачивают долгосрочную способность восстанавливать систему крови. Большинство современных методов опираются на смеси факторов роста и генетические модификации, но они не воссоздают полностью сложную физическую среду костного мозга, где стволовые клетки постоянно испытывают толчки, растяжение и давление.
Скрытый механический переключатель на стволовых клетках
Исследователи сосредоточились на белке Piezo1 — крошечном канале в мембране клетки, который открывается при изгибе или растяжении мембраны, пропуская ионы кальция и запускающий внутриклеточные сигналы. При изучении множества типов кровяных клеток они обнаружили, что Piezo1 особенно богат в истинных кроветворных стволовых клетках. Когда Piezo1 удаляли генетически или блокировали лекарством, стволовые клетки, выращенные в культурах, больше не могли эффективно расширяться или восстанавливать кровоток у мышей после трансплантации. Интересно, что постоянная стимуляция Piezo1 химическими активаторами также была вредной: клетки накапливали избыточный кальций, производили вредные реактивные молекулы и хуже приживались. Эти результаты указывали на то, что стволовым клеткам нужна кратковременная, правильно рассчитанная механическая активация Piezo1, а не постоянное химическое воздействие.
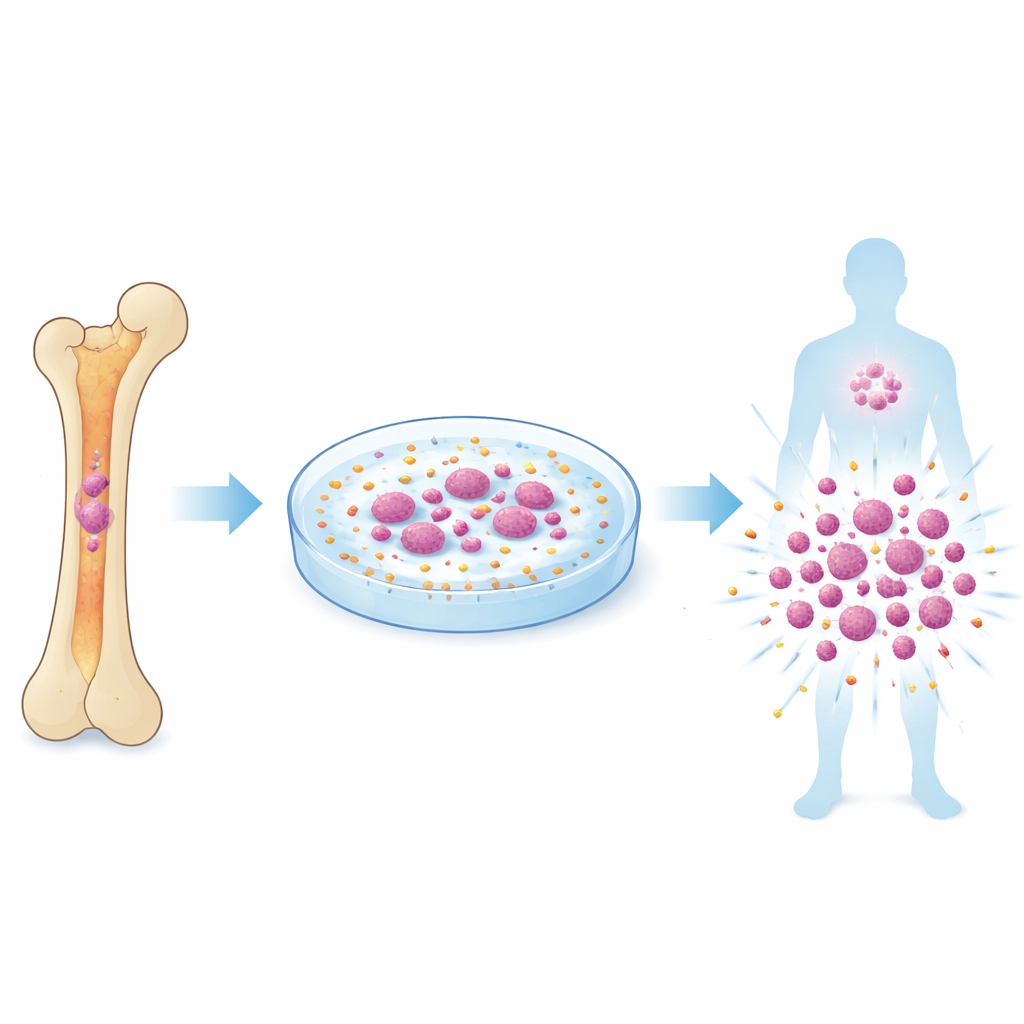
Использование крошечных шариков для нажатия на датчик
Чтобы обеспечить именно тот механический толчок, который нужен, команда обратилась к микроскопическим полимерным сферам — по сути гладким пластиковым шарикам, которые могли слегка сталкиваться со стволовыми клетками в культуре. Они тестировали шарики разного размера и жёсткости и обнаружили, что полистироловые сферы диаметром 500 нанометров — названные PS500 — оказались исключительно эффективными. Когда костный мозг мышей выращивали вместе с такими шариками, число стволовых клеток резко увеличивалось, и эти клетки сохраняли сильную долгосрочную способность к восстановлению крови при последовательных пересадках через несколько поколений мышей. Тщательная визуализация и механические измерения показали, что шарики многократно вдавливают мембрану стволовой клетки с крошечными силами, достаточными для открытия каналов Piezo1 в короткие промежутки времени, но без перегрузки клеток.
От механического прикосновения к сигнальным путям роста
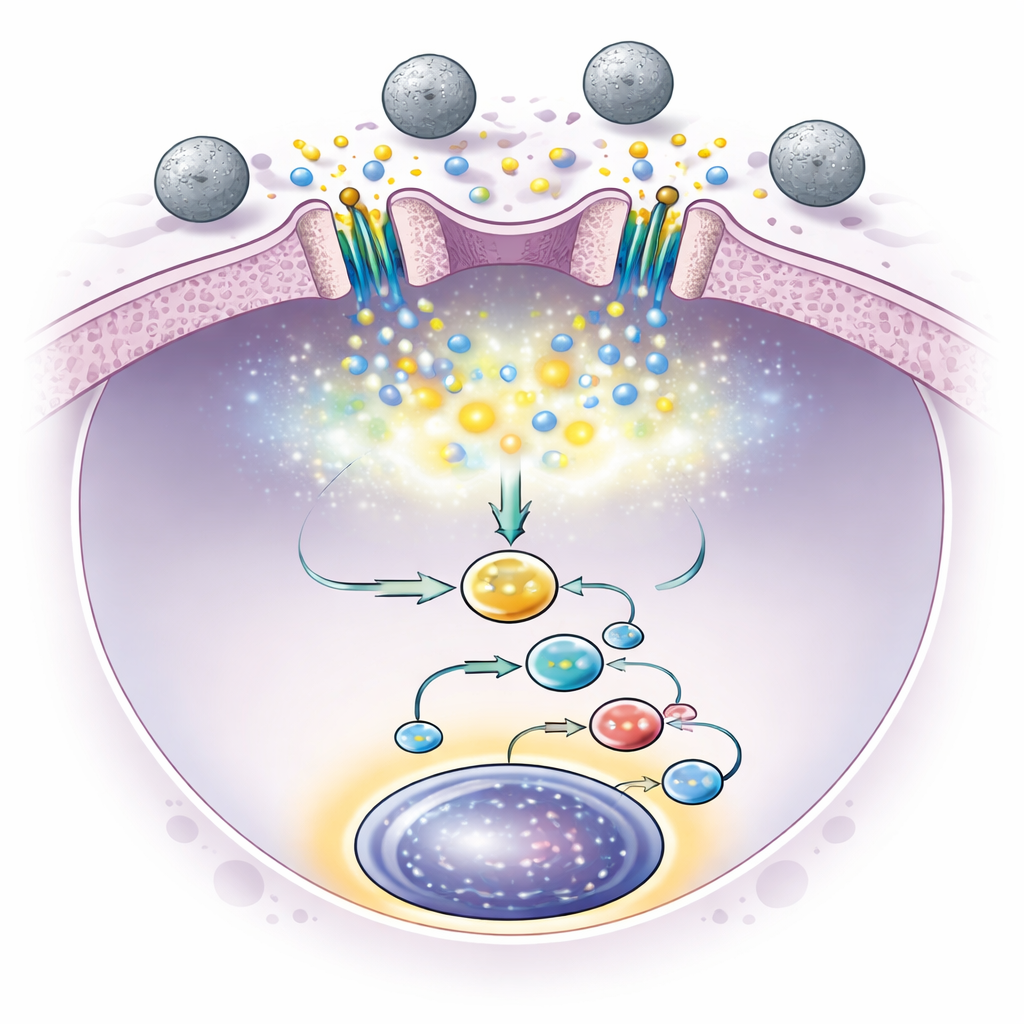
Кратковременное открытие каналов Piezo1 вызывало небольшие всплески поступления кальция в стволовые клетки. Это, в свою очередь, активировало внутриклеточные пути, побуждавшие клетки производить определённые сигнальные белки, в частности фактор роста интерлейкин‑6. Интерлейкин‑6 затем действовал обратно на стволовые клетки и активировал белок Stat3 в их ядрах, который известен поддержкой выживания и самоподдержания стволовых клеток. Когда исследователи блокировали путь Stat3, благоприятный эффект шариков исчезал, что подтвердило, что эта цепочка событий — механическое прикосновение, всплеск кальция, высвобождение интерлейкина‑6 и активация Stat3 — была ключевой для расширения. Важно, что после лишь короткого периода воздействия шариков сигнализация оставалась активной, и число стволовых клеток продолжало расти, что подчёркивает: постоянная стимуляция не требовалась.
Перспективы для человеческих трансплантаций
Далее команда применила тот же подход к человеческим кроветворным стволовым клеткам, полученным из пуповинной крови — распространённого, но часто ограниченного источника для трансплантации. С шариками PS500 эти человеческие клетки расширялись в несколько раз больше, чем только при ведущих методах с малыми молекулами, при этом сохраняли способность постоянно восстанавливать кроветворение у иммунодефицитных мышей. Исследования безопасности на мышах показали, что шарики не проникают в стволовые клетки, их можно эффективно удалить простой центрифугой или фильтрацией, и при протестированных дозах они не вызывают заметного повреждения органов или нарушений крови. Это позиционирует систему на основе шариков как практичную и потенциально масштабируемую технологию для банков крови и центров трансплантации.
Что это может означать для пациентов
По сути, исследование показывает, что мягкий механический сигнал — доставляемый дрейфующими наномасштабными шариками — может побудить кроветворные стволовые клетки размножаться, сохраняя их потенциал, за счёт кратковременной активации встроенного датчика давления, а не его перегрузки. Если это будет перенесено в клинику, подход может упростить получение достаточного числа качественных стволовых клеток из небольшой единицы пуповинной крови или частичного донора, расширив доступ к излечивающим трансплантациям для многих людей. Это также подчёркивает, что внимание следует уделять не только химической «среде» вокруг клеток, но и физическим ощущениям, которые они испытывают, — это может открыть новые способы управления судьбой клеток.
Цитирование: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
Ключевые слова: гемопоэтические стволовые клетки, механочувствительные ионные каналы, Piezo1, микросферы из полистирола, трансплантация стволовых клеток