Clear Sky Science · ru
Интегративный конвейер пространственного профилирования для определения архитектуры ТМЭ в архивных клинических образцах с использованием суперплекс-технологии CmTSA
Почему скрытый ландшафт вокруг опухолей имеет значение
Опухоли не растут в изоляции. Их окружает оживлённый «район» из иммунных клеток, клеток‑сопровождения, кровеносных сосудов и рубцовой ткани, которые вместе формируют «микроокружение» опухоли. В этой статье предложен практический способ детально картировать этот скрытый ландшафт на основе стандартных госпитальных образцов ткани. Показывая, какие типы клеток находятся рядом друг с другом и как они организуются в полезные или вредоносные сообщества, метод может помочь врачам лучше предсказывать поведение рака у пациента и выбирать наиболее эффективные методы лечения.
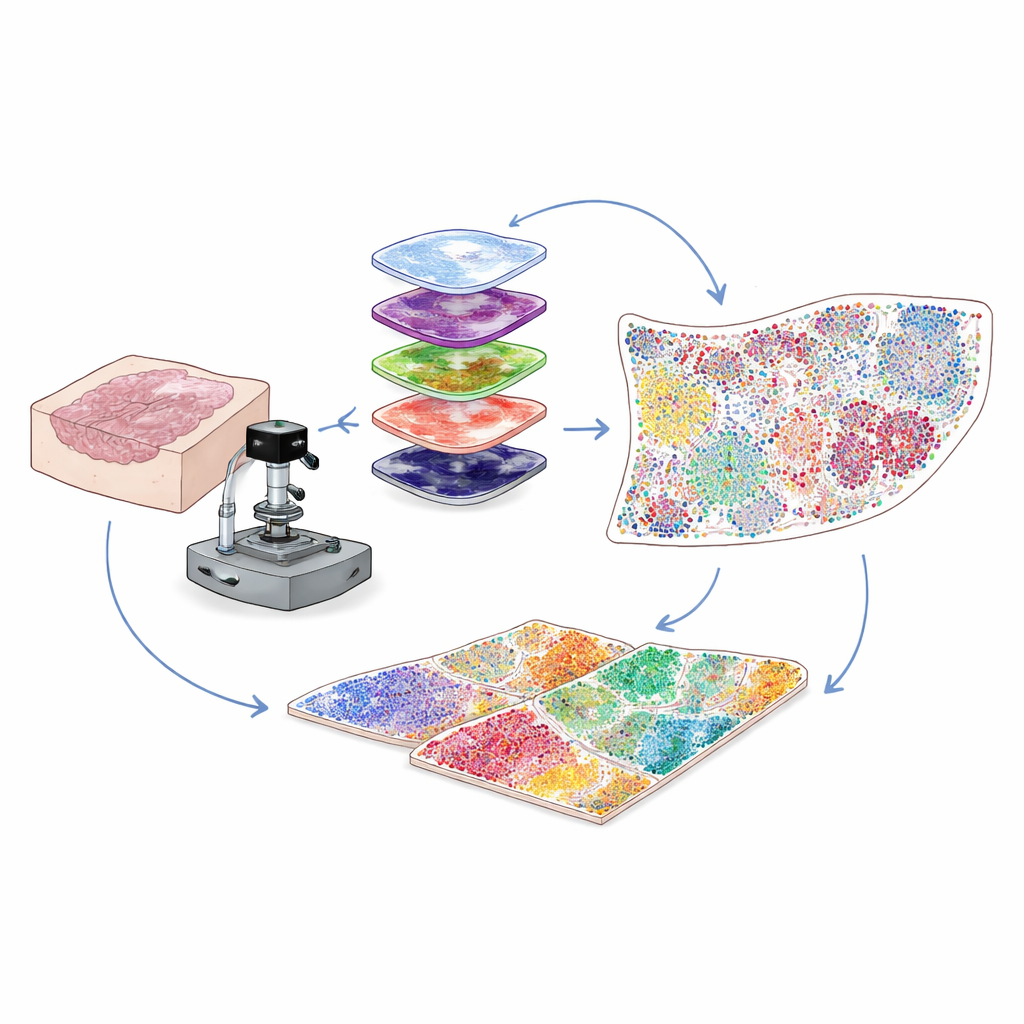
Увидеть больше в обычных госпитальных образцах
Большинство клинических онкологических образцов хранится в виде тонких срезов парафиновых блоков, известных как FFPE, которые можно сохранять годами. Это кладезь для исследований, но техническая проблема мешала учёным: такие образцы дают собственную фонную флуоресценцию, которая заглушает слабые сигналы многих важных белков. Авторы решили эту проблему, комбинировав интенсивное, точно настроенное освещение с мягкой химической обработкой, чтобы выборочно стереть фон без повреждения ткани или мишеней‑белков. Этот гибридный оптическо‑химический шаг «бликования» резко повышает чёткость изображений, позволяя обнаруживать слабые белковые сигналы, которые в противном случае были бы утеряны.
Окрашивание десятков белковых меток на одном и том же срезе
Чтобы понять, какие клетки присутствуют и чем они занимаются, учёные окрашивают ткани антителами, связывающими конкретные белки. Традиционные мультиплексные методы либо испытывают трудности при низкой интенсивности сигнала для редких белков, либо позволяют отслеживать ограниченное количество маркеров за раз. Здесь команда использует подход, называемый циклическим усилением сигнала тирамидом (cyclic tyramide signal amplification). В каждом цикле небольшой набор маркеров окрашивается и ферментативно «проявляется» в яркие, прочно связанные флуоресцентные точки. Антитела затем мягко удаляются, сигнал остаётся, фон снова бликуется, и добавляют следующий набор маркеров. Повторяя этот цикл многократно и выравнивая изображения по постоянному сигналу из ядер клеток, можно надёжно визуализировать 30–60 различных белков на одном срезе ткани по всему предметному стеклу с разрешением на уровне одиночных клеток.
Преобразование цветных изображений в атлас «клетка за клеткой»
Изображения с высокой мультиплексностью содержат миллионы пикселей, намного больше, чем способен проанализировать человек невооружённым глазом. Поэтому авторы создают конвейер компьютерного зрения, который сначала находит и обводит каждое ядро клетки с помощью инструментов глубокого обучения, изначально разработанных для общей сегментации клеток. Затем, исходя из того, где проявляется флуоресценция каждого белка — на мембране, в цитоплазме или в ядре — и на основании набора логических правил, каждой клетке присваивают тип или подтип, например опухолевая клетка, вспомогательная Т‑клетка, цитотоксическая Т‑клетка, В‑клетка, фибробласт и другие. На выходе получается цифровая таблица, где для каждой клетки на слайде указаны её тождественность и точные координаты. Это превращает сложное изображение в количественную карту того, кто и где находится в микросреде опухоли.
Выявление клеточных «соседств», формирующих исход
Клетки редко действуют в одиночку; важно, кто у них по соседству. Чтобы это захватить, исследователи тестируют разные способы определения локальных соседств вокруг каждой клетки и останавливаются на подходе на основе радиуса. Представьте, что вокруг каждой клетки рисуется маленький круг — примерно толщиной с человеческий волос — и в нём перечисляют, кто в него входит. Группируя клетки, окружные круги которых имеют схожие сочетания соседей, метод выделяет повторяющиеся «функциональные ниши», например зоны, богатые иммунными клетками, барьеры с преобладанием фибробластов или участки, доминируемые опухолью. Применение этой стратегии к тканям толстой кишки показывает, что радиусный подход лучше согласуется с известными анатомическими структурами, чем альтернативные методы. В образцах рака шейки матки от пациентов с хорошим и плохим исходом команда обнаруживает, что нишы, богатые иммунными клетками, скапливаются у края опухоли у пациентов с благоприятным прогнозом, тогда как у пациентов с худшим исходом выявляются плотные, богатые фибробластами зоны, окружающие опухолевые клетки и, по‑видимому, изолирующие атакующие иммунные клетки.
От пространственных карт к персонализированному лечению
Комбинируя качественное и доступное окрашивание множества белков с надёжным анализом изображений, эта работа представляет сквозной конвейер, применимый к большому числу стандартных госпитальных образцов. Метод превращает сохранённую ткань в подробные карты того, как опухолевые, иммунные и стромальные клетки располагаются и взаимодействуют. Для широкой аудитории вывод заключается в том, что важно не только какие клетки присутствуют, но и их точные соседские паттерны — это влияет на поведение рака. Эта платформа может помочь исследователям выявлять защитные иммунные очаги, определять супрессивные клеточные барьеры и, в конечном счёте, поддержать более точную прогностику и более тонко настроенные стратегии иммунотерапии.
Цитирование: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Ключевые слова: микроокружение опухоли, пространственная протеомика, мультиплексная визуализация, иммунология рака, анализ на уровне одиночных клеток