Clear Sky Science · ru
Хронобиология нейротропных вирусов: ритмичный вход вирусов и аритмичные часы хозяина
Почему время имеет значение при инфекциях мозга
Многие опасные вирусы, включая вирус бешенства и герпесвирусы, обладают способностью поражать головной мозг и нервную систему. В этом исследовании задают на первый взгляд простой, но важный вопрос: влияет ли время суток на то, как легко эти «нейротропные» вирусы проникают в нашу нервную систему, и могут ли сами вирусы нарушать наши внутренние часы? Понимание этого двустороннего диалога между биологическими часами и вирусами может открыть новые возможности для того, чтобы оптимально назначать вакцины, противовирусные препараты и корректировать сменную работу для снижения риска.
Ежедневные биологические часы и «дверные ручки» вирусов
Практически каждая клетка организма оснащена внутренней 24‑часовой системой отсчёта, обычно называемой циркадными часами. Её задают набор основных часовых белков, в том числе BMAL1 и REV-ERBα, которые включают и выключают тысячи генов в ритмических волнах. Авторы сосредоточились на «ручках дверей», которыми вирусы пользуются для проникновения в клетки — белках‑рецепторах на поверхности клеток — для десятков вирусов, ориентированных на мозг или проникающих в него. Исследуя мозгоподобные органоиды, выращенные из стволовых клеток, нервные клеточные линии и ткани мышей, они обнаружили, что большинство этих вирусных рецепторов поднимаются и падают в течение дня. Эти ритмы тесно коррелировали с активностью компонентов часов, что свидетельствует о том, что наша суточная система управления тихо контролирует, сколько точек входа для вирусов доступно в любой конкретный час.
Фактор клеточного цикла становится посредником часов
Углубляясь, исследователи спросили, как белок, обычно связанный с контролем деления клетки и называемый E2F8, вписывается в эту сеть времени. Они обнаружили, что сам E2F8 находится под циркадным контролем и действует как ретранслятор между часами и по крайней мере одним ключевым рецептором бешенства, p75NTR. Когда активен часовой белок REV-ERBα, он подавляет E2F8. В свою очередь, низкий уровень E2F8 снимает тормоз с гена p75NTR, что позволяет синтезировать больше этого рецептора и делает клетки более восприимчивыми к вирусу бешенства. Примечательно, что E2F8 также оказывает обратную связь на часы: он может непосредственно связываться с регуляторными участками основных часовых генов, таких как REV-ERBα и PER2, и ослаблять их активность. Это создаёт петлю обратной связи, в которой регулятор клеточного цикла помогает формировать суточные ритмы и, через них, уязвимость нервных клеток к инфекции.
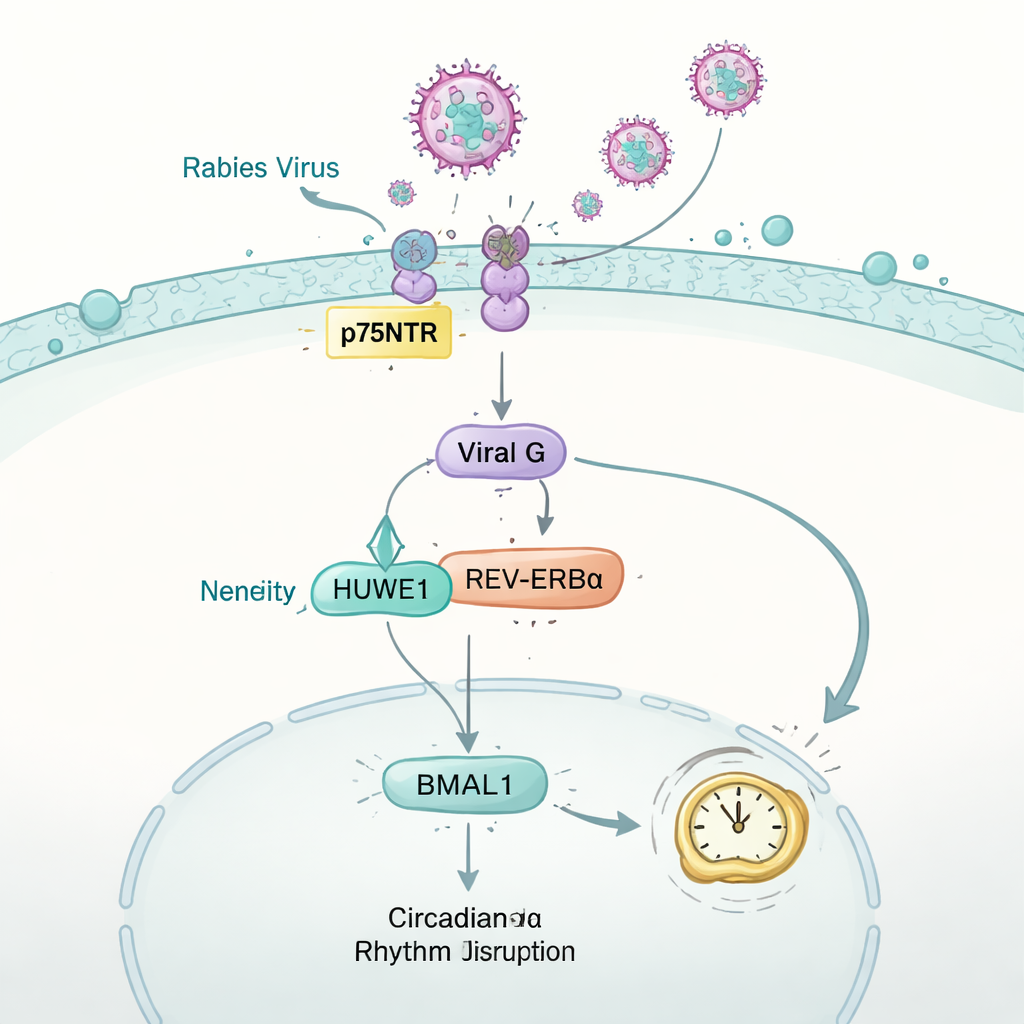
Как вирус бешенства сбивает часы с ритма
Далее учёные перевернули вопрос: может ли вирус давать ответ часам? На мышах, инфицированных вирусом бешенства, команда мониторила активность бега в колесе, обмен веществ и газообмен. Несмотря на нормальное потребление пищи на ранних этапах инфекции, животные постепенно теряли привычные суточные колебания активности, характерные для здоровых мышей. В мозге и ряде других органов уровень критически важного часового белка BMAL1 резко снижался. В нервоподобных клетках этот эффект можно было проследить до гликопротеина «G» вируса бешенства — поверхностного белка, который обычно помогает вирусу сливаться с клетками. G перехватывал клеточный фермент HUWE1, который обычно метит для утилизации другой часовой белок, REV-ERBα. Соперничая за HUWE1, вирусный белок G стабилизировал REV-ERBα, что приводило к дополнительному подавлению BMAL1 и, в конечном итоге, к нарушению часового механизма, поддерживающего суточный порядок физиологии.
Время, джетлаг и тяжесть инфекции
Чтобы проверить, важны ли эти молекулярные изменения для целого организма, команда инфицировала мышей бешенством в разное время суток, при обычном чередовании света и темноты, при хронических условиях «джетлага», а также у животных, генетически лишённых REV-ERBα. Мыши, инфицированные в начале своей активной (ночной) фазы, когда уровень рецептора p75NTR достигает пика, быстрее теряли вес, имели более высокие вирусные нагрузки в нескольких регионах мозга, сильнее выраженное воспаление мозга и умирали быстрее, чем мыши, инфицированные в начале фазы покоя. Мыши, подвергнутые повторным сдвигам фаз, имитирующим ротацию сменной работы, теряли нормальные ритмы часов в мозге, демонстрировали постоянно повышенные уровни p75NTR, имели ослабленные базовые противовирусные сигналы и страдали от более тяжёлого течения болезни. Напротив, мыши без REV-ERBα экспрессировали меньше p75NTR, несли меньшие вирусные нагрузки и дольше выживали после инфекции, что указывает на то, что этот компонент часов является критическим «привратником» тяжести бешенства.
Что это значит для людей
Проще говоря, исследование показывает, что наши внутренние часы не только задают время сна; они также открывают и закрывают молекулярные входы, которыми пользуются вирусы, вторгающиеся в мозг, а те же вирусы могут ответить, спутывая часы. Один фактор, REV-ERBα, занимает ключевой узел: вместе с E2F8 он формирует и уровни рецепторов, и суточную динамику, в то время как вирус бешенства манипулирует им в собственных интересах. Эти выводы указывают на практические пути. Вакцины или противовирусные препараты могут работать эффективнее в определённое время суток, когда рецепторы находятся в минимуме или иммунные ответы максимально сильны. Люди с хронически нарушенными ритмами — например, сменные рабочие или частые путешественники — могут подвергаться повышенному риску некоторых нейротропных инфекций. Мишени типа REV-ERBα или родственные пути могут помочь склонить чашу весов в пользу хозяина, делая инфекции менее тяжёлыми и улучшая исходы.
Цитирование: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Ключевые слова: циркадные часы, нейротропные вирусы, бешенство, вирусные рецепторы, хронотерапия