Clear Sky Science · ru
Динамические изменения иммунной микроокружения при раке яичников после неоадъювантной химиотерапии
Почему это исследование важно для женщин с раком яичников
Поздние стадии рака яичников часто лечат сильной химиотерапией до или после операции, но у многих женщин болезнь всё равно возвращается и перестаёт отвечать на препараты. В этом исследовании поставлен актуальный вопрос: как химиотерапия незаметно перестраивает собственную защиту организма вокруг опухоли и можно ли скорректировать эту реакцию, чтобы продлить эффективность лечения? Анализируя отдельные клетки и испытывая новые комбинации препаратов на мышах, исследователи выявили скрытую роль жироподобных гормоноподобных молекул — простагландинов — в помощи опухолям ускользать от иммунной системы после химиотерапии.
Меняющееся поле битвы вокруг опухоли
Опухоли яичников не растут в изоляции: они находятся в плотно населённом «районе» иммунных клеток, соединительной ткани и брюшной жидкости. До лечения это окружение уже смещено в пользу рака: мало агрессивных цитотоксических Т‑клеток и много клеток, подавляющих иммунную атаку. Команда проанализировала ранее опубликованные данные одно‑клеточного РНК‑секвенирования от женщин с высокозлокачественным серозным раком яичников, сравнив образцы до и после неоадъювантной химиотерапии (химиотерапия, проведённая до операции). Они обнаружили, что химиотерапия не просто убивает опухолевые клетки; она также временно пробуждает иммунную активность, усиливая сигналы, связанные со стимуляцией Т‑клеток и воспалением, и одновременно снижая часть регуляторных Т‑клеток, которые обычно подавляют атаку.
Когда полезные изменения становятся вредными
Несмотря на этот кратковременный подъём, большинство пациентов всё равно рецидивируют и становятся резистентны к платиновым препаратам, таким как цисплатин. Чтобы понять, почему, исследователи глубже изучили, как разные типы клеток общаются друг с другом после лечения. Они обнаружили, что химиотерапия сильно увеличивает экспрессию генов, вовлечённых в синтез простагландинов, в макрофагах, ассоциированных с опухолью, и фибробластах, а также усиливает взаимодействие между этими клетками и Т‑клетками. С помощью продвинутых математических инструментов они показали, что общее окружение смещается в сторону провоспалительного, но в конечном счёте подавляющего состояния, с ростом уровня хемокинов, привлекающих миелоидные клетки, и усилением путей, которые со временем «истощают» Т‑клетки. Это навело на мысль, что простагландины могут действовать как молекулярный переключатель, превращая первоначально полезный иммунный всплеск в длительный тормоз противоопухолевого иммунитета.
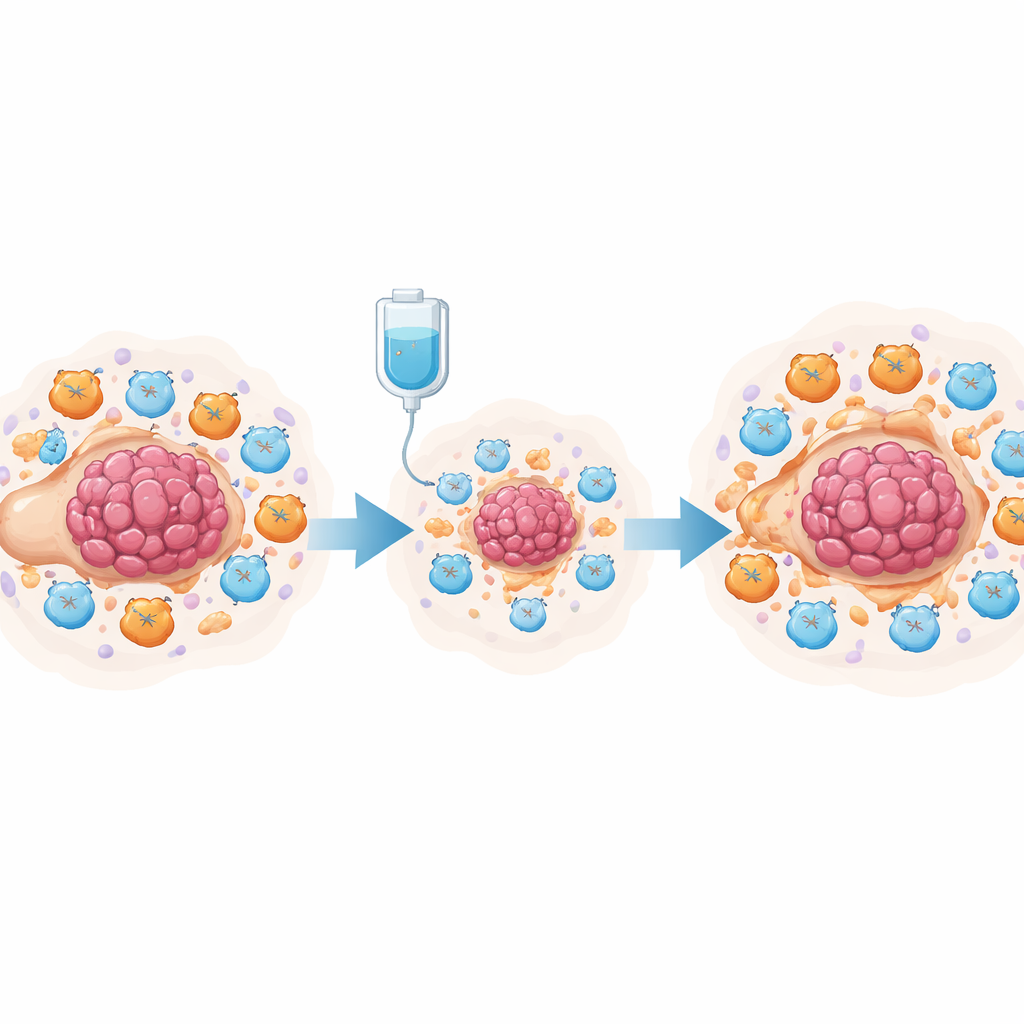
Химиотерапия, простагландины и подавленные Т‑клетки
Чтобы экспериментально проверить эту гипотезу, команда использовала модель рака яичников у мышей, лечившихся цисплатином. Анализ одно‑клеточных данных десятков тысяч клеток из брюшной полости показал, что цисплатин уменьшал количество опухолевых клеток и увеличивал общее число Т‑клеток, но при этом заметно расширялся пул миелоидных иммунорегуляторных клеток (MDSC) и «истощённых» цитотоксических Т‑клеток. Как опухолевые клетки, так и эти супрессивные клетки продуцировали высокий уровень ферментов синтеза простагландинов. В совместных культурах цисплатин‑лечёные опухолевые клетки вызывали у костномозговых клеток состояние, подобное MDSC, и ослабляли активность и пролиферацию CD8+ цитотоксических Т‑клеток. Исследователи проследили этот эффект до сигнального пути NF‑κB в опухолевых клетках, который включал ген PTGES — ключевой этап в производстве простагландина E2. Блокировка этого пути снижала уровни PTGES и выработку простагландинов.
Переломить ситуацию комбинированной терапией
Самый практичный вопрос заключался в том, может ли блокада простагландинов усилить эффект химиотерапии. У мышей учёные использовали генетическое удаление Ptges в опухолевых клетках, антитела, нейтрализующие простагландин E2, или низкомолекулярные ингибиторы простагландин‑E‑синтетазы. Все эти подходы снижали уровень простагландинов, уменьшали накопление MDSC и восстанавливали способность CD8+ Т‑клеток к убийству и их стволоподобную устойчивость. В сочетании с цисплатином или со стандартной схемой цисплатин‑паклитаксел ингибиторы простагландинов замедляли рост и метастазирование опухоли эффективнее, чем только химиотерапия. Данные указывают на то, что индуцируемое простагландинами иммунное подавление — не побочный эпизод, а ключевая причина побега опухолей после первоначального ответа.
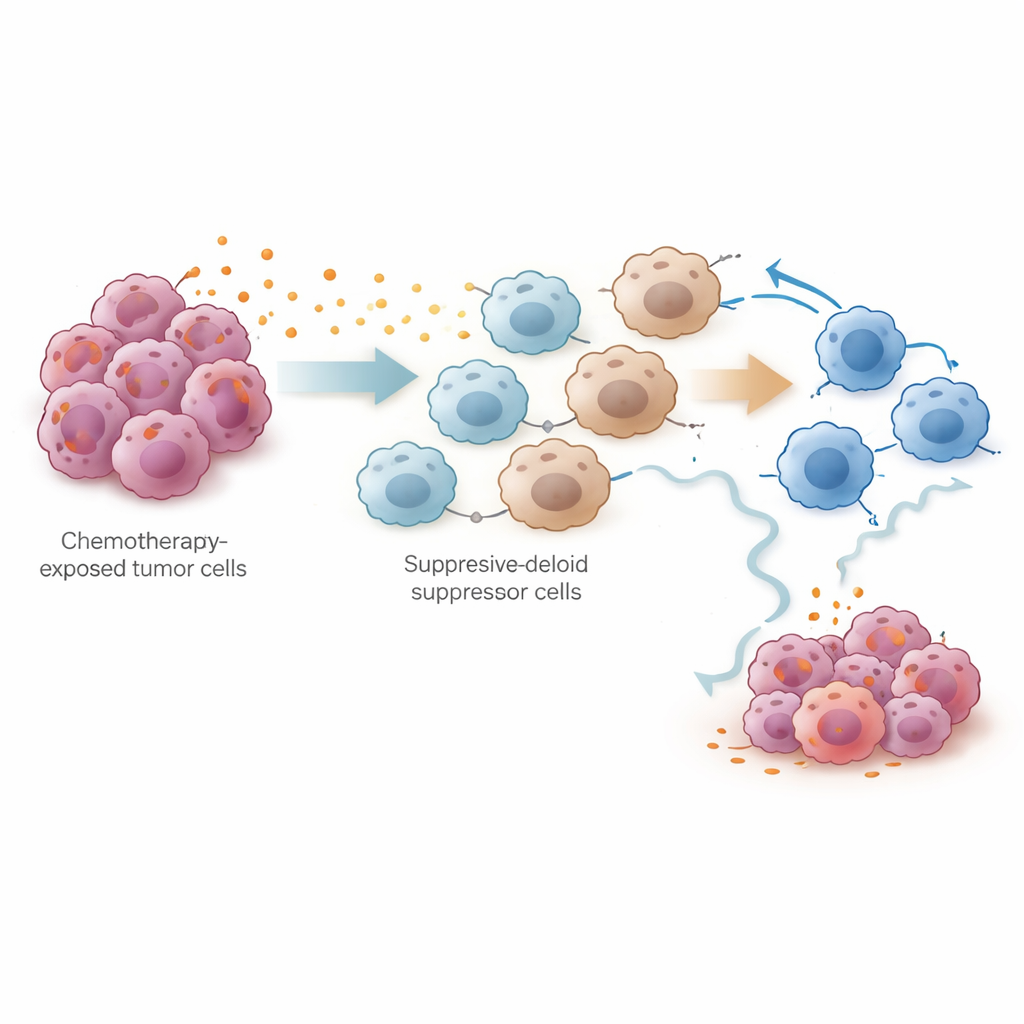
Новый подход к поддержанию эффективности лечения
Проще говоря, эта работа показывает, что химиотерапия меняет окружение опухоли в две фазы: сначала она ослабляет рак и кратковременно мобилизует иммунную систему, но затем вызывает волну простагландинов, которая привлекает супрессивные клетки и утомляет природные противоопухолевые силы организма. Выявив PTGES‑опосредованное производство простагландинов как ключевого виновника, исследование указывает на реальную стратегию: сочетание стандартной платиновой химиотерапии с препаратами, блокирующими пути простагландинов, может помочь поддерживать мощную иммунную атаку и отсрочить или предотвратить рецидив при раке яичников. Хотя требуются клинические испытания, такой комбинированный подход предлагает обнадеживающее направление для продления пользы от существующих методов лечения.
Цитирование: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Ключевые слова: рак яичников, микроокружение опухоли, резистентность к химиотерапии, простагландины, иммунотерапия