Clear Sky Science · ru
Состояние метилирования белковой фосфатазы 2A влияет на альфа-синуклеинопатию в мышиных моделях
Почему это важно для здоровья мозга
Болезнь Паркинсона и родственные расстройства постепенно лишают людей движения, памяти и независимости. Основной виновник — белок мозга альфа-синуклеин, который может неправильно сворачиваться, слипаться и повреждать нейроны. В этом исследовании ставится обнадеживающий вопрос: вместо того чтобы атаковать сам белок, можно ли настроить собственные механизмы очистки мозга, чтобы не допустить превращения альфа-синуклеина в токсичную форму?
История о липком белке
При болезни Паркинсона и деменции с телами Леви внутри нейронов накапливаются скрученные скопления альфа-синуклеина, образующие характерные «тела Леви». Особая химическая метка на этом белке, добавленная в одной позиции, называемой серином 129, тесно связана с его наиболее вредной формой. При избытке этой метки альфа-синуклеин с большей вероятностью формирует жесткие фибриллы и агрегаты. В норме мозг балансирует такие метки с помощью ферментов, которые их накладывают, и других, которые их снимают. Поскольку многие ферменты могут добавлять метку, блокировка лишь одного из них вряд ли будет эффективной. Поэтому авторы сосредоточились на основной семье ферментов, снимающих метку — белковой фосфатазе 2A (PP2A), действующей как молекулярный ластик для этой опасной модификации.
Ластик мозга и его два переключателя
PP2A по умолчанию не работает на полную мощность. Ее активность зависит от небольшой химической метки — метилирования — на одном из субъединиц. Два других белка управляют этим переключателем: LCMT-1 добавляет метку и переводит PP2A в более активную, защитную форму, а PME-1 снимает метку и сдвигает PP2A в менее активное, вредоносное состояние. Ранние работы на тканях человеческого мозга показали, что при болезни Паркинсона и деменции с телами Леви уровень LCMT-1 обычно снижен, а PME-1 повышен, в результате чего PP2A ослаблена. В настоящем исследовании прямо проверяют, что происходит, когда эти переключатели намеренно смещают в ту или иную сторону в живых мышах с патологией альфа-синуклеина.
Проверка равновесия в живом мозге
Исследователи использовали две дополняющие друг друга мышиные модели. В одной мыши были генетически модифицированы так, чтобы в мозге производился человеческий альфа-синуклеин; с возрастом у них постепенно образуются белковые скопления и возникают двигательные и когнитивные нарушения. Этих животных дополнительно модифицировали так, чтобы они чрезмерно экспрессировали либо PME-1 («выключатель» PP2A), либо LCMT-1 («включатель» PP2A) в нейронах переднего мозга. Во второй модели команда вводила заранее собранные фибриллы альфа-синуклеина в стриатум — глубокую область мозга, участвующую в контроле движений. Эти фибриллы выступают в роли семян, привлекают нормальный альфа-синуклеин и в течение месяцев распространяют патологию у иначе нормальных или модифицированных по ферментам мышей. В обеих моделях ученые измеряли накопление белка, состояние нейронов, воспаление мозга и поведение животных.
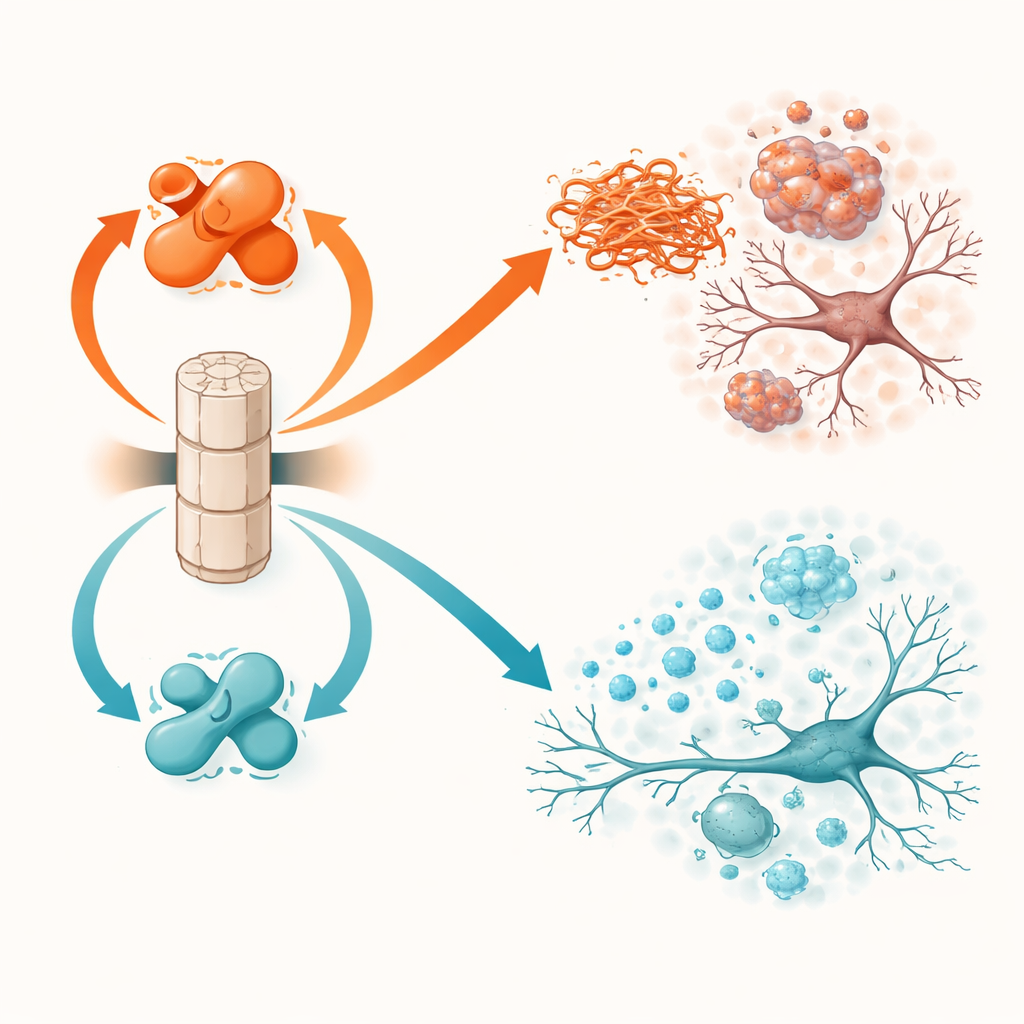
Когда ластик слабеет, повреждение распространяется
Мыши с повышенной экспрессией PME-1 и, следовательно, со сниженной активностью PP2A, чувствовали себя хуже. У трансгенных животных с альфа-синуклеином усиление PME-1 приводило к большему числу меток и агрегатов альфа-синуклеина в коре и гиппокампе, сильнее выраженной утрате нейронной структуры, ослаблению сигналов нейрональной активности и более выраженной активации иммунных клеток мозга. Эти изменения отражались в худшей работоспособности на двигательных тестах и заданиях на обучение и память. В модели с введением фибрилл сверхэкспрессия PME-1 позволяла токсичным сборкам альфа-синуклеина накапливаться и распространяться более широко, особенно в дофаминергические нейроны черной субстанции (substantia nigra) — ключевой области, утрачиваемой при болезни Паркинсона. У таких мышей наблюдалась более выраженная потеря дофаминовых волокон, интенсивное воспаление и более сильные нарушения моторики и укладывания в гнездо.
Включая ластик снова
Обратная манипуляция — повышенная экспрессия LCMT-1, поддерживающая PP2A в сильно метилированном и активном состоянии — имела в целом защитный эффект. У трансгенных мышей с альфа-синуклеином LCMT-1 уменьшал нагрузку меток и агрегированного белка почти до нормальных уровней и сохранял как структуру, так и активность нейронов. Маркеры воспаления были ниже, а поведение животных в тестах равновесия и памяти приближалось к показателям здоровых контрольных особей. В модели с фибриллярным заражением LCMT-1 ограничивал как локальное накопление, так и отдаленное распространение токсичного альфа-синуклеина, сохранял дофаминовые нейроны от дегенерации, снижал активацию микроглии и смягчал падение моторной координации и поведения при гнездовании. Во всех экспериментах сдвиг PP2A в активное, метилированное состояние последовательно превращал молекулярные преимущества в функциональную защиту.
Что это может значить для будущих лечебных подходов
Для неспециалистов вывод прост: у мозга есть встроенный «ластик», который может снимать вредную метку с альфа-синуклеина и не допускать его превращения в опасные комки. Когда этот ластик ослаблен, повреждение, воспаление и симптомы усиливаются; когда он усилен, нейроны защищены. Исследование дает прямое доказательство в живых животных того, что состояние метилирования PP2A является ключевым регулятором токсичности альфа-синуклеина и ее последствий. Это указывает на новую терапевтическую стратегию: вместо охоты за каждой вредной формой белка можно разработать препараты, которые сдвинут PP2A и его регуляторы LCMT-1 и PME-1 в более защитное состояние. Такие подходы потребуют тщательной проверки безопасности, но они дают надежду на замедление или предотвращение болезни Паркинсона и родственных состояний за счет восстановления собственной способности мозга контролировать альфа-синуклеин.
Цитирование: Maddila, S., Hassanzadeh, K., Liu, J. et al. Protein phosphatase 2A methylation state impacts α-synucleinopathy in mouse models. Cell Death Discov. 12, 172 (2026). https://doi.org/10.1038/s41420-026-03045-7
Ключевые слова: Болезнь Паркинсона, альфа-синуклеин, белковая фосфатаза 2A, нейродегенерация, воспаление мозга