Clear Sky Science · ru
Эпигенетический контекст определяет транскрипционную активность канонического и неканонического сигнального пути NF-κB при раке поджелудочной железы
Почему это исследование важно для пациентов
Рак поджелудочной железы — один из самых смертоносных видов рака, частично потому, что его клетки прекрасно «читают» и реагируют на сигналы опасности в окружении. В этом исследовании рассматривают два таких сигнала — TNFα и TWEAK — и показывают, как они запускают разные «режимы чтения» в ДНК раковых клеток. Понимание этих режимов может открыть новые пути для замедления роста опухоли, ограничения её распространения и повышения эффективности лечения.
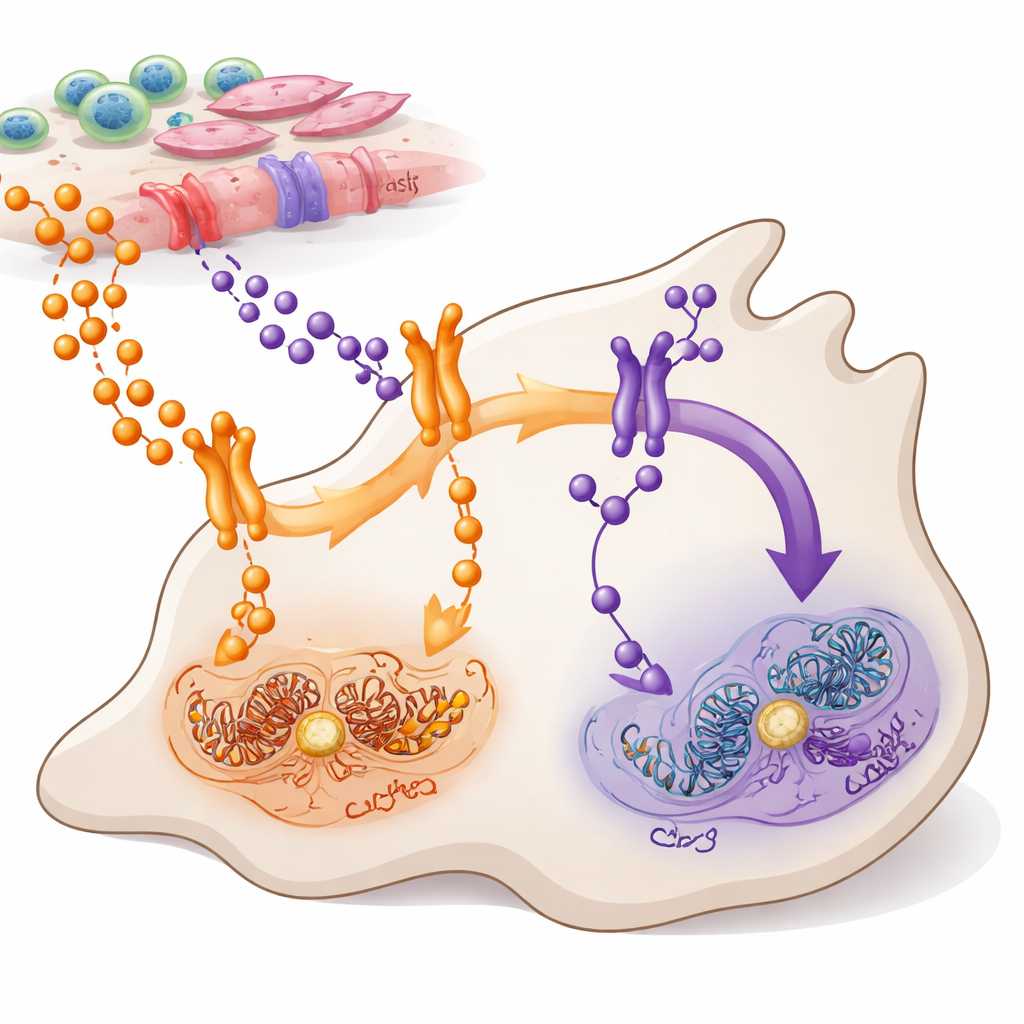
Два маршрута сообщений в раковые клетки
TNFα и TWEAK — это небольшие белковые сигналы, которые выделяют клетки внутри и вокруг опухоли. Оба они передают сведения в крупную управляющую систему внутри клеток, известную как NF-κB, которая помогает решать, расти клетке, мигрировать или погибнуть. Авторы сосредоточились на аденокарциноме протоков поджелудочной железы — наиболее распространённой и агрессивной форме рака поджелудочной железы, где NF-κB аномально активен в большинстве опухолей. Они картировали, какие клетки производят TNFα и TWEAK, какие клетки несут их рецепторы и как эти сигналы проходят через два связанных ветвления NF-κB — часто называемые каноническим (через RELA) и неканоническим (через RELB) путями.
Кто посылает сигналы в окрестностях опухоли
Объединив данные одноклеточного РНК-секвенирования тысяч клеток из опухолей пациентов с продвинутой микроскопией, команда обнаружила, что TNFα в основном выделяется иммунными клетками, особенно макрофагами и определёнными T- и B-клетками. TWEAK, напротив, продуцируется более широким кругом клеток: макрофагами, фибробластами, эндотелиальными клетками и звездчатыми клетками (stellate cells). Их рецепторы тоже различаются. Опухолевые клетки и прилегающие фибробласты сильно экспрессируют основной рецептор TNFα и ключевой рецептор TWEAK. Сетевой анализ показал, что сигналы, основанные на TWEAK, формируют более широкую и сложную сеть общения между опухолевыми и поддерживающими клетками, в то время как TNFα действует более локально в зонах, богатых иммунными клетками.
Разная глубина ответов внутри раковых клеток
В линиях клеток рака поджелудочной железы исследователи обрабатывали клетки TNFα или TWEAK и измеряли, какие гены включаются со временем. TNFα вызвал быструю и широкую волну генетической активности, связанную с воспалением, клеточной миграцией, ремоделированием ткани и выживанием. TWEAK индуцировал меньший, более медленный набор изменений, который в основном перекрывался с мишенями TNFα, а не запускал уникальную программу. Оба сигнала могли усиливать миграцию клеток и, в определённых условиях, запускать клеточную смерть, но TNFα сильнее влиял на подвижность. При анализе данных пациентов из The Cancer Genome Atlas авторы обнаружили, что опухоли с высоким уровнем TNFα или высокими уровнями TWEAK разделяют множество активированных генов, что подтверждает эти закономерности в реальном человеческом материале.
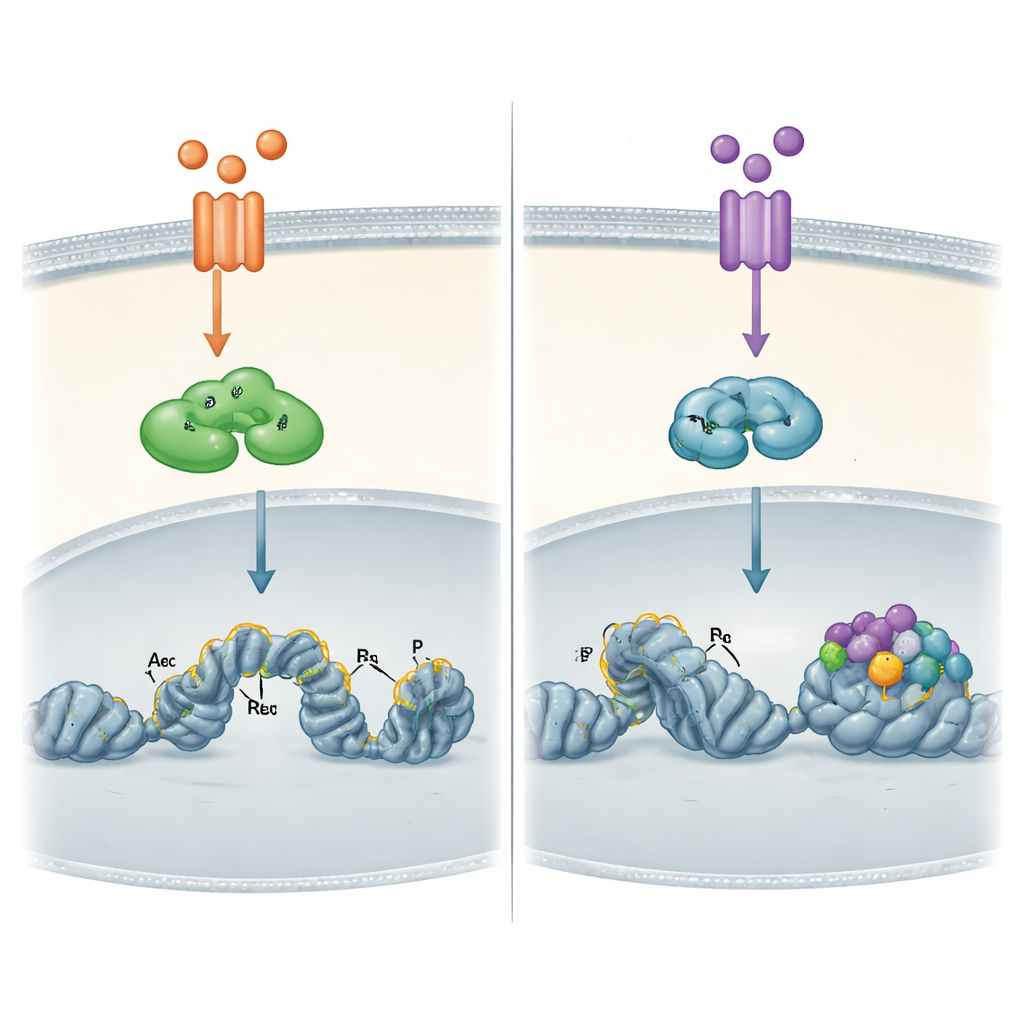
Как ландшафт ДНК формирует каждый путь
Самые поразительные различия стали очевидны при прямом изучении хроматина раковых клеток — упакованной формы ДНК и связанных с ней белков. С помощью картирования связывания по всему геному авторы показали, что RELA, активируемый TNFα, может связываться не только с уже открытыми областями ДНК, но и с более плотными участками, после чего способствовать их «открытию», добавляя химические метки, связанные с активными переключателями. RELB, включаемый позже TWEAK, связывался почти исключительно с уже доступными сайтами, украшенными такими активными метками. Эти сайты RELB были особенно богаты докинговыми мотивами для другой семьи факторов, AP-1, что указывает на зависимость RELB от других белков, которые «подготавливают почву» перед его действием.
Что это значит для будущих методов лечения
Для неспециалиста главный вывод таков: TNFα и TWEAK используют один и тот же инструментарий NF-κB очень по-разному. TNFα через RELA действует как главный переключатель, способный распахивать закрытые участки ДНК раковой клетки и активировать широкий спектр генов, вовлечённых в рост, выживание и распространение. TWEAK через RELB больше похож на специалиста, который может действовать только там, где ДНК уже открыта и присутствуют ко-факторы, такие как AP-1. Такое разделение функций предполагает, что препараты, нацеленные на ремоделирование хроматина, AP-1 или конкретные ветви NF-κB, могут выборочно подавлять вредоносные генетические программы при раке поджелудочной железы, сохраняя при этом другие функции более нетронутыми.
Цитирование: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Ключевые слова: рак поджелудочной железы, сигнализация NF-kappaB, опухолевый микроокружение, эпигенетическая регуляция, TNF и TWEAK