Clear Sky Science · ru
Использование пироптоза в терапии рака молочной железы: иммунологические механизмы и новые стратегии на основе биоматериалов
Превращение гибели клеток в новое оружие против рака молочной железы
Рак молочной железы по-прежнему остается одним из самых распространенных и упорных видов рака в мире. Многие опухоли со временем обходят хирургическое вмешательство, химиотерапию и даже современные методы иммунной терапии. В этом обзоре рассматривается новая идея: намеренное вызвание огненной формы гибели клеток — пироптоза — внутри опухолей молочной железы. Заставляя раковые клетки контролируемо разрываться с воспалением, ученые надеются как напрямую уничтожать опухоль, так и пробуждать иммунную систему для совместной атаки.
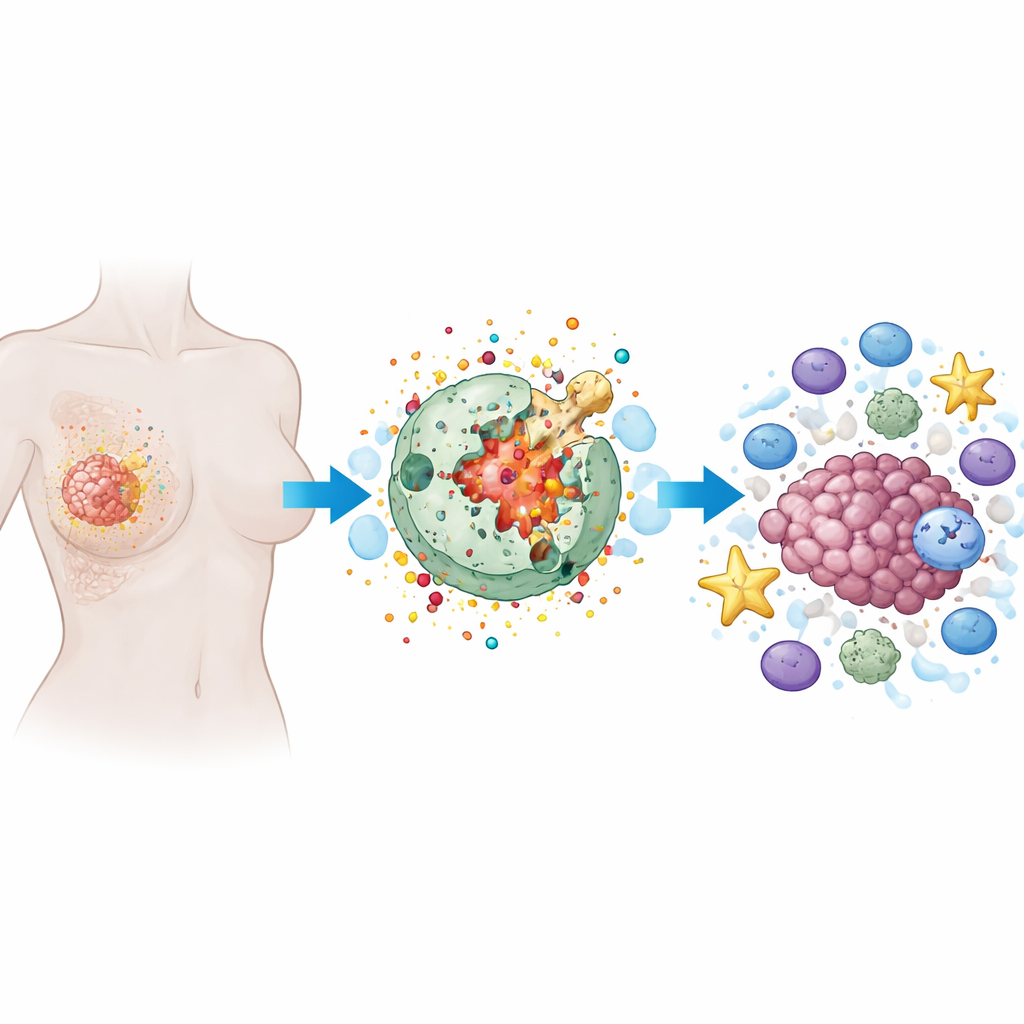
Как работает огненная форма гибели клеток
Пироптоз — это программируемая форма гибели клеток, при которой клетка набухает, её наружная мембрана покрывается порами и в конечном итоге разрывается, выпуская своё содержимое. В отличие от тихой, аккуратной смерти клеток, наблюдаемой при многих терапиях, пироптоз шумный и воспалительный. Специализированные белки, особенно семейство газдерминов, действуют как крошечные зарядные устройства. После расщепления внутренними ферментами газдермины проделывают отверстия в мембране клетки. Это не только уничтожает раковую клетку, но и высвобождает сигналы тревоги и воспалительные молекулы, которые могут призывать и активировать клетки иммунной системы.
Почему опухоли молочной железы представляют особую сложность
Рак молочной железы — не одно заболевание, а совокупность подтипов с разным поведением. Некоторые, например тройной отрицательный рак молочной железы, лишены общих мишеней для лекарств и часто устойчивы к лечению. Многие опухоли молочной железы считаются «иммунологически холодными», то есть в них мало активных иммунных клеток. В обзоре объясняется, как особенности микроокружения опухоли молочной железы — включая стромальные клетки, иммуносупрессивные клетки и локальную нехватку кислорода — могут одновременно создавать предпосылки для пироптоза и, при плохом контроле, превращать его воспаление в топливо для роста и распространения опухоли. Такая двусмысленность требует особенно тщательной точности.
Газдерминовые переключатели внутри опухолевых клеток
Центральная идея статьи — то, как разные белки газдерминов действуют как молекулярные переключатели внутри раковых клеток молочной железы. Варианты, такие как GSDMD и GSDME, способны преобразовывать сигналы от химиотерапии, облучения или атакующих иммунных клеток в полноценный пироптоз. Другие, например GSDMC и некоторые формы GSDMB, часто повышены в агрессивных опухолях и могут как способствовать, так и сдерживать болезнь в зависимости от того, как они активируются. Во многих раках молочной железы GSDME химически «замолкает», что притупляет пироптоз и активацию иммунитета. Восстановление или селективное запускание нужных газдерминов может определить, приведёт ли терапия лишь к гибели нескольких клеток или превратит всю опухоль в вакцину in situ, сигнализирующую иммунной системе.
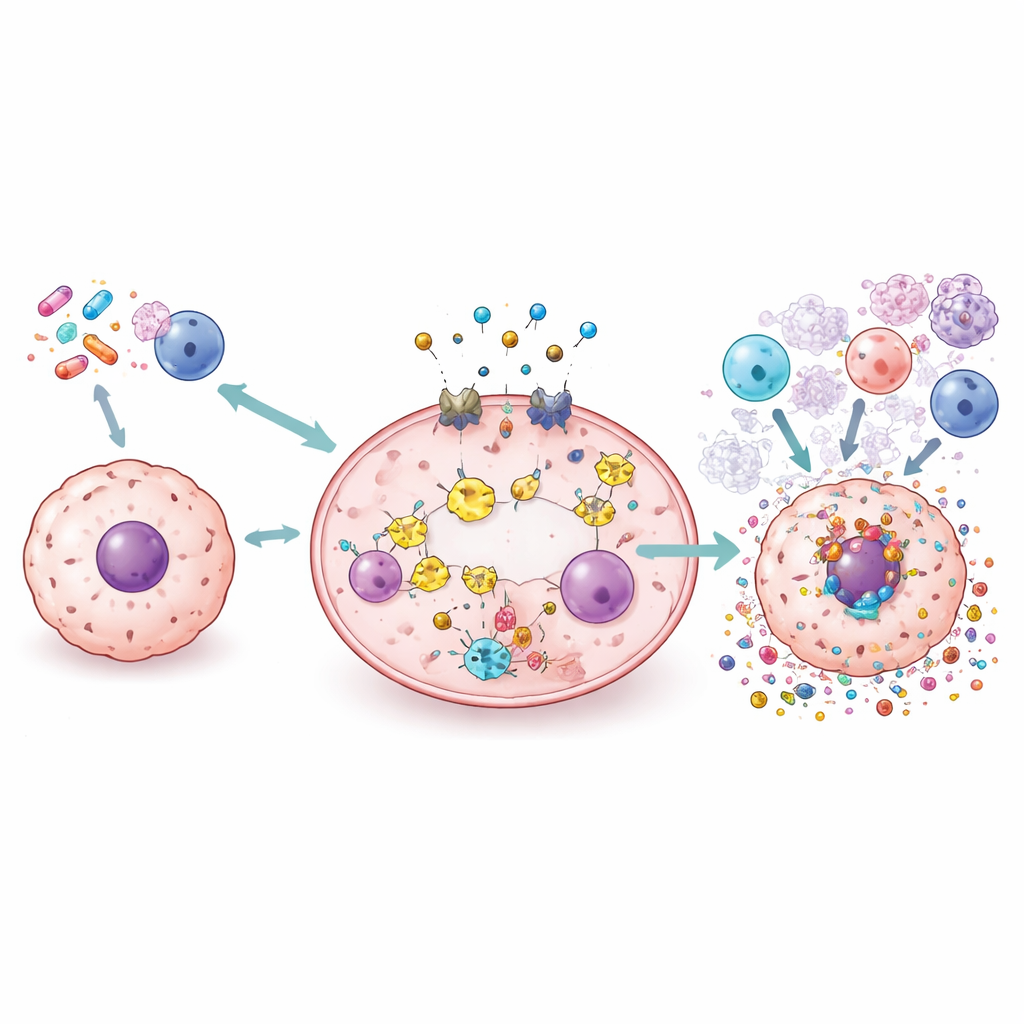
Новые инструменты: лекарства, наночастицы, вирусы и облучение
В обзоре представлен широкий спектр подходов, изучаемых для безопасного использования пироптоза. Стандартные препараты, такие как цисплатин и доксорубицин, могут быть переориентированы или реформулированы так, чтобы склонять раковые клетки к газдермин-зависимому разрыву вместо тихой смерти. Малые молекулы могут либо усиливать, либо блокировать части пути, чтобы тонко настраивать воспаление. Наночастицы и биомиметические носители разрабатываются для доставки химиопрепаратов, ионов меди или светочувствительных молекул непосредственно в опухоль, где они вызывают пироптоз, щадя здоровые ткани. Онколитические вирусы и радиотерапия также могут быть сконструированы или сочетаемы с другими агентами для провокации пироптоза и перестройки иммунного ландшафта опухоли, потенциально делая ингибиторы контрольных точек иммунитета более эффективными.
Баланс между мощной пользой и реальными рисками
Поскольку пироптоз столь воспалителен, те же реакции, которые помогают иммунной системе бороться с раком, могут также повреждать нормальные ткани или даже способствовать росту опухоли, если становятся хроническими. Авторы выделяют ранние биомаркеры — такие как генетические сигнатуры, паттерны метилирования, фрагменты белков газдерминов в крови и профили цитокинов — которые могут помочь определить, какие пациенты с наибольшей вероятностью получат пользу и кто находится в группе повышенного риска опасных «цитокиновых штормов». Продвинутые конструкции наномедицины, тщательно подобранные комбинации препаратов и мониторинг маркеров воспаления в реальном времени исследуются для того, чтобы держать ответ сильным, но контролируемым.
Что это может значить для будущих пациентов
Проще говоря, в обзоре утверждается, что заставлять раковые клетки «умирать громко» может изменить уход за больными раком молочной железы. Вызывая пироптоз в точно выбранном подмножестве опухолевых клеток, врачи могут как уменьшить размер опухоли, так и пробудить мощный, длительный иммунный ответ, делая холодные опухоли теплыми и более отзывчивыми на современные иммунотерапии. Однако пироптоз — нестабильный союзник: при слишком широком или продолжительном высвобождении он может усугубить воспаление или поощрить рост устойчивых клеток. Будущие исследования будут сосредоточены на том, кто получит пользу, совершенствовании целевых систем доставки и проведении клинических испытаний, которые сочетают подходы, индуцирующие пироптоз, с иммунными препаратами. Если эти задачи удастся решить, использование пироптоза может добавить мощное новое измерение в лечение рака молочной железы.
Цитирование: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Ключевые слова: пироптоз, рак молочной железы, газдермин, микроокружение опухоли, наномедицина