Clear Sky Science · ru
Абсолютная динамика и относительная статика: взаимосвязь гликолиза и ОФЭФ (OXPHOS) в развитии рака
Почему выбор энергии у рака имеет значение
Раковые клетки похожи на экстремальных спортсменов на выносливость: им постоянно нужно подпитываться, чтобы расти, распространяться и избегать лечения. В этом обзоре объясняется, как опухолевые клетки используют две основные энергетические системы — одну быструю и одну эффективную — и, что важнее, как они комбинируют и переключаются между ними. Понимание этих сменяющихся энергетических стратегий открывает новый взгляд на диагностику и лечение рака на протяжении всего течения болезни.
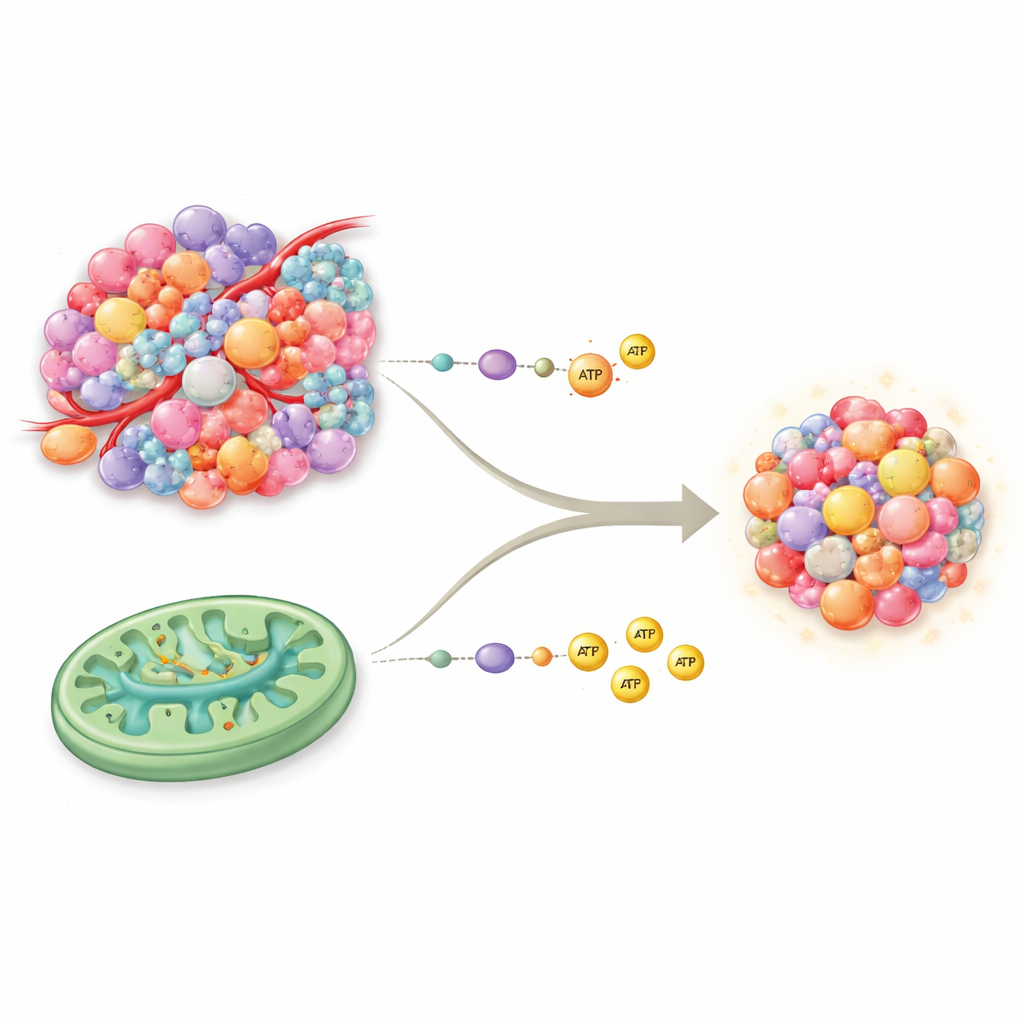
Два основных пути выработки энергии в клетке
Наши клетки обычно получают энергию двумя основными путями. Гликолиз — быстрый, «наличный» механизм, который быстро расщепляет сахар, но даёт сравнительно мало энергии на единицу. Окислительное фосфорилирование, или ОФЭФ (OXPHOS), проходит в митохондриях и работает как высокоэффективная электростанция: оно производит значительно больше энергии, но требует достаточного снабжения кислородом и питательными веществами. Десятилетиями считалось, что рак почти исключительно полагается на гликолиз даже при наличии кислорода — явление, известное как эффект Варбурга. Новые данные опрокидывают это упрощённое представление: во многих опухолях митохондрии полностью функционируют, и клетки могут использовать ОФЭФ и цикл трикарбоновых кислот (TCA) наряду с гликолизом, что предоставляет им более богатый и гибкий набор энергетических инструментов, чем считалось ранее.
Множество типов клеток — множество топливных решений
Опухоль — это не однородная масса. Это небольшой экосистемный комплекс, содержащий раковые клетки, вспомогательные клетки, кровеносные сосуды и иммунные клетки, каждая из которых имеет свои потребности в топливе. Некоторые раковые клетки находятся близко к сосудам и получают много кислорода и питательных веществ; другие погружены в плохо снабжаемые участки. В результате клетки внутри одной и той же опухоли могут предпочитать гликолиз, преимущественно полагаться на ОФЭФ или использовать оба пути одновременно. Такая метаболическая вариабельность — гетерогенность — возникает из различий в кровоснабжении, уровне питательных веществ, типе клеток и сигналах окружающей среды. К тому же опухоли часто демонстрируют метаболический симбиоз: гликолитические клетки экспортируют лактат как «отход», который соседние ОФЭФ-зависимые клетки импортируют и сжигают как ценное топливо. Похожий обмен лактатом происходит между раковыми клетками и поддерживающими клетками, например фибробластами, клетками сосудов и иммунодепрессивными клетками, что в совокупности помогает опухоли выживать и сопротивляться терапии.
Постоянные изменения: как энергетика опухоли меняется со временем
Метаболизм опухоли не только разнообразен в любой момент времени; он также чрезвычайно динамичен. По мере роста опухоли условия вокруг неё изменяются: возникает гипоксия, накапливается кислотность, иссякают питательные вещества, меняется жёсткость ткани. В суровых условиях с низким содержанием кислорода многие раковые клетки смещаются в сторону гликолиза. При накоплении кислот или голодании по сахару они могут вернуться к более интенсивному использованию ОФЭФ. Та же гибкость проявляется в ключевые биологические моменты. Быстро делящиеся клетки полагаются на гликолиз для генерации строительных блоков для ДНК, липидов и мембран. Покойные или циркулирующие в крови клетки часто зависят больше от ОФЭФ. В процессе инвазии и метастазирования раковые клетки многократно подстраивают свой выбор топлива: на некоторых этапах выигрывает гликолиз, на других — ОФЭФ, а метастатические клетки, осваивающие новые органы, подстраивают метаболизм под «почву» ткани-мишени.
Гены, ферменты и «электростанции», управляющие переключением
В глубине клеточной машины гены и ферменты направляют эти энергетические решения. Онкогены и супрессоры опухолей могут смещать клетки в сторону гликолиза или ОФЭФ, либо позволять им усиливать оба пути. Мутации или изменения в ключевых ферментах TCA, например в тех, что обрабатывают цитрат, сукцинат или изоцитрат, могут наклонить равновесие и иногда запускать сигналы, способствующие опухолеобразованию, такие как рост сосудов и инвазия. Ферменты, находящиеся в критических развилках — например пируваткиназа M2, которая помогает решать, станет ли углерод из сахара источником энергии или строительным материалом — связывают гликолиз и митохондриальную функцию. В то же время различия в количестве, структуре и работоспособности митохондрий в разных областях опухоли ещё больше расширяют спектр возможных энергетических состояний.
Переосмысление лечения через призму подвижной энергетической мишени
Поскольку опухолевые клетки способны переключаться между гликолизом и ОФЭФ, простая блокада одного пути зачастую оказывается недостаточной: рак может перенаправить потребление топлива и выжить. Авторы утверждают, что энергетический метаболизм в раке лишь кратковременно стабилен и по сути постоянно меняется. Они предлагают рассматривать опухоли как находящиеся на «спектре энергетического метаболизма», который нужно измерять во времени, а не однократно. На практике это может означать отслеживание топливных предпочтений опухоли на разных этапах болезни и подбор сочетаний ингибиторов гликолиза и ОФЭФ в индивидуализированном режиме. Такие динамические стратегии, основанные на метаболизме, могли бы эффективнее отрезать питание опухоли, ограничивать её адаптивность и улучшать долгосрочный контроль за болезнью.
Цитирование: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Ключевые слова: метаболизм рака, гликолиз, окислительное фосфорилирование, микроокружение опухоли, метаболическая пластичность