Clear Sky Science · ru
APOA2-опосредованный эндотелиально-мезенхимальный переход и перепрограммирование липидного метаболизма опухоли обеспечивают резистентность к антиангиогенной терапии через TGF-β
Почему это открытие важно для пациентов
Врачи все чаще применяют препараты, которые «голодают» опухоли печени, перекрывая им кровоснабжение, но у многих пациентов после первоначального эффекта рак перестает отвечать на лечение. В этом исследовании ставится актуальный вопрос: почему некоторые раки печени становятся резистентными к терапии, блокирующей сосуды, и как этого можно избежать? Авторы выявляют скрытое взаимодействие между белком крови, переносящим жиры, и мощным фактором роста, которое позволяет опухолям перепрограммировать и свои сосуды, и энергетический метаболизм, указывая на новый подход к лечению трудно излечимого рака.
Опухоль, которая научилась жить без привычного источника жизни
Гепатоцеллюлярная карцинома, наиболее частая форма рака печени, сильно зависит от новых кровеносных сосудов для роста. Стандартные препараты при распространенном заболевании нацелены на блокировку ключевого пути неоваскуляризации, централизованного вокруг VEGF и его рецептора VEGFR2. Тем не менее у многих пациентов опухоли продолжают прогрессировать, несмотря на эти лекарства. Сравнив образцы опухолей пациентов, ответивших и не ответивших на антиангиогенный препарат апатиниб, авторы обнаружили, что один ген, APOA2, выделялся особенно ярко. У опухолей у резистентных пациентов уровни APOA2 были значительно повышены — белка, прежде всего известного своей ролью в транспортировке жиров в крови. Это навело на мысль, что APOA2 может помогать опухолям ускользать от препаратов, нацеленных на сосуды.
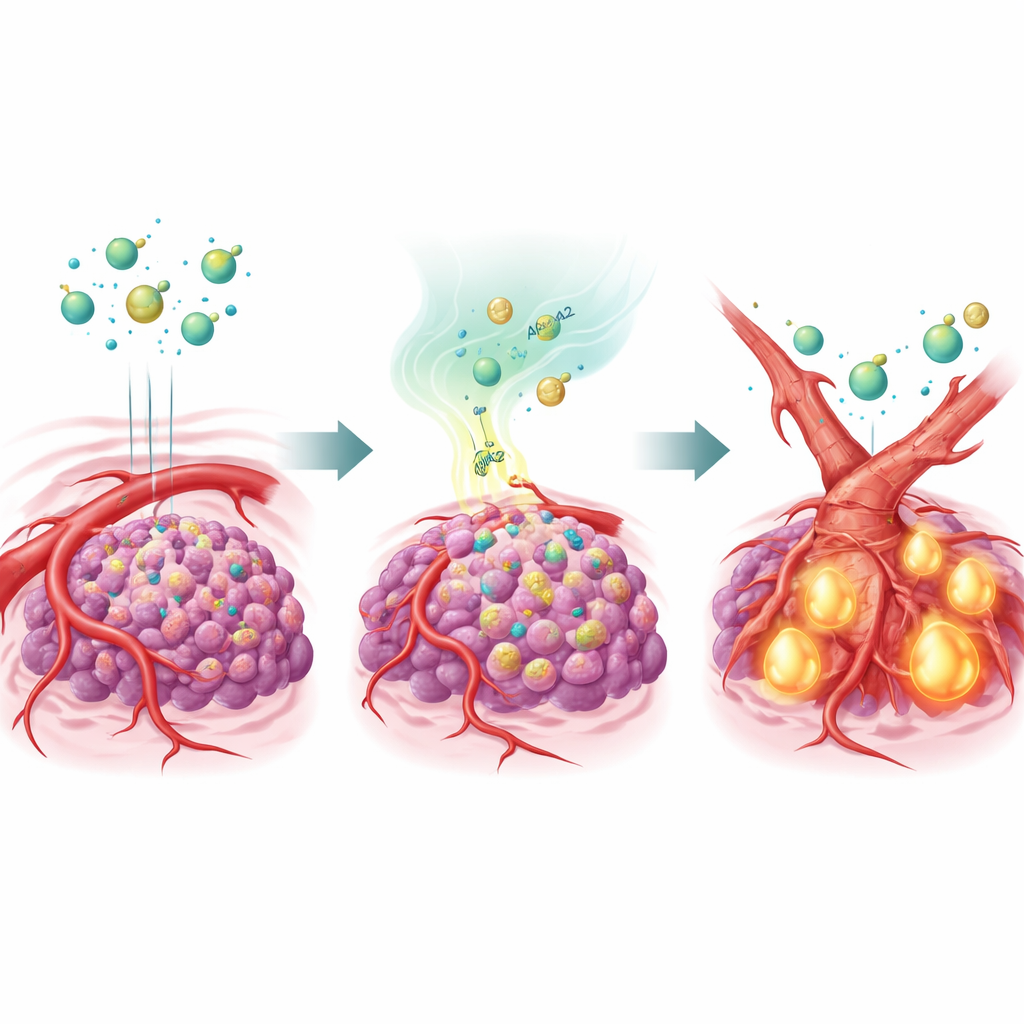
Белок транспортировки жиров, который перестраивает сосуды
Чтобы проверить эту идею, команда модифицировала клетки рака печени так, чтобы они перепроизводили APOA2, и имплантировала их мышам. При лечении несколькими антиангиогенными препаратами такие опухоли с высоким уровнем APOA2 в значительной степени игнорировали терапию: их сосуды сохранялись, а опухоли продолжали расти. Детальный анализ показал, что в этих опухолях был существенно активирован главный сигнал — TGF-β, уровни которого были повышены как в микроокружении опухоли, так и в крови животных. TGF-β воздействовал на клетки, выстилающие сосуды, заставляя их менять идентичность в процессе, называемом эндотелиально-мезенхимальным переходом. По мере перехода к более рубцоподобному, мезенхимальному состоянию эти клетки теряли большую часть VEGFR2 — той самой мишени, за которую «хватались» антиангиогенные препараты. По сути, сосуды перестраивались в форму, недоступную для действия этих лекарств.
Метаболический объезд, который поддерживает питание опухоли
История не закончилась на стенке сосуда. Тот же сигнал TGF-β, стимулируемый APOA2, также перепрограммировал то, как клетки опухоли получают энергию. Вместо того чтобы опираться главным образом на распад сахаров, клетки с высоким уровнем APOA2 стали поглощать больше свободных жирных кислот из окружения и окислять их в митохондриях через бета-окисление жирных кислот. Эксперименты по измерению использования нутриентов и потребления кислорода показали, что эти клетки стали больше зависеть от жиров как источника энергии и производили больше клеточного топлива (АТФ). Этот сдвиг позволял опухолевым клеткам продолжать активно делиться и избегать гибели, даже когда кровоснабжение было под давлением антиангиогенной терапии.
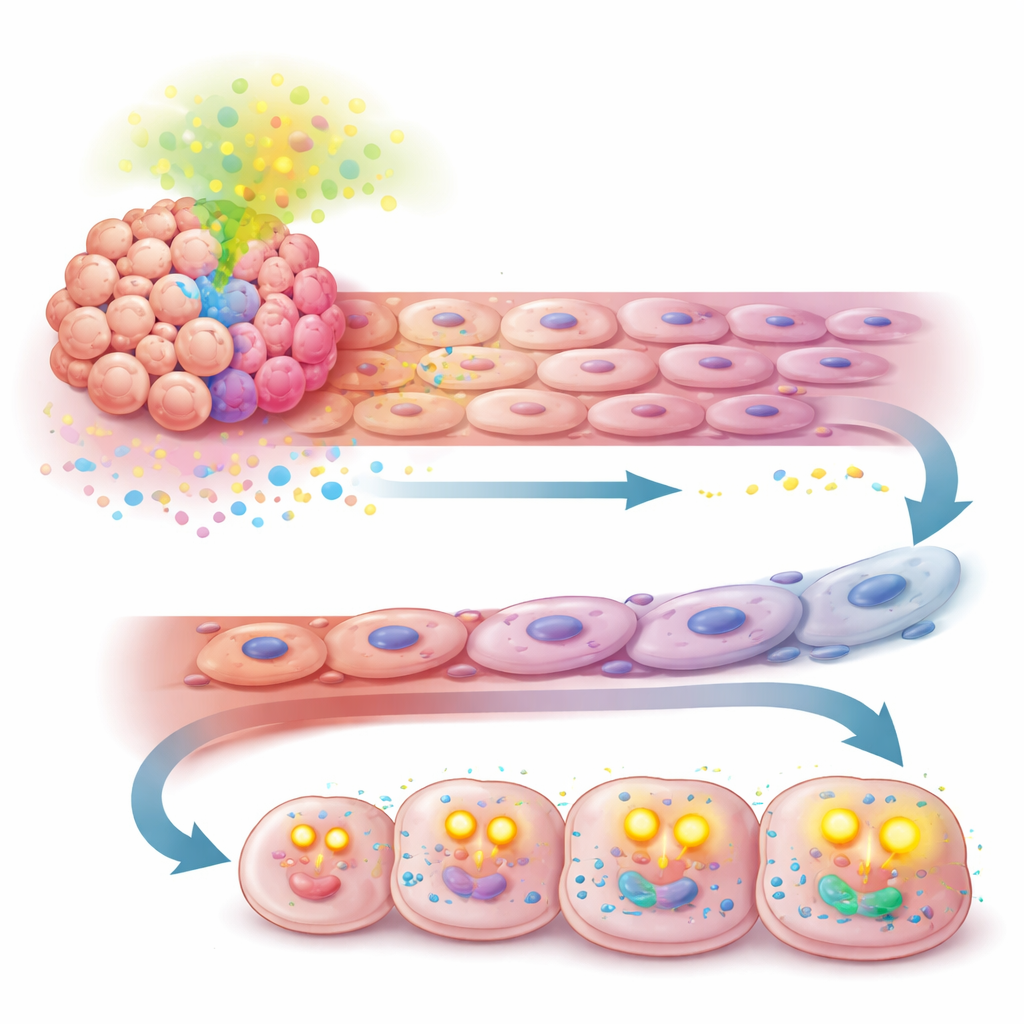
Преобразование уязвимости в новую терапевтическую мишень
Критически важно, что при блокировании TGF-β преимущества, обеспечиваемые APOA2, исчезали. Ингибирование этого сигнала в моделях на мышах снижало аномальные изменения сосудов, восстанавливало чувствительность к терапии и замедляло рост опухоли. Еще более перспективным оказалось лекарство в виде двойной антитела, которое одновременно блокирует TGF-β и иммунный контрольный пункт PD-1: оно работало лучше, чем любой из подходов по отдельности, в опухолях с высоким APOA2. Эти результаты указывают, что в подгруппе раков печени с повышенным APOA2 заболевание тихо переключилось с привычного пути VEGF на маршрут, центрированный вокруг TGF-β, который поддерживает и сосуды, и метаболизм опухоли.
Что это значит для будущего лечения рака печени
Для непрофессионала основное сообщение таково: некоторые опухоли печени ускользают от действующих препаратов против сосудов, перепрограммируя как «водопровод», так и «энергоснабжение». Ассоциированный с липидами белок APOA2 усиливает сигнал TGF-β, который, в свою очередь, маскирует сосуды так, что существующие препараты их не замечают, и учит раковые клетки жить за счет жиров вместо сахара. Исследование предполагает, что тестирование опухолей на APOA2 может выявить пациентов, которым стандартные антиангиогенные препараты вряд ли помогут, но которые могли бы ответить на лекарства, блокирующие TGF-β, особенно в сочетании с современной иммунотерапией. Коротко говоря, раскрывая механизмы адаптации опухолей, эта работа указывает на более индивидуализированную стратегию, атакующую и сосуды, и источник энергии, от которого зависят эти стойкие раки.
Цитирование: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Ключевые слова: гепатоцеллюлярная карцинома, резистентность к антиангиогенной терапии, APOA2, сигнализация TGF-бета, липидный метаболизм рака