Clear Sky Science · ru
KCTD1 стабилизирует c-Myc, увеличивает экспрессию PD-L1 и подавляет противоопухолевый иммунитет при гепатоцеллюлярной карциноме
Почему это важно для будущей терапии рака
Многие люди с раком печени не получают пользы от самых перспективных современных иммунотерапий, направленных на мобилизацию собственных Т‑клеток организма против опухоли. В этом исследовании изучают, почему основная форма рака печени — гепатоцеллюлярная карцинома — все еще может уклоняться от иммунной атаки даже при лечении, и выявляют новый молекулярный переключатель, называемый KCTD1, который может повысить эффективность существующих препаратов иммунотерапии.
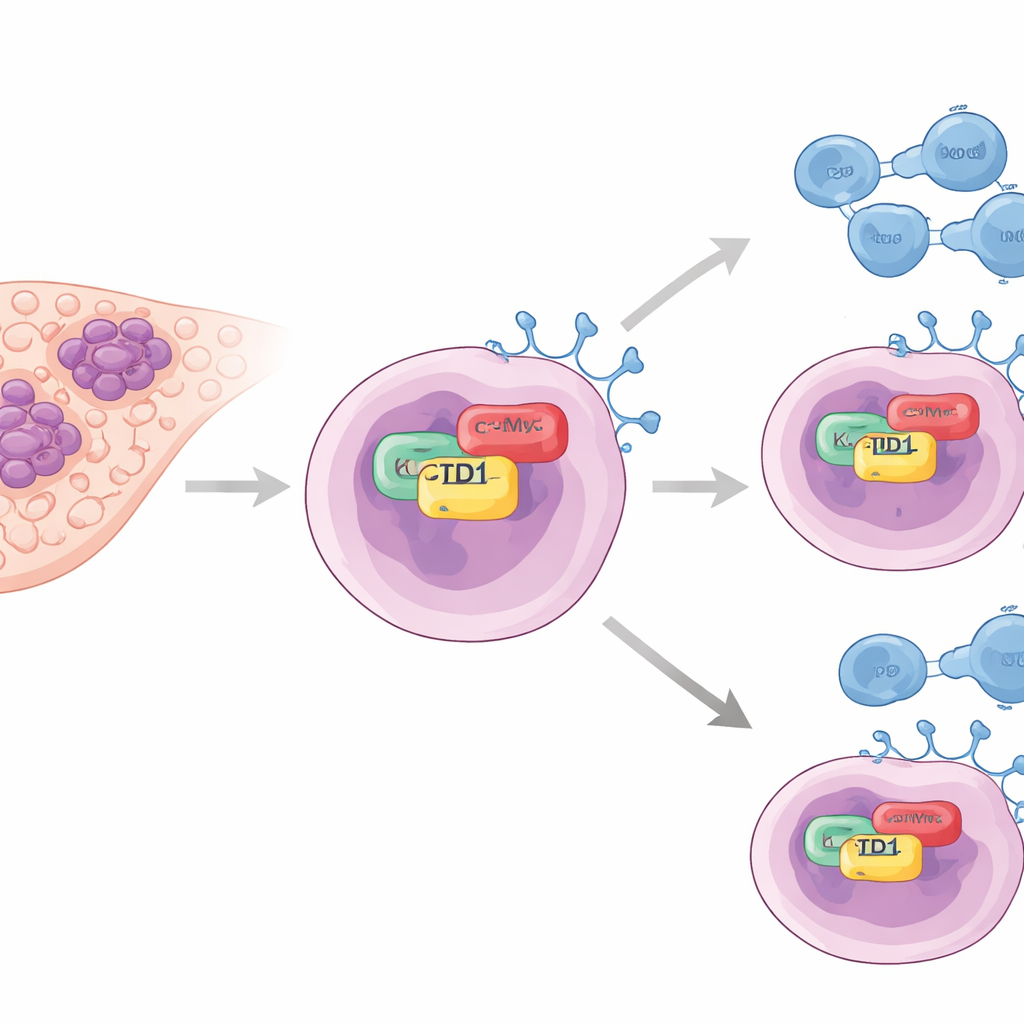
Скрытый помощник «выключателей» иммунитета опухоли
Авторы сосредоточили внимание на белке KCTD1, ранее связанном с ростом опухоли печени, но плохо изученном в контексте иммунного ухода. В образцах опухолей пациентов уровни KCTD1 были значительно выше в раковой ткани по сравнению с нормальной печенью. Важно, что опухоли с высоким содержанием KCTD1 также имели повышенную экспрессию PD-L1 — поверхностного белка на раковых клетках, который связывается с PD-1 на Т‑клетках и фактически приказывает иммунной системе притормозить ответ. У пациентов с более низким уровнем KCTD1 в опухоли выживаемость была лучше, что указывает на связь этого белка с тяжестью заболевания и силой иммунного «щитa» опухоли.
Соединяя молекулярные точки внутри раковых клеток
Чтобы понять, как KCTD1 усиливает PD-L1, команда использовала линии клеток рака печени, выращенные в лаборатории. При снижении уровня KCTD1 белок PD-L1 уменьшался, а оставшийся PD-L1 быстрее распадался, что указывает на то, что KCTD1 помогает стабилизировать PD-L1, а не только включает его ген. С помощью биохимических вытягивающих экспериментов и флуоресцентной микроскопии показали, что KCTD1 физически связывается с другим ключевым драйвером рака — онкобелком c-Myc — внутри ядра клетки. Это взаимодействие осуществляется через специфические контактные участки на обоих белках и ведет к более стабильному c-Myc, что, в свою очередь, усиливает выработку PD-L1. Когда c-Myc уменьшали самостоятельно, PD-L1 падал даже при наличии большого количества KCTD1, что ставит c-Myc в роль критического промежуточного звена в цепочке KCTD1–c-Myc–PD-L1.
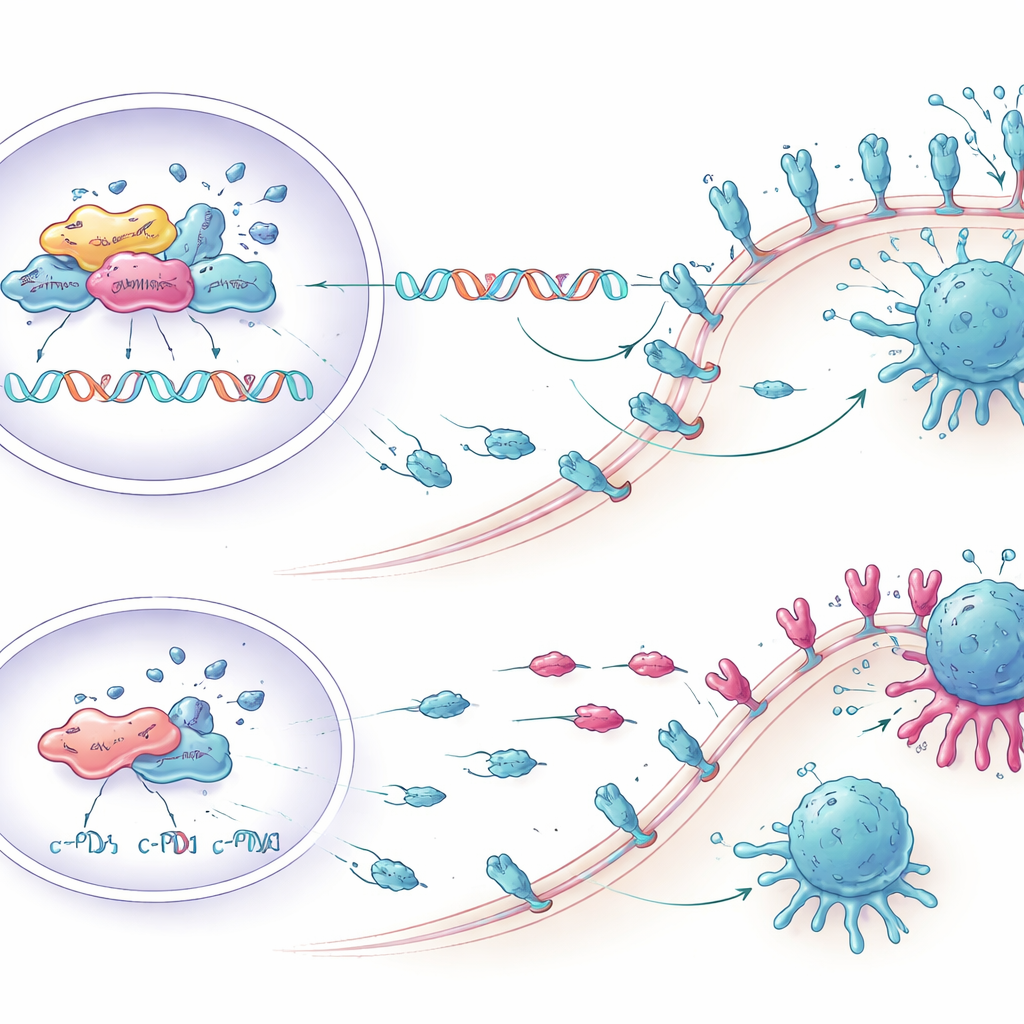
«Пробуждение» Т‑клеток в культуре
Затем исследователи проверили, может ли снижение KCTD1 реально усилить иммунную атаку. Они совместно культивировали человеческие клетки рака печени с иммунными клетками, взятыми у доноров крови. Опухолевые клетки с пониженным уровнем KCTD1 и, следовательно, PD-L1 вызывали более сильный отклик CD8 Т‑клеток — основных убийц опухолевых клеток в иммунной системе. Больше Т‑клеток вырабатывало провоспалительные молекулы, такие как TNF-α и интерферон‑гамма, демонстрировали повышенные маркеры пролиферации и активации и меньше признаков истощения. В результате при подавлении KCTD1 больше опухолевых клеток проходило через программируемую смерть, что показывает, что молекулярные изменения привели к реальному усилению иммунного уничтожения опухоли.
Проверка механизма на мышах
Чтобы выяснить, сохраняется ли та же картина в живом организме, команда внедрила мышиные клетки рака печени с дефицитом KCTD1 прямо в печень мышей. Опухоли с пониженным KCTD1 формировали меньшее и меньшее по размеру количество узелков, демонстрировали более медленную клеточную пролиферацию и больше клеток, проходящих апоптотическое разрушение. В этих опухолях также наблюдали сниженные уровни c-Myc и PD-L1. Удаление CD8 Т‑клеток у мышей устраняло большую часть этого эффекта, что указывает на то, что замедление роста опухоли в значительной мере зависело от активности Т‑клеток. Наконец, сочетание нокдауна KCTD1 с анти‑PD‑1 антителом — существующим препаратом, блокирующим контрольные точки иммунитета — дало наименьшую опухолевую нагрузку и самый высокий уровень инфильтрации опухоли CD4 и CD8 Т‑клетками.
Что это может значить для пациентов
В совокупности результаты показывают, что KCTD1 является центральным коорднатором, который стабилизирует c-Myc, усиливает экспрессию PD-L1 на клетках рака печени и ослабляет атаку CD8 Т‑клеток. Нарушение этого пути делает опухоли более уязвимыми для иммунной системы и более отзывчивыми на препараты, блокирующие PD-1, у мышей. Для пациентов это означает, что в будущем препараты, нацеленные на KCTD1 или на контактную поверхность между ним и c-Myc, могли бы использоваться в комбинации с текущими иммунотерапиями, чтобы больше людей с раком печени получили пользу от долговременного иммунного контроля заболевания.
Цитирование: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Ключевые слова: гепатоцеллюлярная карцинома, онкоиммунная терапия, путь PD-1 PD-L1, сигналинг c-Myc, Т-клеточный противоопухолевый иммунитет