Clear Sky Science · ru
Молекулярные механизмы противораковой активности силодозина: перспективная стратегия перепрофилирования при раке молочной железы
Почему старый препарат вновь привлекает внимание
Рак молочной железы остаётся одним из самых распространённых и смертельно опасных заболеваний у женщин, и у многих пациенток в конечном счёте исчерпываются эффективные варианты лечения. В этом исследовании проверяли, можно ли перепрофилировать силодозин — препарат, уже безопасно применяемый при урологических проблемах у мужчин — для борьбы с раком молочной железы. Поскольку это одобренный, доступный и с известным профилем безопасности препарат, доказательство его способности замедлять или уничтожать раковые клетки могло бы ускорить появление новых терапевтических подходов, особенно для людей с агрессивными формами болезни.
Знакомое лекарство в новой роли
Силодозин в настоящее время назначают для облегчения мочевых симптомов при увеличенной предстательной железе, он блокирует определённые нервные сигналы, называемые адренергическими. Эти сигналы управляют не только мышечной деятельностью; растущие данные указывают, что они также могут способствовать росту опухолей, их распространению и образованию новых сосудов. Авторы предположили, что силодозин может вмешиваться в эти вредоносные сигналы и в раковых клетках молочной железы. Они протестировали препарат на нескольких линиях человеческих раковых клеток молочной железы, выращенных в лаборатории — как чувствительных к гормонам, так и трудно поддающихся лечению тройных негативных — и сравнили его эффекты с влиянием на здоровые клетки молочной железы.
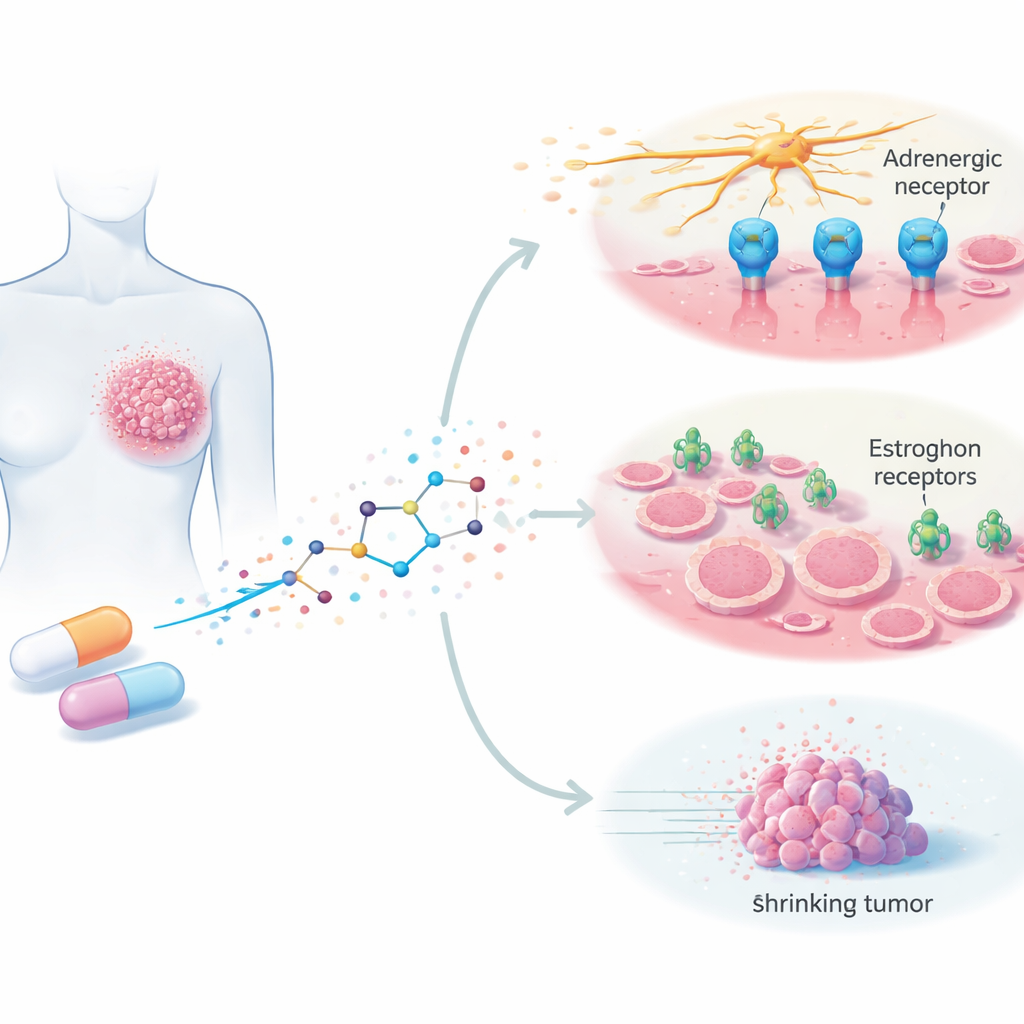
Замедление роста и индукция гибели клеток
При воздействии силодозином рост раковых клеток молочной железы замедлялся в зависимости от времени и дозы. Особенно чувствительными оказались гормон-чувствительные клетки, но даже агрессивные тройные негативные клетки продемонстрировали сниженную выживаемость и способность образовывать колонии со временем, тогда как нормальные клетки молочной железы в целом оставались менее затронутыми. Дальнейшие эксперименты показали внутриклеточные механизмы: силодозин задерживал клетки на ранней фазе клеточного цикла — последовательности шагов, необходимых для деления. Уменьшалась концентрация ключевых «стимулирующих» белков, продвигающих деление, тогда как «тормозные» белки и хорошо знакомый «страж» p53 увеличивались. Препарат также направлял раковые клетки на путь программируемой гибели, что подтверждалось растущей долей клеток с фрагментированной ДНК.
Блокирование миграции и 3D-роста, похожего на опухоль
Рак становится опасным для жизни, когда клетки мигрируют и образуют новые очаги в других местах. Используя модель «царапанья» в монослое клеток, исследователи обнаружили, что силодозин замедлял скорость, с которой как гормон-чувствительные, так и тройные негативные клетки могли заполнять образовавшийся зазор. Команда также использовала трёхмерные сфероиды — маленькие шаровидные скопления клеток, которые лучше имитируют реальные опухоли, чем плоские слои. Силодозин заметно снижал формирование и размеры этих сфероидов. Одновременно препарат понижал уровень E-кадгерина — молекулы, помогающей клеткам сцепляться друг с другом и участвующей в сигналах роста и выживания — что указывает на то, что нарушение клеточно-клеточных контактов может быть одним из способов, которыми препарат нарушает организацию опухоли и её распространение.
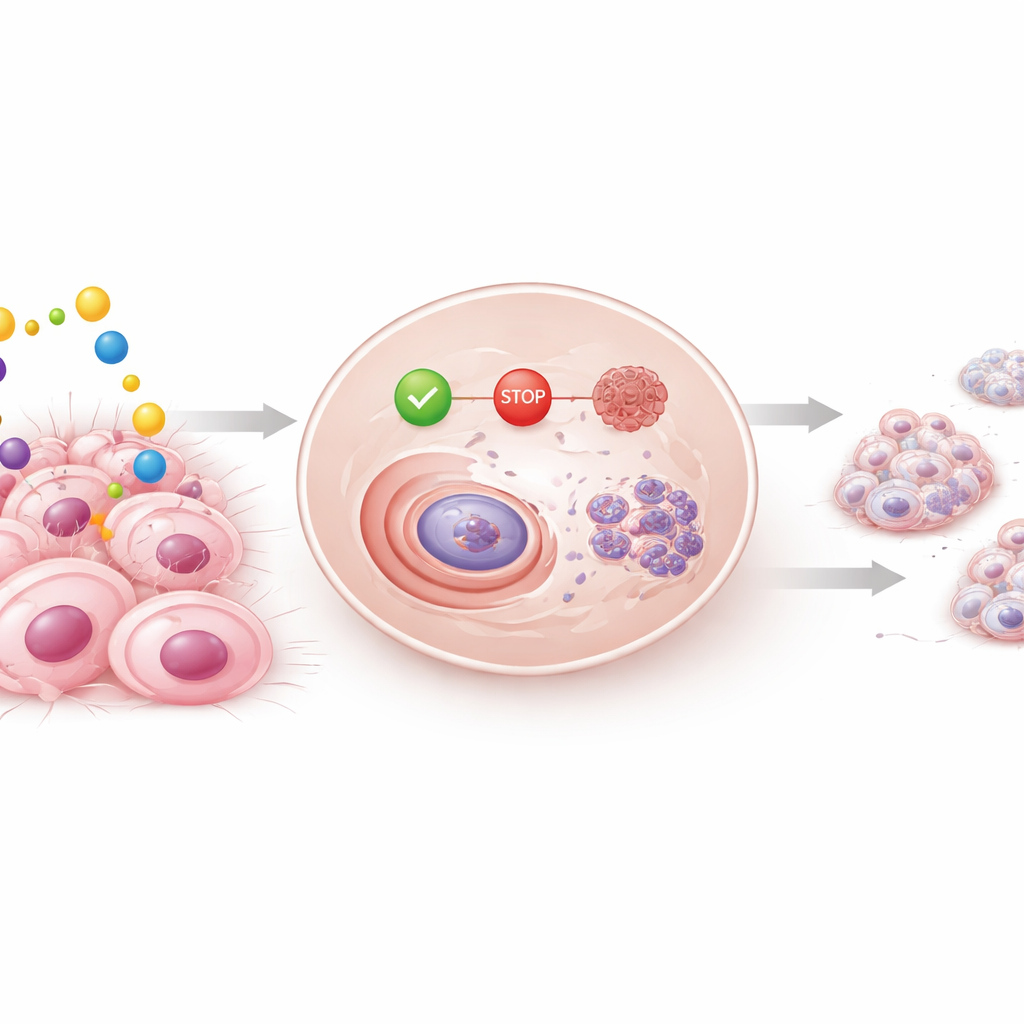
Неожиданная вторая мишень внутри клеток
Силодозин был разработан для блокирования адренергических рецепторов, но данные не укладывались в простую модель «только одна мишень». Некоторые раковые клетки молочной железы, которые сильно реагировали на препарат, имели мало или вовсе не выявляли тот адренергический рецептор, на который направлен силодозин, а клетки с большим количеством этого рецептора не всегда были более чувствительны. Чтобы найти другие возможные мишени, авторы использовали компьютерное моделирование, чтобы проверить, может ли силодозин также связываться с эстрогеновыми рецепторами — молекулярными переключателями, которые управляют многими опухолями молочной железы и являются основными целями препаратов вроде тамоксифена. Их симуляции показали, что силодозин способен прочно встраиваться в обе основные формы эстрогенового рецептора, взаимодействуя с теми же ключевыми контактными точками, что и тамоксифен. Это позволяет предположить, что силодозин может действовать как модулятор эстрогенового рецептора помимо блокирования нервосвязанных сигналов.
Что это может значить для пациентов
В совокупности эксперименты указывают на силодозин как на многоцелевого «нападающего» против раковых клеток молочной железы: он замедляет их рост, стимулирует автоликвидацию, препятствует их миграции и не позволяет организовываться в опухлеподобные сфероиды, при этом, вероятно, воздействуя на адренергические и эстрогенозависимые пути. Эффективные концентрации в культурах клеток выше, чем те, что достигаются у пациентов при стандартных урологических дозах, поэтому потребуются дополнительные исследования на животных и комбинированные подходы, чтобы оценить потенциал в реальной клинике. Тем не менее, поскольку силодозин уже одобрен и в целом хорошо переносится, это исследование создаёт основу для его перепрофилирования как части новых терапевтических стратегий, особенно для пациентов с ограниченными вариантами лечения, например при тройном негативном раке молочной железы.
Цитирование: Pellegrino, M., Occhiuzzi, M.A., Marra, M. et al. Molecular insights into Silodosin’s anti-cancer effects: a promising repurposing strategy for breast cancer. Cell Death Discov. 12, 128 (2026). https://doi.org/10.1038/s41420-026-02973-8
Ключевые слова: рак молочной железы, перепрофилирование лекарств, силодозин, эстрогеновый рецептор, тройной негативный рак молочной железы