Clear Sky Science · ru
Мультиомика выявляет гетерогенность и функциональные популяции предшественников олигодендроцитов, индуцированных человеческими нейрональными стволовыми клетками
Почему важно защищать «изоляцию» мозга
Проводящие пути мозга зависят от жирового покрытия, называемого миелином, которое обвивает нервные волокна подобно изоляции на электрических кабелях. Когда миелин повреждён, как при рассеянном склерозе и других заболеваниях, нервные сигналы замедляются или прерываются, вызывая нарушения движения, зрения и мыслительных функций. В этом исследовании рассматривается особая группа человеческих клеток, способных восстанавливать миелин, и задаётся практический вопрос: какие клетки лучше подходят для будущих клеточных терапий по ремонту этой важной «изоляции»?
От стартовых клеток мозга к строителям миелина
Исследователи начали с человеческих нейрональных стволовых клеток — универсальных стартовых клеток, полученных из фетальной ткани мозга, которые уже настроены на превращение в клетки нервной системы. В условиях лаборатории они направили эти стволовые клетки на дифференцировку в предшественники олигодендроцитов, или hOPC, которые являются прямыми предшественниками клеток, образующих миелин. Под микроскопом клетки изменили форму: от простых круглых они стали более сложными с множественными ветвями, а также включили характерные белки, отмечающие этапы на пути к зрелым миелинобразующим клеткам. Это обеспечило надёжный, относительно безопасный источник человеческих предшественников миелиновых клеток для детального анализа.
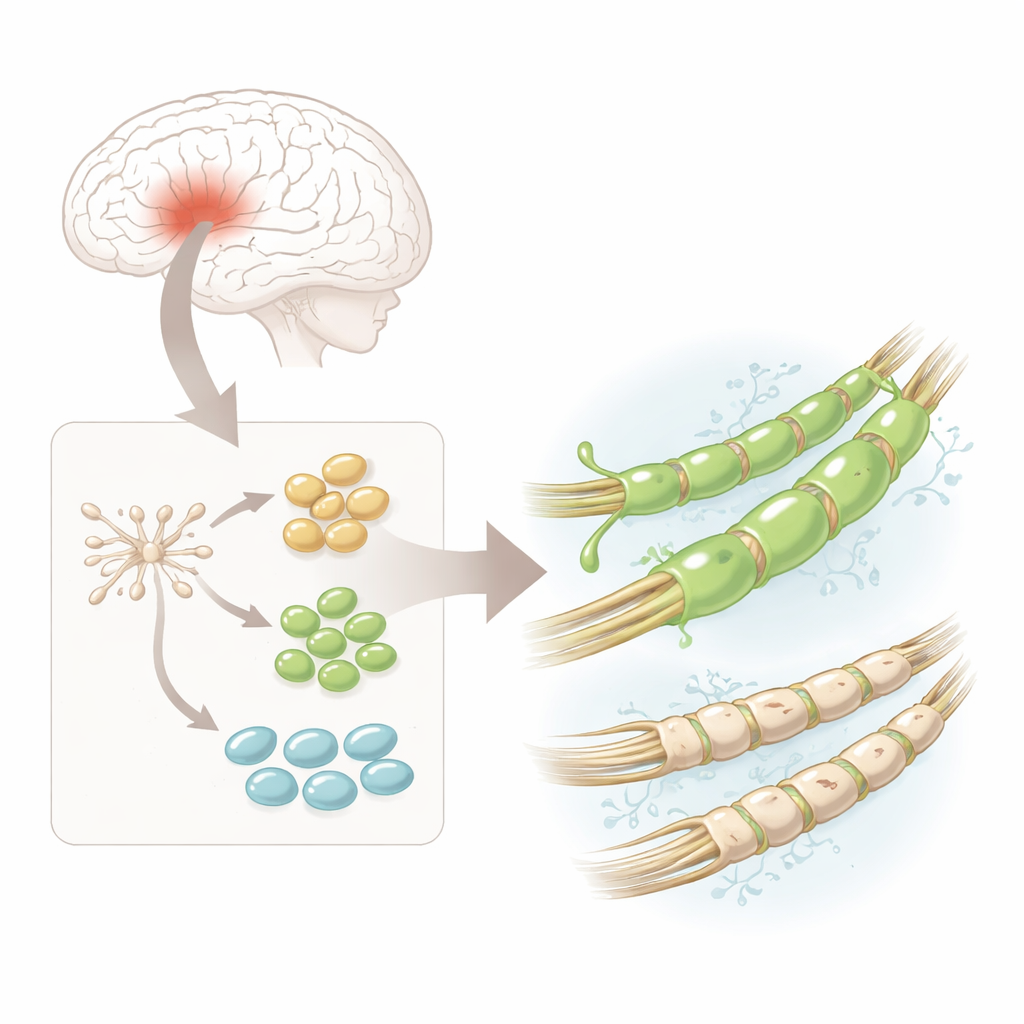
Одна популяция — множество скрытых вариаций
С помощью секвенирования РНК по одной клетке — метода, который показывает, какие гены активны в тысячах отдельных клеток — команда обнаружила, что hOPC вовсе не однородны. Вместо этого они сгруппировались в три основных стадии: ранние «пред-предшественники», более приверженные предшественники и клетки, приближающиеся к полной идентичности олигодендроцитов. На всех этих этапах выделялся один ген: PDGFRA, кодирующий рецептор на поверхности клетки. Очень чувствительный метод визуализации RNA-Scope подтвердил, что мРНК и белок PDGFRA встречаются в больших количествах по сравнению с другими ключевыми маркерами на каждой стадии, что указывает на то, что этот рецептор может определять особенно способные клетки для строительства миелина.
Отделение наиболее мощных клеток ремонта
Чтобы проверять эту гипотезу, учёные разделили hOPC на две группы в зависимости от наличия на поверхности рецептора PDGFR-α. Затем они сравнили PDGFR-α–положительные клетки, PDGFR-α–отрицательные клетки и несортированные клетки в серии функциональных тестов. После трансплантации в «шиверер»-мышей — животных, неспособных формировать нормальный миелин — PDGFR-α–положительные клетки образовывали более плотный, компактный миелин вокруг нервных волокон по сравнению с другими группами. Эти клетки также мигрировали дальше и быстрее делились в лабораторных тестах. Другими словами, популяция PDGFR-α–положительных клеток показала наибольшую активность в перемещении к нужным местам, увеличении численности и восстановлении «изоляции».
Внутриклеточные сигналы, стимулирующие рост и ремонт
Углубляя анализ, команда сравнила активность генов в PDGFR-α–положительных и –отрицательных клетках. Они обнаружили, что положительные клетки включают сети генов, связанные с ростом глиальных клеток и формированием миелина, а также несколько ключевых внутриклеточных сигнальных путей. Особенно выделялись два пути: PI3K–AKT–mTOR, давно связанный с ростом клеток и продукцией миелина, и сигнальная каскада TGF-β, влияющая на выбор судьбы молодых клеток мозга. Данные предполагали, что активация PDGFR-α передаёт сигнал через PI3K–AKT–mTOR, что в свою очередь усиливает сигналы, связанные с TGF-β, вместе подталкивая клетки к становлению эффективными строителями миелина.
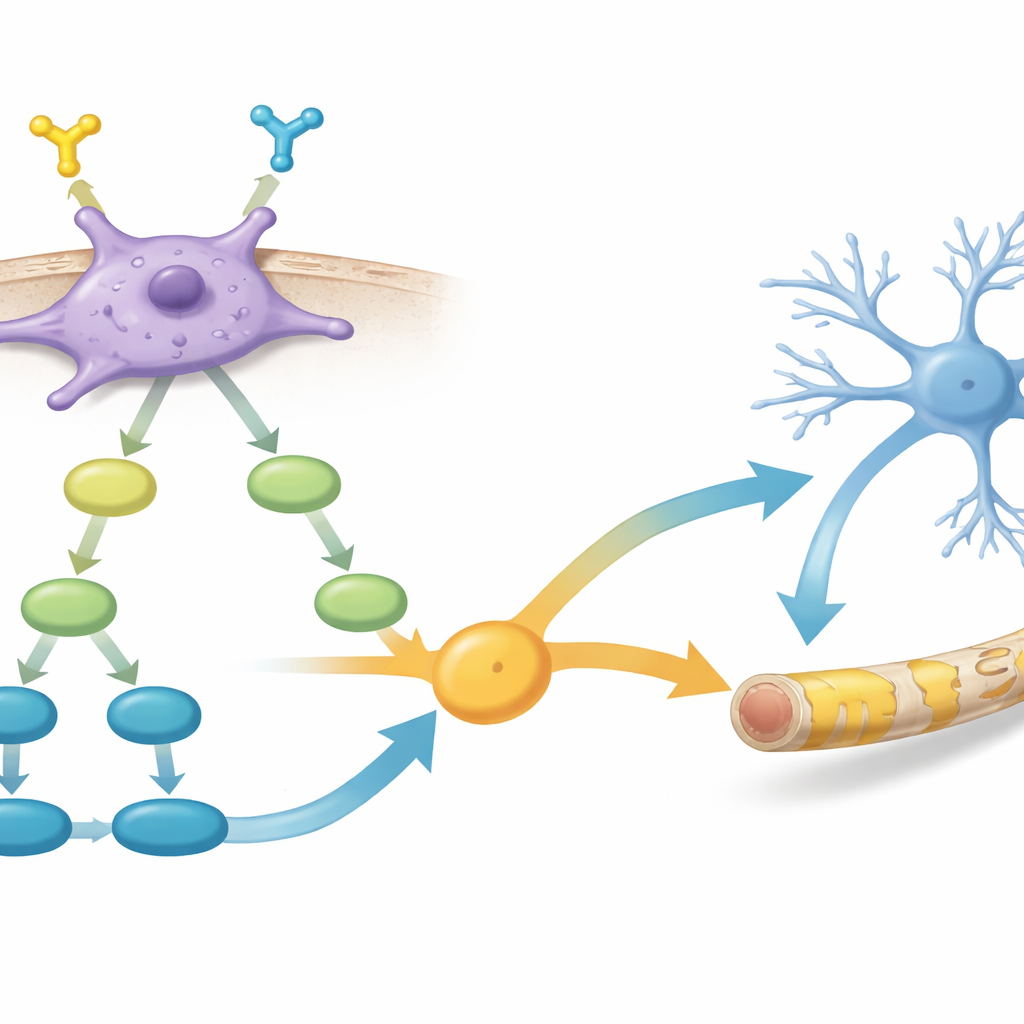
Усиление ремонта миелина с помощью химического помощника
Затем исследователи поинтересовались, можно ли ещё больше улучшить эти перспективные клетки. Они обработали PDGFR-α–положительные hOPC малой молекулой, активирующей путь TGF-β, и изучили как активность генов, так и поведение клеток. После обработки эти клетки продемонстрировали повышенный уровень нескольких генов, связанных с миелином, и образовали более толстые, более полные миелиновые оболочки при трансплантации в шиверер-мышей по сравнению с нелечеными PDGFR-α–положительными клетками. Это подтверждает идею, что точная настройка внутриклеточных сигналов в уже отобранных предшественниках может дополнительно улучшить их работу как живых инструментов для ремонта миелина.
Что это значит для будущих терапий
Для неспециалистов ключевое сообщение таково: не все предшественники миелина одинаковы. В сочетании мощных методов чтения генов и визуализации это исследование выделяет заметную подгруппу — PDGFR-α–положительные hOPC — которые лучше мигрируют, быстрее делятся и эффективнее восстанавливают миелин по сравнению со сверстниками. Оно также показывает внутриклеточные сигнальные пути, которые можно химически подкорректировать, чтобы сделать эти клетки ещё более эффективными. Вместе эти выводы прокладывают дорожную карту для разработки более безопасных и эффективных клеточных терапий по восстановлению «изоляции» мозга при заболеваниях, связанных с потерей миелина.
Цитирование: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Ключевые слова: ремонт миелина, предшественники олигодендроцитов, нейрональные стволовые клетки, клеточная терапия, считывание РНК по одной клетке